Với công thức tính số mol OH- trong bài toán thủy phân peptit Hoá học lớp 12 chi tiết nhất giúp học sinh dễ dàng nhớ toàn bộ các công thức tính số mol OH- trong bài toán thủy phân peptit từ đó biết cách làm bài tập Hoá học 12. Mời các bạn đón xem:
Công thức tính số mol OH- trong bài toán thủy phân peptit hay nhất – Hoá học lớp 12
Việc viết phương trình và tính theo phương trình bài toán thủy phân peptit rất mất thời gian khi giải trắc nghiệm. Vậy có cách nào để tính nhanh bài toán thủy phân peptit? Bài viết dưới đây sẽ giúp em hiểu rõ vấn đề này.
1. Công thức tính
– Phương trình thủy phân hoàn toàn peptit trong môi trường kiềm
n–peptit + (n – 1 + b)NaOH → n muối của ∝–amino axit + bH2O
Trong đó: b là tổng số nhóm – COOH còn tự do trong peptit (các nhóm –COOH không tạo liên kết peptit)
Ví dụ:
Gly–Glu–Gly + 4NaOH → 2H2N–CH2–COONa + NaOOC–(CH2)2–CH(NH2)–COONa + 2H2O
– Tỉ lệ mol:
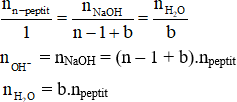
– Định luật bảo toàn khối lượng:
mpeptit + mNaOH = mmuối + m
– Bảo toàn gốc ∝–amino axit:
n một muối ∝–amino axit = (số lượng nhóm ∝–amino axit đó có mặt trong n–peptit).npepetit
– Công thức tính phân tử khối của n–peptit
Ví dụ: Đun nóng m gam hỗn hợp gồm a mol tetrapeptit mạch hở X và 2a mol tripeptit mạch hở Y với 600 ml dung dich NaOH 1M vừa đủ. Sau khi các phản ứng kết thúc, cô cạn dung dịch thu được 72,48 gam muối khan của các amino axit đều có một nhóm –COOH và một nhóm –NH2 trong phân tử. Giá trị của m là:
A. 51,72.
B. 54,30.
C. 66,00.
D. 44,48.
Hướng dẫn giải
Phương trình phản ứng
X + 4NaOH → 4Muối + H2O
a 4a a
Y + 3NaOH → 3Muối + H2O
2a 6a 2a
Ta có:
nNaOH = 4a + 2.3a = 10a = 0,6
→ a = 0,06 mol
n = a + 2a = 3a = 3.0,06 = 0,18 mol
Áp dụng định luật bảo toàn khối lượng:
mpeptit + mNaOH = mmuối + m
m + 0,6.40 = 72,48 + 0,18.18
→ m= 51,72 gam
→ Đáp án A
2. Kiến thức mở rộng
– Thủy phân hoàn toàn peptit trong môi trường trung tính (xúc tác enzim)
n–peptit X + (n–1)H2O n–amino axit
Ví dụ:
Gly–Gly–Gly + 2H2O → 3H2N–CH2–COOH
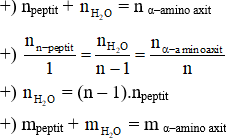
– Thủy phân hoàn toàn peptit trong môi trường axit
n–peptit+ (n – 1)H2O + aHCl → nmuối của ∝–amino axit
Trong đó:
a là số nguyên tử N trong peptit
Ví dụ:
Gly–Gly–Lys + 2H2O + 4HCl → 2ClH3N–CH2–COOH + ClH3N–(CH2)4–CH(NH3Cl)–COOH
– Tỉ lệ mol:
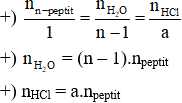
– Định luật bảo toàn khối lượng:
mpeptit + m + mHCl = mmuối
– Bảo toàn gốc ∝–amino axit:
n một muối ∝–amino axit = (số lượng nhóm ∝–amino axit đó có mặt trong n–peptit).npepetit
3. Bài tập minh họa
Câu 1: Thủy phân hoàn toàn 32,55 gam tripeptit mạch hở (Ala–Gly–Ala) bằng dung dịch NaOH (vừa đủ), sau phản ứng thu được dung dịch X. Cô cạn X thu được m gam muối khan. Giá trị m là:
A. 47,85 gam
B. 42,45 gam
C. 35,85 gam
D. 44,45 gam
Hướng dẫn giải
nAla–Gly–Ala = 0,15 mol. Vì Glyxin và Alanin đều chứa 1 nhóm –COOH trong phân tử nên ta có:
nNaOH = 3. nAla–Gly–Ala = 3.0,15 = 0,45 mol
n = 1. nAla–Gly–Ala = 0,15 mol
Áp dụng định luật bảo toàn khối lượng:
mpeptit + mNaOH = mmuối + m
32,55 + 0,45.40 = mmuối + 0,15.18
→ mmuối = 47,85 gam.
→ Đáp án A
Câu 2: Thủy phân hoàn toàn 24,6 gam một peptit X chỉ được tạo bởi từ một amino axit thu được 30 gam gly. X thuộc loại
A. đipeptit
B. tripeptit
C. tetrapeptit
D. pentapeptit
Hướng dẫn giải
Phương trình phản ứng
Peptit X + (n – 1)H2O → ngly
Áp dụng định luật bảo toàn khối lượng:
mpeptit + m = m α–amino axit
→ 24,6 + = 30
→ m = 5,4 gam
→ n = 0,3 mol
ngly = 0,4 mol
Ta có tỉ lệ
→ n = 4
→ X là tetrapeptit (gly–gly–gly–gly)
→ Đáp án C
Xem thêm các công thức Hoá học lớp 12 đầy đủ, chi tiết khác:
Công thức tính hiệu suất phản ứng este hóa
Công thức phản ứng xà phòng hóa este
Công thức phản ứng xà phòng hóa chất béo
Công thức bài toán đốt cháy este
Công thức bài toán đốt cháy chất béo
Công thức tính số mắt xích tinh bột
Công thức tính số mắt xích xenlulozơ
Công thức tính nhanh số đồng phân amin, amino axit
Công thức giải bài toán đốt cháy amin
Công thức bài toán đốt cháy amino axit
Công thức tính số mol OH- trong bài toán thủy phân peptit
Công thức tính số mắt xích (hệ số polime hóa) polime
Công thức tính lượng chất thu được ở điện cực
Công thức tính bài toán nhiệt nhôm
Công thức tính nhanh số mol OH- hoặc số mol Al(OH)3 khi cho muối nhôm phản ứng với dung dịch kiềm
Công thức tính nhanh số mol H+ khi cho từ từ axit vào muối AlO2 (muối aluminat)
Công thức khử oxit sắt bằng CO và H2