Bài viết Công thức tính nguyên tử khối trung bình của các nguyên tố hóa học hay nhất, chi tiết với bài tập minh họa có lời giải sẽ giúp học sinh nắm vững Công thức tính nguyên tử khối trung bình của các nguyên tố hóa học từ đó biết cách làm bài tập về tính nguyên tử khối trung bình của các nguyên tố hóa học.
Công thức tính nguyên tử khối trung bình của các nguyên tố hóa học hay nhất
Nhiều nguyên tố hóa học tồn tại nhiều đồng vị trong tự nhiên nên nguyên tử khối của các nguyên tố này là nguyên tử khối trung bình của các đồng vị đó.
Vậy tính được nguyên tử khối trung bình của các nguyên tố hóa học như thế nào? Bài viết này sẽ giúp các em trả lời các câu hỏi trên.
1. Công thức tính nguyên tử khối trung bình của nguyên tố hóa học
- Giả sử một nguyên tố có 2 đồng vị X và Y. Kí hiệu X, Y đồng thời là nguyên tử khối của 2 đồng vị, tỉ lệ phần trăm số nguyên tử tương ứng là a và b. Khi đó: nguyên tử khối trung bình (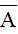 ) của nguyên tố này là:
) của nguyên tố này là:
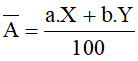
Chú ý: Một cách gần đúng, nguyên tử khối được lấy xấp xỉ bằng số khối.
2. Bạn nên biết
- Các đồng vị của cùng một nguyên tố là những nguyên tử có cùng số proton nhưng khác nhau về số nơtron, do đó có số khối A khác nhau.
- Phần lớn các nguyên tố hóa học là hỗn hợp của nhiều đồng vị. Các đồng vị của cùng một nguyên tố hóa học có số nơtron trong hạt nhân khác nhau, nên có một số tính chất vật lí khác nhau.
- Có các đồng vị bền và các đồng vị không bền. Hầu hết các đồng vị có số hiệu nguyên tử Z > 82 là không bền, chúng còn được gọi là các đồng vị phóng xạ.
3. Mở rộng
Xác định nguyên tử khối trung bình cho nguyên tố có n đồng vị:
Công thức: 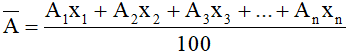
Trong đó: A1, A2, A3, .....An : là nguyên tử khối các đồng vị.
x1, x2, x3,.....xn : là thành phần % số nguyên tử của các đồng vị.
4. Bài tập minh họa
Câu 1: Cacbon có hai đồng vị là 12C chiếm 98,89% và 13C là 1,11%. Nguyên tử khối trung bình của nguyên tố cacbon là:
A. 12,0111
B. 12,0219
C. 12,0525
D. 12,5245
Hướng dẫn
Nguyên tử khối trung bình của nguyên tố cacbon là:
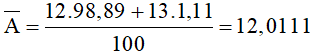
Đáp án A
Câu 2:Nitơ trong thiên nhiên là hỗn hợp gồm hai đồng vị là 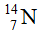 (99,63%) và
(99,63%) và 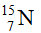 (0,37%). Nguyên tử khối trung bình của nitơ là:
(0,37%). Nguyên tử khối trung bình của nitơ là:
A. 14,7
B. 14,0
C. 14,4
D. 13,7
Hướng dẫn
Nguyên tử khối trung bình của nitơ là:
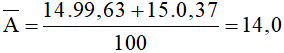
Đáp án B
Câu 3: Agon tách ra từ không khí là hỗn hợp ba đồng vị: 99,6% 40Ar; 0,063% 38Ar; 0,337% 36Ar. Nguyên tử khối trung bình của nguyên tố Agon là
A. 39,99
B. 37,99
C. 38,99
D. 35,99
Hướng dẫn:
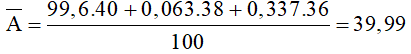
Đáp án A
Xem thêm các Công thức Hóa học lớp 10 quan trọng hay khác:
Công thức xác định thành phần nguyên tử
Công thức xác định thành phần các hạt trong ion
Công thức tính nguyên tử khối trung bình của các nguyên tố hóa học
Công thức tính phần trăm số nguyên tử mỗi đồng vị
Công thức tính bán kính nguyên tử
Công thức tính thể tích nguyên tử
Công thức oxit cao nhất, công thức hợp chất khí với hiđro các nguyên tố nhóm A
Công thức xác định hai nguyên tố thuộc hai chu kì liên tiếp trong cùng một nhóm A
Công thức xác định hai nguyên tố thuộc hai nhóm A liên tiếp trong cùng một chu kì
Công thức tính hiệu độ âm điện
Công thức tính nhanh khối lượng muối clorua tạo thành sau phản ứng
Công thức tính nhanh khối lượng muối sunfat
Công thức tính nhanh số mol OH- khi cho SO2 với dung dịch kiềm
Công thức tính nhanh số mol OH- khi cho H2S tác dụng với dung dịch kiềm
Công thức tính tốc độ phản ứng
Công thức tính hằng số cân bằng