Với giải Vận dụng trang 48 Hóa học lớp 11 Cánh diều chi tiết trong Bài 7: Sulfuric acid và muối sulfate giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 11. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 11 Bài 7: Sulfuric acid và muối sulfate
Vận dụng trang 48 Hoá học 11: Quá trình sản xuất sulfuric acid có thể ảnh hưởng đến môi trường và người tham gia sản xuất. Hãy tìm hiểu nguyên nhân và đề xuất một số biện pháp hạn chế những tác hại đó.
Lời giải:
- Một số nguyên nhân dẫn đến rủi ro, sự cố:
+ Nổ bình chứa, ống dẫn khí SO2, SO3.
+ Vỡ, thủng các bồn chứa acid.
+ Rò rỉ hệ thống đường ống dẫn hơi, các van, mối nối trên hệ thống đường ống.
+ Cháy nổ do chập điện…
- Một số biện pháp đề xuất để hạn chế tác hại:
+ Thực hiện nghiêm túc nội quy an toàn lao động; trang bị đầy đủ các phương tiện bảo vệ cá nhân (quần áo bảo hộ lao động, kính mắt, gang tay, ủng …) khi làm việc.
+ Thường xuyên kiểm tra máy móc, thiết bị vận hành…
+ Sử dụng các thiết bị tách mù tiên tiến, có hiệu xuất xử lí cao, ví dụ như thiết bị tách mù acid bằng lọc bụi tĩnh điện ướt (ở nhà máy Super phosphate Lâm Thao) …
Lý thuyết Sulfuric acid
1. Cấu tạo phân tử và tính chất vật lí
- Cấu tạo phân tử:
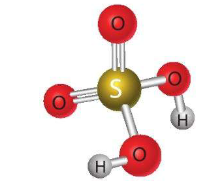
- Tính chất vật lí:
+ Là chất lỏng sánh như dầu, không màu, không bay hơi.
+ Dung dịch sulfuric acid đặc có khả năng hút ẩm.
2. Tính chất hóa học
a, Tính chất hóa học của dung dịch sulfuric acid loãng
+ Đổi màu quý tím thành đỏ
+ Tác dụng với kim loại hoạt động.
+ Tác dụng với basic oxide và base.
+ Tác dụng với nhiều muối.
b, Tính chất hóa học của dung dịch sulfuric acid đặc
- Tính oxi hóa mạnh
+ Oxi hóa hầu hết các kim loại (trừ vàng, platinium), nhiều phi kim như carbon, sulfur, phosphorus… và nhiều hợp chất
VD: H2SO4 + Cu → CuSO4 + SO2 + 2H2O
2H2SO4 + S → 3SO2 + 2H2O
- Tính háo nước
+ Dung dịch sulfuric acid đặc hấp thụ mạnh nước.
3. Bảo quản và xử lí bỏng sulfuric acid
- Bảo quản: Chai, lọ đựng sulfuric acid phải để ở nơi ít có nguy cơ bị va chạm, xa nguồn nhiệt và các hóa chất khác.
- Xử lí bỏng sulfuric acid: Sơ cứu người bị bỏng bằng cách rửa vết bỏng dưới vòi nước sạch ít nhất 20 phút trước khi đưa đến cơ sở y tế.
+ Tuyệt đối không chườm đá lạnh, khong xoa vết bỏng bằng các loại kem, gel, dầu …
4. Ứng dụng và sản xuất sulfuric acid
a, Ứng dụng
- Sản xuất phân bón.
- Chất tẩy rửa, phẩm màu, thuốc trừ sâu…
b, Sản xuất sulfuric acid bằng phương pháp tiếp xúc
S(s) + O2(g) → SO2(g)
4FeS2(s) + 11O2(g) → 2Fe2O3(s) + 8SO2(g)
2SO2 + O2(g) → 2SO3
H2SO4(aq) + nSO3(g) → H2SO4.nSO3(l)
H2SO4.nSO3 (l) + nH2O → (n+1) H2SO4
Xem thêm lời giải bài tập Hóa học lớp 11 Cánh diều hay, chi tiết khác:
Câu hỏi 1 trang 44 Hoá học 11: Hãy viết công thức Lewis của phân tử H2SO4.....
Thí nghiệm 2 trang 45 Hoá học 11: Tính háo nước và tính oxi hoá của dung dịch sulfuric acid đặc....
Xem thêm các bài giải SGK Hóa học lớp 11 Cánh diều hay, chi tiết khác: