Với tóm tắt lý thuyết Hóa học lớp 11 Bài 21: Phenol sách Kết nối tri thức hay, chi tiết cùng với bài tập trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 11.
Lý thuyết Hóa học lớp 11 Bài 21: Phenol
A. Lý thuyết Phenol
1. Khái niệm
Phenol là những hợp chất hữu cơ trong phân tử có nhóm –OH liên kết trực tiếp với nguyên tử carbon của vòng benzene.
Hợp chất phenol đơn giản nhất có công thức là C6H5OH cũng có tên gọi riêng là phenol. Tên thông thường của một số phenol:
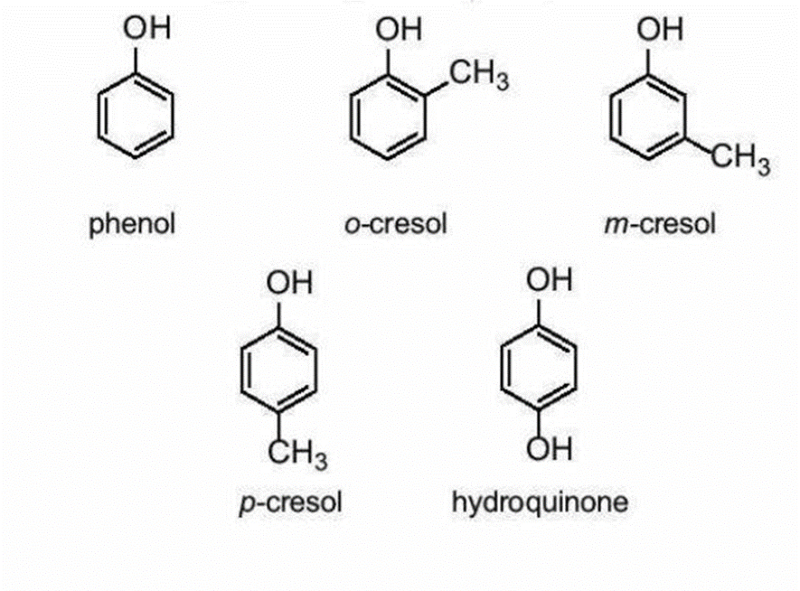
2. Đặc điểm cấu tạo của phenol
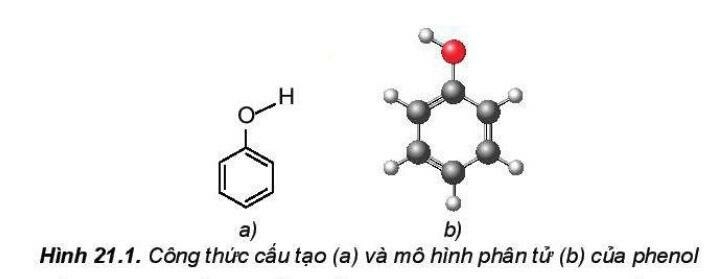
Trong phân tử phenol, do ảnh hưởng của vòng benzene nên liên kết C-H của phenol phân cực mạnh hơn so với alcohol, vì vậy phenol thể hiện tính acid yếu.
3. Tính chất vật lí
- Là chất có tính độc.
- Ở điều kiện thường, phenol là chất rắn không màu, nóng chảy ở 43°C, sôi ở 181,8oC.
- Ít tan trong nước ở điều kiện thường (độ tan trong nước ở 25°C: 8,42 g/100g nước), tan nhiều khi đun nóng (tan vô hạn ở 66°C); tan tốt trong các dung môi hữu cơ như ethanol, ether và acetone.
4. Tính chất hoá học
a. Phản ứng thế nguyên tử H của nhóm –OH (tính acid của phenol)
Trong dung dịch nước, phenol phân li theo cân bằng sau:
C6H5OH + H2O ⇌ C6H5O- + H3O+
Phenol là một acid yếu, dung dịch phenol không làm đổi màu quỳ tím và có thể phản ứng được với các kim loại kiềm, dung dịch base,…
b. Phản ứng thế ở vòng thơm
* Phản ứng bromine hóa:
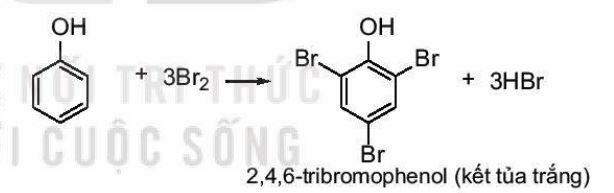
Phenol phản ứng với nước bromine tạo sản phẩm thể 2,4,6-tribromophenol ở dạng kết tủa màu trắng. Do ảnh hưởng của nhóm –OH, phản ứng thể nguyên tử hydrogen ở vòng benzene của Br 2,4,6-tribromophenol (kết tủa trắng) phend xảy ra dễ dùng hơn so với benzene.
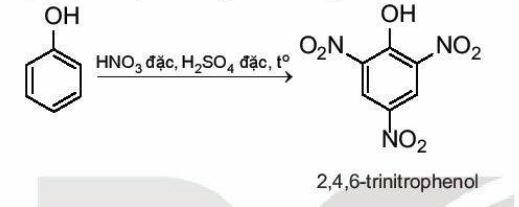
* Phản ứng nitro hóa:
Phenol phản ứng với dung dịch nitric acid đặc trong dung dịch sulfuric acid đặc tạo thành sản phẩm 2,4,6-trinitrophend (picric acid).
5. Ứng dụng
- Sản xuất mĩ phẩm.
- Sản xuất tơ sợi.
- Sản xuất chất dẻo.
- Sản xuất phẩm nhuộm.
- Sản xuất dược phẩm.
- Sản xuất thuốc sát trùng.
- Sản xuất thuốc diệt cỏ.
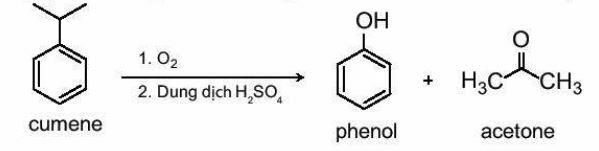
6. Điều chế
Phenol được tổng hợp từ cumene (isopropylbenzene) bằng phản ứng oxi hoá bởi oxygen rồi thuỷ phân trong môi trường acid thu được hai sản phẩm là phenol và acetone:
Sơ đồ tư duy Phenol
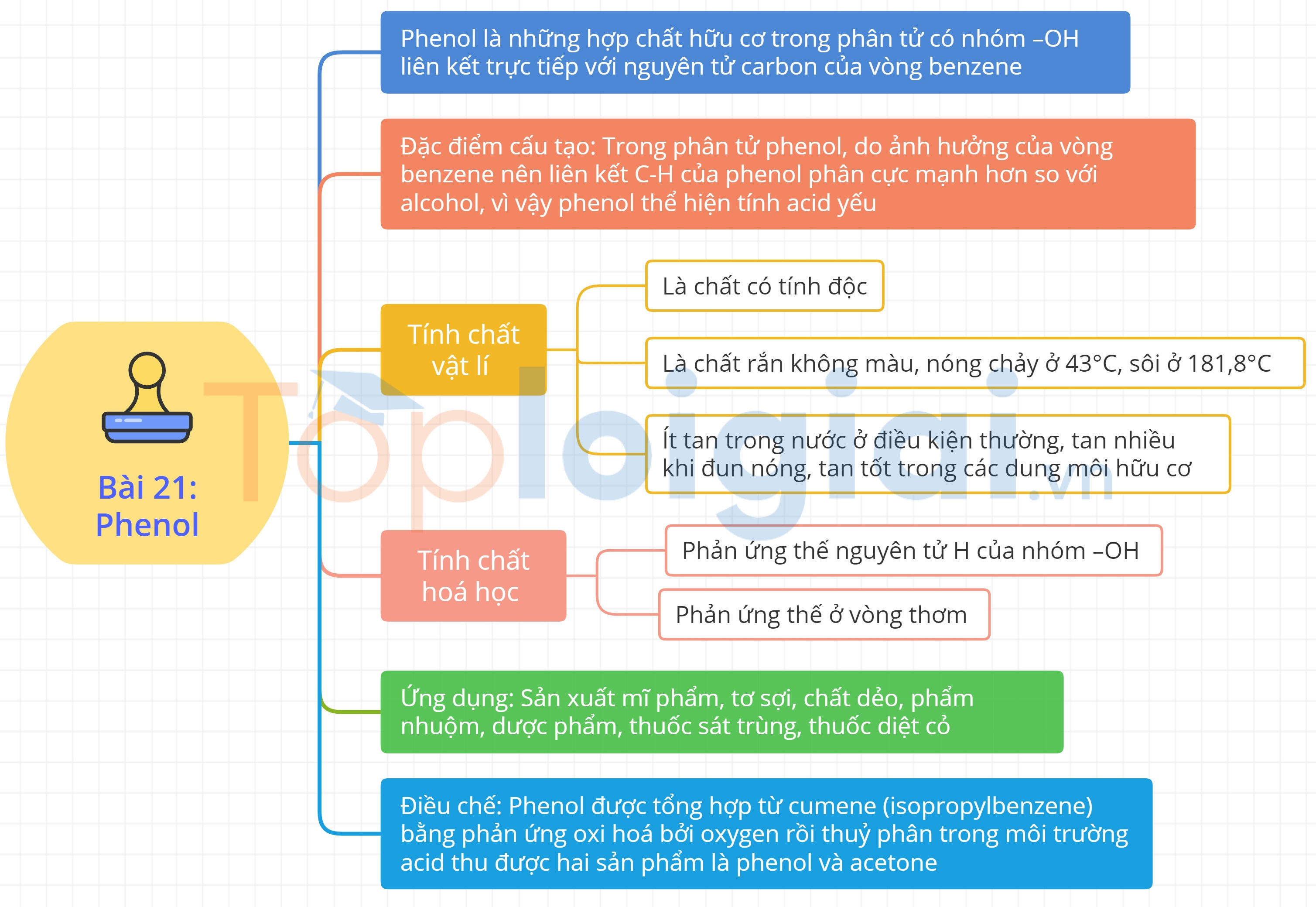
B. Trắc nghiệm Phenol
Câu 1: Phenol không thể phản ứng được với
A. phi kim.
B. kim loại kiềm.
C. dung dịch base.
D. muối sodium carbonate.
Đáp án đúng là: A
Phenol có thể phản ứng được với kim loại kiềm, dung dịch base, muối sodium carbonate,…
Câu 2: Dãy gồm với các chất đều tác dụng với phenol là
A. dung dịch NaCl, dung dịch NaOH, kim loại Na.
B. ethyl alcohol, dung dịch bromine, kim loại Na.
C. dung dịch bromine, kim loại Na, dung dịch NaOH.
D. dung dịch NaOH, khí methane, ethyl alcohol.
Đáp án đúng là: C
A sai vì có dung dịch NaCl không tác dụng với phenol.
B sai vì có ethyl alcohol không tác dụng với phenol.
D sai vì có khí methane không tác dụng với phenol.
Câu 3: Nhỏ từ từ từng giọt bromine vào ống nghiệm chứa dung dịch phenol hiện tượng quan sát được là
A. nước bromine bị mất màu.
B. xuất hiện kết tủa trắng.
C. xuất hiện kết tủa trắng sau tan dần.
D. xuất hiện kết tủa trắng và nước bromine bị mất màu.
Đáp án đúng là: D
Nhỏ từ từ từng giọt bromine vào ống nghiệm chứa dung dịch phenol hiện tượng quan sát được là xuất hiện kết tủa trắng và nước bromine bị mất màu.
C6H5OH + 3Br2 → C6H2(OH)Br3↓ + 3HBr
Câu 4: Các phát biểu đúng về phenol là
(1) Phenol có tính acid nhưng yếu hơn carbonic acid.
(2) Phenol làm đổi màu quỳ tím thành đỏ.
(3) Hydrogen trong nhóm –OH của phenol linh động hơn hydrogen trong nhóm –OH của ethanol, như vậy phenol có tính acid mạnh hơn ethanol.
(4) Phenol tan trong nước (lạnh) vô hạn vì nó tạo được liên kết hydrogen với nước.
(5) Acid picric có tính acid mạnh hơn phenol rất nhiều.
(6) Phenol không tan trong nước nhưng tan tốt trong dung dịch NaOH.
A. (1), (2), (3), (6).
B. (1), (2), (4), (6).
C. (1), (3), (5), (6).
D. (1), (2), (5), (6).
Đáp án đúng là: C
(2) sai vì phenol không làm đổi màu quỳ tím thành đỏ.
(4) phenol ít tan trong nước ở điều kiện thường.
Câu 5: Cho các phát biểu sau về phenol
(a) Phenol vừa tác dụng được với dung dịch NaOH vừa tác dụng được với Na.
(b) Phenol tan được trong dung dịch KOH.
(c) Nhiệt độ nóng chảy của phenol lớn hơn nhiệt độ nóng chảy của ethyl alcohol.
(d) Phenol phản ứng được với dung dịch KHCO3 tạo CO2.
(e) Phenol là một alcohol thơm.
Trong các trường hợp trên, số phát biểu đúng là
A. 5.
B. 2.
C. 3.
D. 4.
Đáp án đúng là: C
Trong các trường hợp trên, phát biểu đúng là a, b, c.
Câu 6: Ở điều kiện thường, phenol là
A. chất lỏng sánh, màu nâu.
B. chất khí màu vàng nhạt.
C. chất rắn không màu.
D. huyền phù.
Đáp án đúng là: C
Ở điều kiện thường, phenol là chất rắn không màu.
Câu 7: Phenol là những hợp chất hữu cơ trong phân tử có nhóm -OH
A. liên kết trực tiếp với nguyên tử carbon của vòng benzene.
B. liên kết trực tiếp với nguyên tử carbon bậc III.
C. liên kết trực tiếp với nguyên tử carbon bậc II.
D. liên kết trực tiếp với nguyên tử carbon bậc I.
Đáp án đúng là: A
Phenol là những hợp chất hữu cơ trong phân tử có nhóm –OH liên kết trực tiếp với nguyên tử carbon của vòng benzene.
Câu 8: Liên kết O-H của phenol phân cực mạnh hơn so với alcohol do?
A. Ảnh hưởng của vòng benzene.
B. Phân tử khối lớn hơn.
C. Các nguyên tử carbon có độ âm điện lớn hơn nguyên tử oxygen.
D. Đáp án khác.
Đáp án đúng là: A
Trong phân tử phenol, do ảnh hưởng của vòng benzene nên liên kết O-H của phenol phân cực mạnh hơn so với alcohol.
Câu 9: Chọn phát biểu không đúng?
A. Phenol có tính acid nhưng yếu hơn carbonic acid.
B. Phenol cho phản ứng cộng dễ dàng với bromine tạo kết tủa trắng 2,4,6-tribromophenol.
C. Do nhân benzene hút điện tử khiến –OH của phenol có tính acid.
D. Dung dịch phenol không làm đổi màu quỳ tím vì tính acid của phenol rất yếu.
Đáp án đúng là: B
Phenol cho phản ứng thế dễ dàng với bromine tạo kết tủa trắng 2,4,6-tribromophenol.
Câu 10: Phát biểu không đúng khi nói về tính chất vật lí của phenol là
A. Phenol ít tan trong nước ở điều kiện thường.
B. Tan tốt trong dung môi hữu cơ.
C. Độc, có thể gây bỏng khi tiếp xúc với da.
D. Ở nhiệt độ cao, phenol không tan trong nước.
Đáp án đúng là: D
Phenol tan nhiều khi đun nóng (tan vô hạn ở 66oC).
Câu 11: Ứng dụng của phenol là
A. Sản xuất mỹ phẩm.
B. Làm chất bảo quản thực phẩm.
C. Kích thích hoa quả chín.
D. Sản xuất sulfuric acid.
Đáp án đúng là: A
Ứng dụng của phenol là sản xuất mỹ phẩm, tơ sợi, chất dẻo, phẩm nhuộn, dược phẩm, thuốc sát trùng, thuốc diệt cỏ,…
Câu 12: Trong công nghiệp, phenol được tổng hợp từ?
A. Acetone.
B. Ethyl alcohol.
C. Benzene.
D. Cumene.
Đáp án đúng là: D
Trong công nghiệp, phenol được tổng hợp từ cumene.
Câu 13: Cho dung dịch bromine dư vào a gam dung dịch phenol (C6H5OH), thu được 33,1 gam kết tủa. Giá trị của a là
A. 4,7 gam.
B. 47 gam.
C. 9,4 gam.
D. 94 gam.
Đáp án đúng là: C
C6H5OH + 3Br2 → C6H2(OH)Br3↓ + 3HBr
Câu 14: Cho hỗn hợp gồm 0,2 mol phenol và 0,3 mol ethylene glycol tác dụng với lượng dư potassium thu được V lít H2 ở đkc. Giá trị của V là?
A. 9,9160.
B. 12,3950.
C. 6,1975.
D. 8,6765.
Đáp án đúng là: A
Câu 15: Để phân biệt dung dịch phenol và benzyl alcohol ta có thể dùng thuốc thử nào trong các thuốc thử sau: Na (1), NaOH, quỳ tím (2), dung dịch nước Br2 (3).
A. Chỉ có (1).
B. (2) và (3).
C. Chỉ có (2).
D. Chỉ có (3.)
Đáp án đúng là: B
Vì dung dịch phenol tác dụng với NaOH và dung dịch nước bromine còn benzyl alcohol thì không.
Xem thêm các bài tóm tắt Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác: