Bài viết Công thức bài toán tách nước của ancol hay nhất, chi tiết với bài tập minh họa có lời giải sẽ giúp học sinh nắm vững Công thức bài toán tách nước của ancol từ đó biết cách làm bài tập về bài toán tách nước của ancol.
Công thức bài toán tách nước của ancol hay nhất
Ancol là những hợp chất hữu cơ trong phân tử chưa nhóm –OH gắn trực tiếp với C no. Hợp chất ancol có phản ứng quan trọng là phản ứng tách nước. Vậy sản phẩm phản ứng là gì? Phương pháp nào giải dạng toán tách nước của ancol nhanh và chính xác nhất? Bài viết dưới đây, sẽ cung cấp cho các em những lý thuyết và phương pháp giải dạng bài tách nước của ancol.
1. Công thức bài toán tách nước của ancol
Phản ứng tách nước của ancol có 2 kiểu như sau:
a) Tách nước từ 1 phân tử ancol tạo hiđrocacbon không no
- Điều kiện: xúc tác H2SO4 đặc, đun nóng (170oC).
- Phương trình:
- Khi giải bài tập có liên quan đến phản ứng tách nước của ancol cần nhớ:
mAncol = manken + + mAncol dư
nancol phản ứng = nanken = nnước
b) Tách nước từ 2 phân tử ancol tạo ete
- Phản ứng tách nước tạo ete của ancol thường chỉ áp dụng với ancol đơn chức.
- Phản ứng xảy ra khi đun nóng ancol hoặc hỗn hợp ancol với H2SO4 đặc, đun nóng đến 140.
Phương trình tổng quát:
- Phương pháp giải:
2. Bạn nên biết
a) Tách nước tạo anken
- Cách thức phản ứng: Nhóm -OH của ancol tách ra cùng với nguyên tử H của C liền kề tạo ra liên kết pi giữa 2 nguyên tử C đó.
- Hướng tạo sản phẩm chính tuân theo quy tắc Zai -xép: Nhóm -OH ưu tiên tách cùng nguyên tử H của C bậc cao hơn.
- Điều kiện của ancol tham gia phản ứng: Ancol có Hα (C liền cạnh C mang nhóm OH còn H)
- Nhiều ancol tách nước tạo ra một anken thì xảy ra các khả năng sau:
+ Có ancol không tách nước.
+ Các ancol là đồng phân của nhau.
b) Ancol tách nước tạo ete
- Nếu tách nước thu được các ete có số mol bằng nhau thì các ancol tham gia phản ứng cũng có số mol bằng nhau.
3. Mở rộng
- Có thể dựa vào tỉ khối của sản phẩm so với ancol (d) để xác định hướng tách nước của ancol:
+ Nếu d < 1 → ancol tách nước tạo anken.
+ Nếu d > 1 → ancol tách nước tạo ete.
4. Bài tập minh họa
Câu 1: Cho các ancol sau:
Số ancol khi tham gia phản ứng tách nước tạo 1 anken duy nhất là
A. 3.
B. 4.
C. 5.
D. 6
Hướng dẫn giải
CH3CH2OH 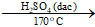
CH3-CH(OH)-CH3 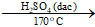
CH3-CH2-CH2OH 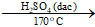
(CH3)2CH-CH2OH 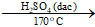
(CH3)C-OH 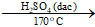
(CH3)2CH-CH(OH)-CH3
Đáp án C
Câu 2: Đun 132,8 gam hỗn hợp ba ancol no, đơn chức với H2SO4 đặc ở 140°C thu được 111,2 gam hỗn hợp các ete có số mol bằng nhau. Số mol mỗi ete là
A. 0,10 mol.
B. 0,15 mol.
C. 0,20 mol.
D. 0,25 mol.
Hướng dẫn giải
Ancol ete + nước
Áp dụng định luật bảo toàn khối lượng: mancol = mete + mnước
Đáp án C
Câu 3: Đun nóng 8,68 gam hỗn hợp X gốm các ancol no, đơn chức, mạch hở với H2SO4 đặc, thu được hỗn hợp Y gồm: ete (0,04 mol), anken và ancol dư. Đốt cháy hoàn toàn lượng anken và ete trong Y, thu được 0,34 mol CO2. Nếu đốt cháy hết lượng ancol trong Y thì thu được 0,1 mol CO2 và 0,13 mol H2O. Phần trăm số mol ancol tham gia phản ứng tạo ete là
A. 21,43%.
B. 26,67%.
C. 31,25%.
D. 35,29%.
Hướng dẫn giải
Đặt công thức chung cho các ancol trong X là CnH2n+2O (x mol)
Đáp án A
Xem thêm các công thức Hoá học lớp 11 đầy đủ, chi tiết khác:
Công thức xác định hằng số điện li
Công thức liên hệ giữa hằng số điện li và độ điện li
Công thức tính hằng số phân li bazơ
Công thức tính hằng số phân li axit
Công thức tính pH trong dung dịch axit yếu/bazơ yếu
Công thức tính pH trong dung dịch axit mạnh/bazơ mạnh
Công thức tính nhanh số mol HNO3 phản ứng
Công thức tính nhanh khối lượng muối nitrat
Công thức tính nhanh hiệu suất tổng hợp NH3
Công thức tính số mol OH- khi cho P2O5 tác dụng với dung dịch kiềm
Công thức tính độ dinh dưỡng của phân bón
Công thức tính số mol OH- ( hoặc CO2) khi cho CO2 tác dụng với dung dịch kiềm
Công thức tính nhanh bài toán khử oxit kim loại bằng CO
Công thức tính độ bất bão hòa hợp chất hữu cơ
Công thức tính % khối lượng các nguyên tố trong hợp chất hữu cơ
Xác định công thức phân tử hợp chất hữu cơ
Công thức xác định số nguyên tử trong hợp chất hữu cơ
Công thức tính nhanh số đồng phân của ankan
Công thức tính nhanh số mol ankan
Công thức tính khí đốt cháy ankan
Công thức tính nhanh đồng phân của anken
Công thức tính nhanh đồng phân của ankin
Công thức tính toán đốt cháy anken
Công thức tính toán đốt cháy ankin
Công thức bảo toàn số mol liên kết pi
Công thức tính nhanh số đồng phân ankylbenzen
Công thức đốt cháy benzen và ankylbenzen
Công thức tính nhanh số đồng phân ancol no, đơn chức, mạch hở
Công thức tính toán đốt cháy ancol
Công thức tính nhanh số đồng phân ete no, đơn chức, mạch hở
Công thức tính số ete tối đa thu được từ hỗn hợp n ancol đơn chức
Công thức bài toán tách nước của ancol
Công thức xác định số nhóm chức ancol
Công thức tính đồng phân phenol
Công thức tính nhanh số đồng phân Anđehit no, đơn chức, mạch hở
Công thức tính nhanh số đồng phân Axit cacboxylic no, đơn chức, mạch hở
Công thức tính nhanh số đồng phân Xeton no, đơn chức, mạch hở
Công thức phản ứng tráng gương (tráng bạc) của anđehit
Công thức bài toán đốt cháy anđehit
Công thức bài toán đốt cháy axit cacboxylic