Với giải Thí nghiệm 4 trang 98 Hóa học lớp 12 Cánh diều chi tiết trong Bài 14: Tính chất hoá học của kim loại giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 12. Mời các bạn đón xem:
Giải bài tập Hóa học 12 Bài 14: Tính chất hoá học của kim loại
Thí nghiệm 4 trang 98 Hóa học 12: Phản ứng của kim loại với dung dịch sulfuric acid loãng, dung dịch sulfuric acid đặc, nóng
Chuẩn bị:
- Hoá chất: Lá đồng, dung dịch sulfuric acid 1 M, dung dịch sulfuric acid khoảng 70%, giấy quỳ.
- Dụng cụ: Ống nghiệm, kẹp ống nghiệm, bông tẩm nước, đèn cồn, bật lửa.
Tiến hành:
- Cho vào mỗi ống nghiệm chứa dung dịch sulfuric acid loãng và ống nghiệm chứa dung dịch sulfuric acid đặc một lá đồng.
- Đậy mỗi ống nghiệm bằng bông tẩm nước.
- Đun hai ống nghiệm trên ngọn lửa đèn cồn. Sau một thời gian, dùng mẫu giấy quỳ kiểm tra pH của bông tẩm nước đã dùng để nút hai ống nghiệm trên.
Yêu cầu: Quan sát, mô tả hiện tượng và giải thích. Viết phương trình hoá học của phản ứng xảy ra (nếu có).
Chú ý: Cẩn thận khi sử dụng dung dịch sulfuric acid đặc.
Lời giải:
- Hiện tượng: Ở ống nghiệm chứa dung dịch sulfuric acid loãng không có hiện tượng xảy ra. Ở ống nghiệm chứa dung dịch sulfuric acid đặc thấy sủi bọt khí không màu, lá đồng tan dần, bông tẩm nước nút ống nghiệp làm giấy quỳ chuyển đỏ.
- Giải thích:
+ Lá đồng không phản ứng với dung dịch sulfuric acid loãng.
+ Lá đồng phản ứng với dung dịch sulfuric acid đặc nóng giải phóng khí sulfur dioxide. Khí này tan trong nước tạo dung dịch acid làm giấy quỳ chuyển đỏ.
+ Phương trình hóa học:
Cu(s) + 2H2SO4(aq) CuSO4(aq) + SO2(g) + 2H2O(l)
SO2(g)+ H2O(l) ⇌ H2SO3(aq)
Lý thuyết Tác dụng với dung dịch acid
1. Tác dụng với dung dịch hydrochloric acid, dung dịch sulfuric acid loãng
Do nên kim loại M có giá trị thế điện cực chuẩn có theẻ khử được ion H+ trong dung dịch hydrchloric acid hoặc dung dihcj sulfuric acid loãng, tạo thành khí H2
Ví dụ: Zn(s) + 2H+(aq) Zn2+ (aq) + H2(g)
Do giá trị thế điện cực chuẩn dương nên các kim loại như Cu, Ag,… không tác dụng với dung dịch hydrochloric acid hoặc dung dịch sulfuric acid loãng.
2. Tác dụng với dung dịch sulfuric acid đặc
Hầu hết các kim loại (trừ Au và Pt) phản ứng được với dung dịch sulfuric acid đặc. Phản ứng này thường tạo thành muối sulfate, nước và sulfur dioxide. Phản ứng diễn ra mạnh hơn khi hỗn hợp phản ứng được đun nóng
Ví dụ: 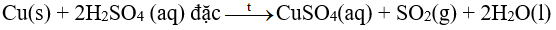
Xem thêm lời giải bài tập Hóa học lớp 12 Cánh diều hay, chi tiết khác:
Thí nghiệm 1 trang 96 Hóa học 12: Kim loại tác dụng với oxygen trong không khí...
Luyện tập 2 trang 97 Hóa học 12: Cho = −2,925 V, = 0,854 V....
Thí nghiệm 2 trang 97 Hóa học 12: Phản ứng của kim loại với dung dịch muối...
Thí nghiệm 3 trang 97 Hóa học 12: Phản ứng của kim loại với dung dịch hydrochloric acid...
Xem thêm các bài giải bài tập Hóa Học lớp 12 Cánh diều hay, chi tiết khác:
Bài 13. Cấu tạo và tính chất vật lí của kim loại
Bài 14. Tính chất hoá học của kim loại
Bài 15. Tách kim loại và tái chế kim loại