Với giải sách bài tập Hóa học 11 Bài 15: Alkane sách Kết nối tri thức hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 15: Alkane
A. C2H6.
B. C3H6.
C. C4H10.
D. C5H12.
Lời giải:
Đáp án đúng là: B
C3H6 không phải là alkane.
Bài 15.2 trang 54 Sách bài tập Hóa học 11: Pentane là tên theo danh pháp thay thế của
A. CH3[CH2]2CH3.
B. CH3[CH2]3CH3,
C. CH3[CH2]4CH3.
D. CH3[CH2]5CH3.
Lời giải:
Đáp án đúng là: B
Pentane là hợp chất thuộc alkane, mạch carbon gồm có 5 carbon liên kết với nhau bằng các liên kết đơn.
Bài 15.3 trang 54 Sách bài tập Hóa học 11: (CH3)2CH-CH3 có tên theo danh pháp thay thế là
A. 2-methylpropane.
B. isobutan.
B. butane.
D. 2-methylbutane.
Lời giải:
Đáp án đúng là: A
(CH3)2CH-CH3 có tên theo danh pháp thay thế là 2-methylpropane.
Bài 15.4 trang 54 Sách bài tập Hóa học 11: Phát biểu nào sau đây không đúng?
A. Trong phân tử alkane chỉ chứa các liên kết bền vững.
B. Các phân tử alkane hầu như không phân cực.
C. Ở điều kiện thường các alkane tương đối trơ về mặt hoá học.
D. Trong phân tử methane, bốn liên kết C-H hướng về bốn đỉnh của một hình vuông.
Lời giải:
Đáp án đúng là: D
Trong phân tử methane, bốn liên kết C-H giống nhau tạo với nhau một góc 109,5o và hướng về bốn đỉnh của một tứ diện đều.
Bài 15.5 trang 54 Sách bài tập Hóa học 11: Phát biểu nào sau đây không đúng (ở điều kiện thường)?
A. Các alkane từ C1 đến C4 và neopentane ở trạng thái khí.
B. Các alkane từ C5 đến C17 (trừ neopentane) ở trạng thái lỏng.
C. Các alkane không tan hoặc tan rất ít trong nước và nhẹ hơn nước.
D. Các alkane không tan hoặc tan rất ít trong các dung môi hữu cơ.
Lời giải:
Đáp án đúng là: D
Ở điều kiện thường, các alkane dễ tan và tan nhiều trong các dung môi hữu cơ.
A. Khá trơ về mặt hoá học, phản ứng đặc trưng là thế và tách.
B. Hoạt động hoá học mạnh, phản ứng đặc trưng là thế và tách.
C. Khá trơ về mặt hoá học, phản ứng đặc trưng là cộng và trùng hợp.
D. Hoạt động hoá học mạnh, phản ứng đặc trưng là cộng và trùng hợp.
Lời giải:
Đáp án đúng là: A
Do phân tử chỉ chứa các liên kết σ bền, nên các alkane khá trơ về mặt hóa học, phản ứng đặc trưng là phản ứng thế và tách.
Số chất là sản phẩm của phản ứng xảy ra khi trộn methane với chlorine và chiếu ánh sáng tử ngoại là
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án đúng là: D
Các chất là sản phẩm của phản ứng xảy ra khi trộn methane với chlorine và chiếu ánh sáng tử ngoại là chloromethane, dichloromethane, trichloromethane và tetrachloromethane.
A. (X).
B. (Y).
C. cả hai chất.
D. chất khác X, Y.
Lời giải:
Đáp án đúng là: C
Phương trình phản ứng xảy ra như sau:
A. ngắn hơn.
B. dài hơn.
C. không đổi.
D. thay đổi
Lời giải:
Đáp án đúng là: A
Cracking alkane là quá trình phân cắt liên kết C-C (bẻ gãy mạch carbon) của các alkane mạch dài để tạo thành hỗn hợp các hydrocarbon có mạch carbon ngắn hơn.
A. Chuyển alkane mạch không phân nhánh thành các alkane mạch phân nhánh.
B. Chuyển alkane mạch không phân nhánh thành các hydrocarbon mạch vòng.
C. Số nguyên tử carbon của chất tham gia và của sản phẩm bằng nhau.
D. Nhiệt độ sôi của sản phẩm lớn hơn nhiều so với alkane tham gia phản ứng.
Lời giải:
Đáp án đúng là: D
Do phản ứng refoming không làm thay đổi số nguyên tử carbon của phân tử nên nhiệt độ sôi của sản phẩm không chênh lệch nhiều so với chất tham gia.
Bài 15.11 trang 55 Sách bài tập Hóa học 11: Phát biểu nào sau đây về ứng dụng của alkane không đúng?
A. Propane C3H8 và butane C4H10 được sử dụng làm khí đốt.
B. Các alkane C6, C7, C8 là nguyên liệu để sản xuất một số hydrocarbon thơm.
C. Các alkane lỏng được sử đụng làm nhiên liệu như xăng hay dầu diesel.
D. Các alkane từ C11 đến C20 được dùng làm nến và sáp.
Lời giải:
Đáp án đúng là: D
Các alkane từ C11 đến C20 được dùng làm kem dưỡng da, sáp nẻ, thuốc mỡ.
A. 2.
B. 3.
C. 4.
D. 5.
Lời giải:
Đáp án đúng là: D
5 đồng phân gồm:
CH3[CH2]4CH3; CH3CH(CH3)CH2CH2CH3; CH3CH2CH(CH3) CH2CH3; CH3CH(CH3)CH(CH3)CH3; (CH3)3CCH2CH3.
Bài 15.13 trang 56 Sách bài tậ Hóa học 11: Alkane (CH3)3C-CH2-CH(CH3)2 có tên gọi là
A. 2,2,4-trimethylpentane.
B. 2,4,4-trimethylpentane.
C. pentamethylpropane.
D. trimetylpentane.
Lời giải:
Đáp án đúng là: A
Alkane (CH3)3C-CH2-CH(CH3)2 có tên gọi là 2,2,4-trimethylpentane.
Bài 15.14 trang 56 Sách bài tập Hóa học 11: Tên gọi của alkane nào sau đây đúng?
A. 2-ethylbutane.
B. 2,2-dimethylbutane.
C. 3-methylbutane.
D. 2,3,3-trimethylbutane
Lời giải:
Đáp án đúng là: B
Công thức cấu tạo của 2,2-dimethylbutane là
Số alkane tồn tại ở thể khí ở điều kiện thường là
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án đúng là: B
Các alkane tồn tại ở thể khí ở điều kiện thường là propane (-187,7 và - 42,1), butane (– 183,3 và – 0,5).
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án đúng là: A
Sản phẩn duy nhất thu được là 1-chloro-2,2-dimethylpropane.
Trong số các chất này, có bao nhiêu chất có thể là sản phẩm reforming hexane?
A. 5.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án đúng là: D
Reforming alkane là quá trình chuyển các alkane mạch không phân nhánh thành các alkane mạch phân nhánh và các hydrocarbon mạch vòng nhưng không làm thay đổi số nguyên tử carbon trong phân tử.
A. HCOOH.
B. CH3COOH.
C. C2H5COOH.
D. CO2.
Lời giải:
Đáp án đúng là: B
Phương trình phản ứng:
2CH3CH2CH2CH3 + 5O2 4CH3COOH + 2H2O
Pentane; 2-methylbutane (isopentane) và 2,2-dimethylpropane (neopentane).
(b) Gọi tên các alkane sau:
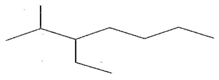 |
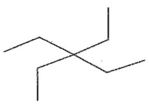 |
|
(i) |
(ii) |
Lời giải:
a) Công thức cấu tạo:
b) Tên gọi các alkane:
Số dẫn xuất một lần thế được tạo thành khi chlorine hoá các hydrocarbon trên là bao nhiêu? Viết công thức cấu tạo và gọi tên các sản phẩm.
Lời giải:
a) Hai sản phẩm:
b) Hai sản phẩm:
c) Một sản phẩm:
Lời giải:
a) Bậc của carbon càng cao, phản ứng thế xảy ra càng dễ dàng. Phản ứng thế ở carbon bậc ba dễ hơn ở carbon bậc hai và phản ứng thế ở carbon bậc hai dễ hơn ở carbon bậc một.
b) Chlorine tham gia phản ứng thế dễ dàng hơn so với bromine. Vì vậy, tính chọn lọc vị trí thế của chlorine yếu hơn so với bromine (nói cách khác, do khả năng phản ứng của bromine yếu, nên bromine chủ yếu lựa chọn phản ứng ở vị trí carbon bậc cao hơn, nơi phản ứng xảy ra dễ dàng hơn).
Lời giải:
Nhiệt cháy của methane là biến thiên enthalpy của phản ứng:
CH4(g) + 2O2 → CO2(g) + 2H2O(l)
Vậy nhiệt hình thành chuẩn của methane là:
Nhiệt cháy của propane là biến thiên enthalpy của phản ứng:
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O(l)
Vậy nhiệt hình thành chuẩn của propane là:
Xem thêm các bài giải SBT Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 17: Arene (Hydrocarbon thơm)
Lý thuyết Alkane
1. Khái niệm, danh pháp
a. Khái niệm và công thức chung của alkane
Alkane là các hydrocarbon no mạch hở chỉ chứa liên kết đơn C-H và C-C trong phân tử.
Công thức chung của alkane là: CnH2n+2 (n là số nguyên, n ≥ 1)
b. Danh pháp
* Alkane không phân nhánh
Tên theo danh pháp thay thế của alkane mạch không phân nhánh:
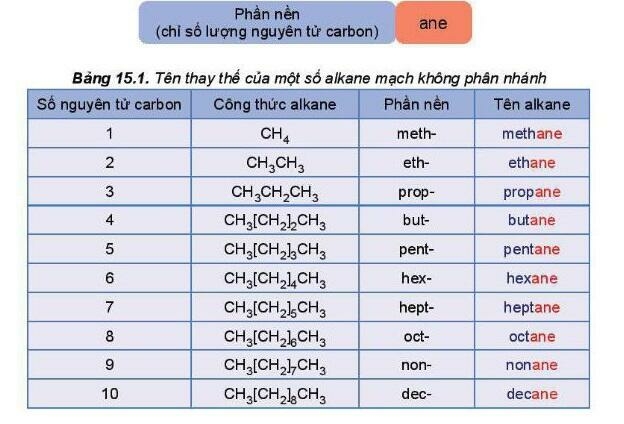
* Alkane mạch nhánh
- Gốc alkyl: Phần còn lại sau khi lấy đi một nguyên tử hydrogen từ phân tử alkane (công thức chung của gốc alkyl là CnH2n+1
Tên gốc alkyl:

- Alkane mạch nhánh gồm alkane mạch chính kết hợp với một hay nhiều nhánh.
Tên theo danh pháp thay thế của alkane mạch phân nhánh:

2. Đặc điểm cấu tạo
Trong phân tử alkane chỉ chứa các liên kết đơn C-C và C-H, các liên kết này là liên kết ở Ϭ bền vững và kém phân cực.
Trong phân tử methane, bốn liên kết C-H giống nhau tạo với nhau một gốc 109,5o và hướng về bốn đỉnh của một từ diện đều.
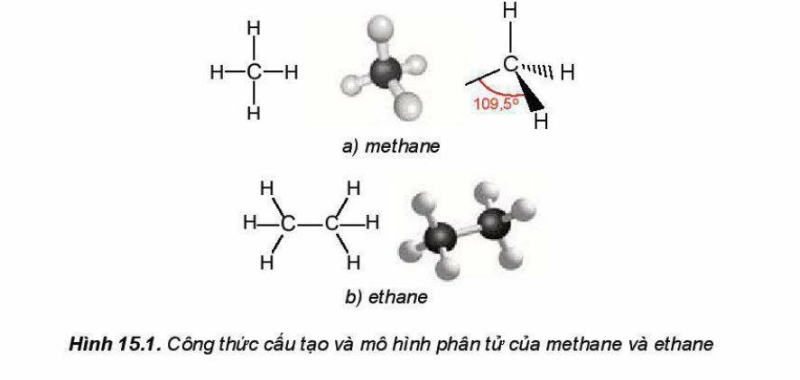
3. Tính chất vật lý
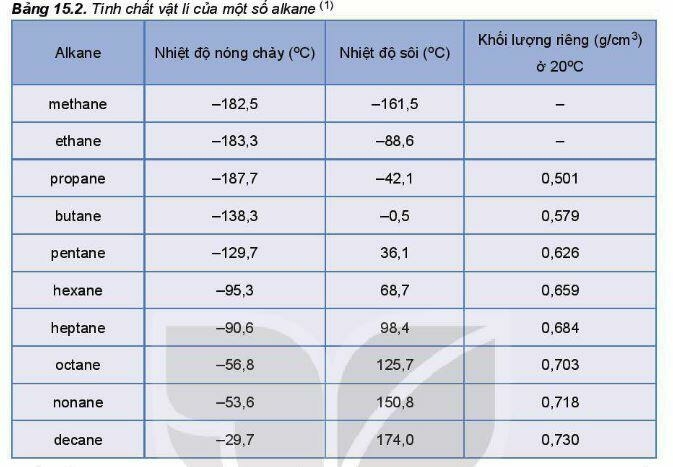
Ở điều kiện thường, alkane từ C1 đến C4 và neopentane ở trang thái khí, từ C5 đến C17 (trừ neopentane) ở trạng thái lỏng, không màu, alkane từ C18 trở lên là chất rắn màu trắng (còn gọi là sáp parafin). Các alkane mạch nhánh thường có nhiệt độ sôi thấp hơn so với đồng phân alkane mach không phân nhánh. Alkane không tan hoặc tan rất ít trong nước và nhẹ hơn nước, tan tốt hơn trong các dung môi hữu cơ.
4. Tính chất hoá học
a. Phản ứng thế
Phản ứng halogen hóa alkane là phản ứng xảy ra khi đặt bình chứa hỗn hợp của alkane với halogen ở nơi có ánh sáng hoặc ở nhiệt độ cao (đun nóng). Sản phẩm của phản ứng halogen hóa là các dẫn xuất halogen.
Phản ứng thế có thể tiếp tục diễn ra với các nguyên tử hydrogen chloromethane cho hỗn hợp các sản phẩm chloromethane, dichloromethane, trichloromethane và tetrachloromethane.
b. Phản ứng cracking
Cracking alkane là quá trình phân cắt liên kết C-C (bẻ gẫy mạch carbon) của các alkane mạch dài để tạo thành hỗn hợp các hydrocarbon có mạch carbon ngắn hơn.
c. Phản ứng reforming
Reforming alkane là quá trình chuyển các alkane mạch không phân nhánh thành các alkane mạch phân nhánh và các hydrocarbon mạch vòng nhưng không làm thay đổi.
d. Phản ứng oxi hoá
* Phản ứng oxi hoá hoàn toàn (phản ứng cháy)
Khi tiếp xúc với oxygen và có tin lớn khơi mào, alkane bị đốt cháy trở thành khí carbon dioxide, hai nước và giải phóng năng lượng.
* Phản ứng oxi hoá không hoàn toàn
Ở nhiệt độ cao, có mặt xúc tác, alkane bị oxi hoá cắt mạch carbon bởi oxygen tạo thành hỗn hợp carboxylic acid.
5. Ứng dụng
- Sử dụng làm nhiên liệu trong sản xuất và đời sống.
- Sản xuất phân bón urea, hydrogen và ammonia. Các alkane lỏng được sử dụng làm nhiên liệu xăng, diesel và nhiên liệu phản lực....
6. Điều chế
a. Phương pháp điều chế alkane
Sau khi loại bỏ các hợp chất không phải là hydrocarbon (đặc biệt là H2S và CO2), khi được dẫn qua đường ống dẫn đến nơi tiêu thụ hoặc được nên lại ở dạng lỏng để dễ dàng vận chuyển.
b. Phương pháp điều chế alkane ở thể lỏng, rắn trong công nghiệp
Khi chưng cất dầu mỏ nhận được hỗn hợp alkane có chiều dài mạch carbon khác nhau ở các phân đoạn sôi khác nhau. Để nhận được các alkane tinh khiết cần phải có các công nghệ tách và tinh chế rất phức tạp.
7. Ô nhiễm không khí do phương tiện giao thông
a. Các chất trong khí thái của phương tiện giao thông gây ô nhiễm không khí
- Quá trình cháy của xăng, dầu diesel trong động cơ các phương tiện giao thông là nguyên nhân chính gây hiệu ứng nhà kính làm Trái Đất nóng lên.
- Ngoài ra quá trình cháy tạo nhiệt độ cao khiến oxygen và nitrogen trong không khi phản ứng với nhau, tạo thành các loại oxide của nitrogen (NO2). Các chất này gây ô nhiễm môi trường không khí.
b. Một số biện pháp hạn chế ô nhiễm môi trường do các phương tiện giao thông
- Sử dụng nhiên liệu cháy sạch.
- Sử dụng nhiên liệu sinh học như xăng pha thêm ethanol (E5, E10...), blodiesel.
- Sử dụng các phương tiện giao thông tiết kiệm năng lượng và chuyển đổi sang các loại động cơ điện