Với giải Bài 1.12 trang 8 SBT Hóa Học lớp 11 Kết nối tri thức chi tiết trong Bài 1: Khái niệm về cân bằng hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa Học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 1: Khái niệm về cân bằng hóa học
Bài 1.12 trang 8 SBT Hóa 11: Phosphorus trichloride (PCl3) phản ứng với chlorine (Cl2) tạo thành phosphorus pentachloride (PCl5) theo phản ứng:
Cho 0,75 mol PCl3 và 0,75 mol Cl2 vào bình kín dung tích 8 lít ở 227oC. Tính nồng độ các chất ở trạng thái cân bằng, biết giá trị hằng số cân bằng Kc ở 227oC là 49.
Lời giải:
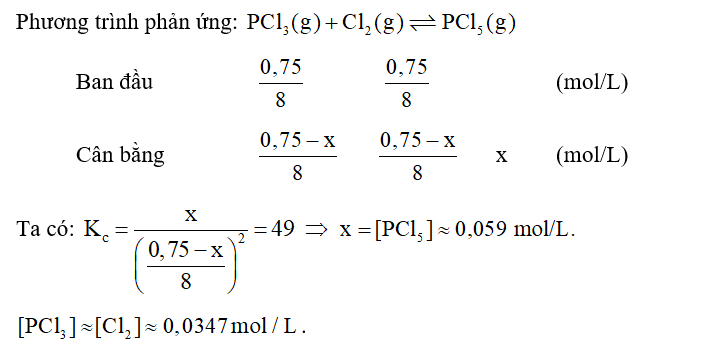
Xem thêm lời giải Sách bài tập Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 1.1 trang 5 SBT Hóa 11: Phản ứng nào sau đây là phản ứng thuận nghịch?...
Bài 1.3 trang 6 SBT Hóa 11: Cho phản ứng hoá học sau: ...
Bài 1.4 trang 6 SBT Hóa 11: Cho phản ứng hoá học sau: ...
Bài 1.5 trang 6 SBT Hóa 11: Cho phản ứng hoá học sau: ...
Bài 1.7 trang 6 SBT Hóa 11: Cho cân bằng hoá học sau:...
Bài 1.9 trang 7 SBT Hóa 11: Cho các phản ứng hoá học sau:...
Bài 1.13 trang 8 SBT Hóa 11: Trong một bình kín xảy ra cân bằng hoá học sau:...
Bài 1.15 trang 9 SBT Hóa 11: Trong dung dịch muối CoCl2 (màu hồng) tồn tại cân bằng hoá học sau:...
Xem thêm các bài giải SBT Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 1: Khái niệm về cân bằng hoá học