Với giải Bài 2.13 trang 8 SBT Hóa Học lớp 11 Cánh diều chi tiết trong Bài 2: Sự điện li trong dung dịch nước. Thuyết Br∅nsted – Lowry về acid - base giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa Học 11 . Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 2: Sự điện li trong dung dịch nước. Thuyết Br∅nsted – Lowry về acid - base
Bài 2.13 trang 8 SBT Hóa học 11: Sodium hydroxide (NaOH) là một chất điện li mạnh, trong khi methanol (CH3OH) là chất không điện li. Hãy mô tả sự khác nhau khi hoà tan các chất trên vào nước. Viết các phương trình minh hoạ.
Lời giải:
Khi hòa tan vào nước, NaOH phân li hoàn toàn thành các ion, còn CH3OH không phân li mà tồn tại chủ yếu ở dạng phân tử.
Xem thêm lời giải Sách bài tập Vật lí lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 2.1 trang 7 SBT Hóa học 11: Điền từ ngữ thích hợp vào các chỗ trống trong mỗi phát biểu sau:...
Bài 2.3 trang 7 SBT Hóa học 11: Phương trình mô tả sự điện li của NaCl trong nước là...
Bài 2.4 trang 7 SBT Hóa học 11: Phương trình mô tả sự điện li của Na2CO3 trong nước là...
Bài 2.6 trang 8 SBT Hóa học 11: Đặc điểm nào sau đây là không đúng khi mô tả về acid mạnh?...
Bài 2.7 trang 8 SBT Hóa học 11: Đặc điểm nào sau đây là không đúng khi mô tả về base yếu?...
Bài 2.10 trang 8 SBT Hóa học 11: Base liên hợp của các acid 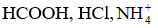
Bài 2.11 trang 8 SBT Hóa học 11: Cho phản ứng:...
Xem thêm các bài giải SBT Hóa học lớp 11 Cánh diều hay, chi tiết khác: