Với tóm tắt lý thuyết Hóa học lớp 11 Bài 5: Một số hợp chất quan trọng của nitrogen sách Cánh diều hay, chi tiết cùng với bài tập trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 11.
Lý thuyết Hóa học lớp 11 Bài 5: Một số hợp chất quan trọng của nitrogen
A. Lý thuyết Một số hợp chất quan trọng của nitrogen
I. Ammonia
1. Cấu tạo phân tử và tính chất vật lí
- Cấu tạo phân tử:
+ Được cấu tạo bởi một nguyên tử nitrogen liên kết với ba nguyên tử hydrogen và có dạng hình học là chóp tam giác.
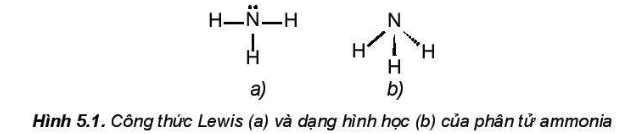
- Tính chất vật lí:
+ Ammonia tồn tại ở cả trong môi trường đất, nước, không khí.
+ Ở điều kiện thường, ammonia tồn tại ở thể khí, không màu, nhẹ hơn không khí, mùi khai và xốc, tan nhiều trong nước.
2. Tính chất hóa học
a, Tính base
- Trong dung dịch, nhận proton của nước: NH3 + H2O ⇌ NH4+ + OH-
- Có môi trường base yếu:
+ Làm quỳ tím chuyển màu xanh.
+ Làm phenolphtalein chuyển màu hồng.
- Thể hiện tính chất của một base: NH3 + HCl → NH4Cl
b, Tính khử
4NH4 + 3O2 → 2N2 + 6H2O
4NH3 + 5O2 → 4NO + 6H2O
3. Tổng hợp ammonia theo quá trình Haber
PTHH:
N2 + 3H2 ⇌ 2NH3
( nhiệt độ 400-450oC, áp suất 150-200 bar, xúc tác Fe)
II. Muối ammonium
1. Tính tan, sự điện li
- Hầu hết các muối ammonium đều dễ tan trong nước và phân li hoàn toàn ra ion.
VD: NH4Cl → NH4+ + Cl-
2. Tác dụng với kiềm – Nhận biết ion ammonuim
- Đun nóng hỗn hợp muối ammonium với dung dịch kiềm, sinh ra khí ammonia có mùi khai.
VD: NH4Cl + NaOH → NH3 + NaCl + H2O
Phương trình ion rút gọn: NH4+ + OH- → NH3 + H2O.
3. Tính chất kém bền nhiệt
- Các muối ammonuin đều kém bền nhiệt và dễ bị phân hủy khi đun nóng.
VD: NH4Cl → NH3 + HCl
III. Ứng dụng của ammonia và một số muối ammonium
- Ứng dụng của ammonia:
+ Tác nhận làm lạnh.
+ Dung môi.
+ Sản xuất nitric acid.
+ Sản xuất phân đạm.
- Ứng dụng của một số muối ammonium:
+ Chất đánh sạch bề mặt kim loại.
+ Thuốc long đờm.
+ Phân bón hóa học.
+ Chất phụ gia thực phẩm.
+ Thuốc bổ sung chất điện giải.
IV. Nguồn gốc một số oxide của nitrogen trong không khí – mưa acid
1. Nguồn gốc một số oxide của nitrogen
- Bầu khí quyển có oxide của nitrogen NOx.
- NO trong khí quyển được tạo ra khi có sấm sét.
- Hoạt động của con người.
2. Mưa acid
- Nguyên nhân chính: acid nitric và sulfuric acid hòa tan trong nước mưa.
- HÌnh thành:
SO2(g) + O2(g) → SO3(g)
SO3(g) + H2O(l) → H2So4(aq)
V. Nitric acid
Công thức Lewis:
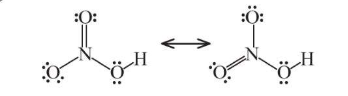
- Nitric acid là chất lỏng, không màu, có tính acid mạnh và tính oxi hóa mạnh
VI. Hiện tượng phú dưỡng
- Khái niệm: Hiện tượng phú dưỡng là sự tích tụ lớn các chất dinh dưỡng, bao gồm cả hợp chất nitrogen và hợp chất phosphorus trong các nguồn nước, do các tác động từ con người.
- Hệ quả: Làm thay đổi hệ sinh thái của nước, tích tụ bùn từ xác của tảo, làm suy kiệt nguồn thủy sản.
- Biện pháp:
+ Tạo điều kiện để nước trong kênh rạch, ao, hồ được lưu thông.
+ Xử lí nước thải trước khi cho chảy vào kênh, rạch, ao, hồ.
+ Sử dụng phân bón đúng liều lượng, đúng cách, đúng thời điểm trong năm.
Sơ đồ tư duy Một số hợp chất quan trọng của nitrogen

B. Trắc nghiệm Một số hợp chất quan trọng của nitrogen
Câu 1: Trong các phản ứng dưới đây, phản ứng nào NH3 thể hiện tính base?
A. 8NH3 + 3Cl2 6NH4Cl + N2.
B. 4NH3 + 5O2 4NO + 6H2O.
C. 2NH3 + 3CuO 3Cu + N2 + 3H2O.
D. NH3 + CO2 + H2O NH4HCO3.
Câu 2: Cho phản ứng: 2NH3 + 3Cl2 6HCl +N2. Kết luận nào sau đây đúng?
A. NH3 là chất khử.
B. NH3 là chất oxi hoá.
C. Cl2 vừa oxi hoá vừa khử.
D. Cl2 là chất khử.
Đáp án đúng là: A
Số oxi hoá của N tăng từ -3 lên 0, do đó NH3 đóng vai trò là chất khử trong phản ứng.
Câu 3: Cho các phát biểu sau:
(1) Các muối ammonium tan trong nước tạo dung dịch chất điện li mạnh;
(2) Ion NH4+ tác dụng với dung dịch acid tạo kết tủa màu trắng;
(3) Muối ammonium tác dụng với dung dịch base thu được khí có mùi khai;
(4) Hầu hết muối ammonium đều bền nhiệt.
Phát biểu đúng là
A. (1) và (3).
B. (1) và (2).
C. (2) và (4).
D. (2) và (3).
Đáp án đúng là: A
Các phát biểu (1) và (3) đúng.
Câu 4: Phú dưỡng là hiện tượng xảy ra do sự gia tăng hàm lượng của nguyên tố
A. Fe, Mn.
B. N, P.
C. Ca, Mg.
D. Cl, F.
Đáp án đúng là: B
Phú dưỡng là hiện tượng xảy ra do sự gia tăng hàm lượng của nguyên tố nitrogen (N) và phosphorus (P).
Câu 5: Phân tử nào sau đây có chứa một liên kết cho - nhận?
A. NH3
B. N2
C. HNO3
D. H2
Đáp án đúng là: C
Câu 6: Khi cho giấy quỳ tím tẩm ướt vào bình đựng khí NH3 thì giấy quỳ tím chuyển sang màu
A. đỏ.
B. xanh.
C. vàng.
D. nâu.
Đáp án đúng là: B
Khi cho giấy quỳ tím tẩm ướt vào bình đựng khí NH3 thì giấy quỳ tím chuyển sang màu xanh.
Câu 7: Cho dung dịch NH3 vào dung dịch chất nào sau đây thu được kết tủa trắng?
A. HCl.
B. H2SO4.
C. H3PO4.
D. AlCl3
Đáp án đúng là: D
3NH3 + AlCl3 + 3H2O → Al(OH)3↓ + 3NH4Cl
Câu 8: Nhiệt phân hoàn toàn muối nào sau đây thu được sản phẩm chỉ gồm khí và hơi?
A. NaCl.
B. CaCO3.
C. KClO3
D. (NH4)2CO3
Đáp án đúng là: D
Câu 9: Phân biệt được đung dịch NH4Cl và NaCl bằng thuốc thử là dung dịch
A. KCl.
B. KNO3.
C. KOH.
D. K2SO4
Đáp án đúng là: C
Phân biệt được đung dịch NH4Cl và NaCl bằng thuốc thử là dung dịch KOH.
+ Nếu có khí mùi khai thoát ra → NH4Cl.
+ Nếu không có hiện tượng xuất hiện → NaCl.
Câu 10: Chất có thể dùng để làm khô khí NH3 là
A. H2SO4 đặc.
B. P2O5.
C. CuSO4 khan.
D. KOH rắn.
Đáp án đúng là: D
KOH rắn có tác dụng hút ẩm và KOH rắn không phản ứng với NH3 nên được dùng để làm khô khí NH3.
Câu 11: Cho phản ứng:
Hệ số tỉ lượng của HNO3 trong phương trình hoá học trên là (biết hệ số tỉ lượng của các chất trong phản ứng là các số nguyên, tối giản)
A. 4.
B. 1.
C. 28.
D. 10.
Đáp án đúng là: C
Câu 12: Cho dung dịch tác dụng với các chất sau: . Số phản ứng trong đó đóng vai trò acid theo thuyết Brønsted – Lowry là
A. 4.
B. 1.
C. 3.
D. 2.
Đáp án đúng là: C
HNO3 đóng vai trò acid theo thuyết Brønsted – Lowry khi phản ứng với NH3, CaCO3, NaOH.
Câu 13: Cho Iron(III) oxide tác dụng với nitric acid thì sản phẩm thu được là
A. Fe(NO3)3, NO và H2O.
B. Fe(NO3)3, NO2 và H2O.
C. Fe(NO3)3, N2 và H2O.
D. Fe(NO3)3 và H2O.
Đáp án đúng là: D
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
Câu 14: Cho m gam Al phản ứng hoàn toàn với dung dịch HNO3 loãng (dư), thu được 4,958 lít khí NO (đkc, sản phẩm khử duy nhất). Giá trị của m là
A. 4,05.
B. 2,70.
C. 8,10.
D. 5,40.
Đáp án đúng là: D
PTHH:
Theo phương trình: nAl = nNO = 0,2 (mol)
→ mAl = 0,2.27 = 5,4 (g).
Câu 15: Cho 19,2 gam kim loại M tan hết trong dung dịch HNO3 dư thu được 4,958 lít khí NO duy nhất (đkc). Kim loại M là
A. Fe.
B. Mg.
C. Al.
D. Cu.
Đáp án đúng là: D
Áp dụng định luật bảo toàn electron: ne nhường = ne nhận
=> (với n là hoá trị của kim loại).
Vậy n = 2; M = 64 thoả mãn. Kim loại là Cu.
Xem thêm các bài tóm tắt Hóa học lớp 11 Cánh Diều hay, chi tiết khác: