Với giải Câu hỏi thảo luận 4 trang 36 Hóa học lớp 11 Chân trời sáng tạo chi tiết trong Bài 6: Sulfur và sulfur dioxide giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 11. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 11 Bài 6: Sulfur và sulfur dioxide
Câu hỏi thảo luận 4 trang 36 Hóa học 11: Nêu hiện tượng xảy ra ở Thí nghiệm 1. Xác định vai trò của các chất trong phản ứng của Fe và S ở thí nghiệm này.
Lời giải:
Hiện tượng: Khi đốt nóng hỗn hợp, lưu huỳnh nóng chảy, tiếp theo hỗn hợp cháy sáng đỏ. Kết thúc phản ứng thu được hợp chất có màu đen. Phản ứng tỏa nhiều nhiệt.
Phương trình hoá học:
Vậy trong phản ứng này, Fe đóng vai trò là chất khử còn S đóng vai trò là chất oxi hoá.
Lý thuyết Đơn chất Sulfur
a) Trạng thái tự nhiên:
- Trong tự nhiên, sulfur lắng đọng thành những mỏ lớn, nằm giữa lớp đá sâu hàng trăm mét.
- Khoáng vật trong tự nhiên chứa sulfur ở dạng hợp chất: quặng pyrite (FeS2), quặng gypsum (CaSO4.2H2O), quặng galena (PbS), quặng barite (BaSO4).
b) Cấu tạo, tính chất vật lý cơ bản của sulfur đơn chất
- Ở dạng phân tử, 8 nguyên tử liên kết cộng hóa trị với nhau tạo thành mạch vòng. Kí hiệu là S.
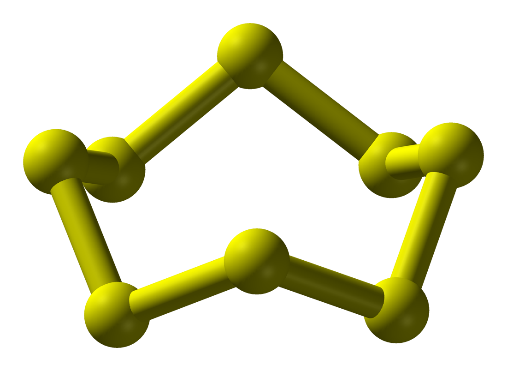
Hình 1: Phân tử sulfur ở điều kiện thường
-Ở điều kiện thường sulfur là: chất rắn, màu vàng, không tan trong nước, tan nhiều trong dung môi hữu cơ (benzine, carbon disulfide,…)
c) Tính chất hóa học
- Tính oxi hóa: sulfur oxi hóa được nhiều kim loại (trừ Au, Pt, Ag) ở nhiệt độ cao -> Muối sulfide
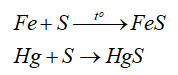
-Tính khử:
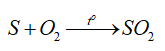
d) Ứng dụng
- Sulfur có nhiều ứng dụng như: điều chế H2SO4, lưu hóa cao su, chế tạo diêm, sản xuất chất tẩy trắng bột giấy, chất dẻo ebonit, dược phẩm, phẩm nhuộm, chất trừ sâu và chất diệt nấm trong nông nghiệp,…
Xem thêm lời giải bài tập Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Câu hỏi thảo luận 3 trang 36 Hóa học 11: Quan sát Hình 6.4, mô tả cấu tạo phân tử sulfur....
Câu hỏi thảo luận 9 trang 38 Hóa học 11: Giải thích sự hình thành mưa acid từ sulfur dioxide....
Bài 1 trang 39 Hóa học 11: Tính chất nào sau đây không phải là tính chất vật lí của sulfur?...
Bài 2 trang 39 Hóa học 11: Số oxi hoá của sulfur trong phân tử SO2 là...
Bài 3 trang 39 Hóa học 11: Cho các phản ứng sau:...
Xem thêm các bài giải SGK Hóa lớp 11 Chân trời sáng tạo hay, chi tiết khác: