Với giải sách bài tập Hóa học 11 Bài 20: Alcohol sách Kết nối tri thức hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 20: Alcohol
Bài 20.1 trang 69 Sách bài tập Hóa học 11: Công thức tổng quát của alcohol no, đơn chức, mạch hở là
A. CnH2n-5OH.
B. CnH2n(OH)2.
C. CnH2n-1OH.
D. CnH2n+1OH.
Lời giải:
Đáp án đúng là: D
Công thức tổng quát của alcohol no, đơn chức, mạch hở là CnH2n+1OH.
Bài 20.2 trang 69 Sách bài tập Hóa học 11: Số đồng phân cấu tạo alcohol có công thức C4H9OH là
A. 2.
B. 3.
C. 4.
D. 5.
Lời giải:
Đáp án đúng là: C
Các đồng phân cấu tạo alcohol có công thức C4H9OH là:
CH3CH2CH2CH2OH; CH3CH2CHOHCH3; (CH3)2CHOHCH3; (CH3)2CHCH2OH.
Bài 20.3 trang 70 Sách bài tập Hóa học 11: Chất nào sau đây là alcohol bậc II?
A. propan-1-ol.
B. propan-2-ol.
C. 2-methylpropan-1-ol.
D. 2-methylpropan-2-ol.
Lời giải:
Đáp án đúng là: B
Hợp chất propan-2-ol có công thức là CH3CH(OH)CH3. Nhóm –OH gắn với carbon bậc 2 nên propan-2-ol là alcohol bậc II.
Bài 20.4 trang 70 Sách bài tập Hóa học 11: Cho alcohol có công thức cấu tạo sau:
Tên theo danh pháp thay thế của alcohol đó là
A. 4-methylpentan-1-ol.
B. 2-methylbutan-3-ol.
C. 3-methylbutan-2-ol.
D. 1,1-dimethylpropan-3-ol.
Lời giải:
Đáp án đúng là: A
Tên theo danh pháp thay thế của alcohol đó là 4-methylpentan-1-ol.
A. CH3OH.
B. C2H5OH.
C. C3H7OH.
D. C2H4(OH)2.
Lời giải:
Đáp án đúng là: A
Công thức phân tử của methanol là CH3OH.
Bài 20.6 trang 70 Sách bài tập Hóa học 11: Cho các hợp chất hữu cơ sau:
(1) C3H8; (2) CH3Cl; (3) C2H5OH; (4) CH3OH.
Thứ tự giảm dần nhiệt độ sôi của các chất trên là
A. (1) > (2) > (3) > (4).
B. (1) > (4) > (2) > (3).
C. (3) > (4) > (2) > (1).
D. (4) > (2) > (1) > (3).
Lời giải:
Đáp án đúng là: C
Alcohol có nhiệt độ sôi > dẫn xuất halogen > hydrocarbon.
Alcohol có phân tử khối càng lớn thì nhiệt độ sôi càng cao.
A. 17o.
B. 7o.
C. 70o.
D. 170o
Lời giải:
Đáp án đúng là: C
Độ cồn (độ rượu) là số ml rượu nguyên chất có trong 100 mL rượu và nước.Vậy hỗn hợp trên có độ cồn là 70o.
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án đúng là: B
Các hợp chất hữu cơ có công thức phân tử C3H8O phản ứng được với Na là hợp chất thuộc alcohol.
Các công thức cấu tạo phù hợp là:
CH3CH2CH2OH; CH3CHOHCH3.
Bài 20.9 trang 70 Sách bài tập Hóa học 11:Cho phản ứng hoá học sau:
Sản phẩm chính theo quy tắc Zaitsev trong phản ưng trên là
A. but-1-ene.
B. but-2-ene.
C. but-1-yne.
D. but-2-yne
Lời giải:
Đáp án đúng là: B
Theo quy tắc tách Zaitsev, phản ứng xảy ra như sau:
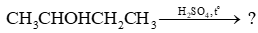
Sản phẩm chính thu được có tên là but-2-ene.
A. CH3CHO.
B. CH3CH2CHO.
C. CH3COCH3.
D. CH3COOH.
Lời giải:
Đáp án đúng là: C
Sản phẩm thu được là CH3COCH3.
Bài 20.11 trang 71 Sách bài tập Hóa học 11: Thuốc thử Cu(OH)2 dùng để nhận biết alcohol nào sau đây?
A. Alcohol bậc I.
B. Alcohol bậc II.
C. Alcohol bậc III.
D. Alcohol đa chức.
Lời giải:
Đáp án đúng là: D
Thuốc thử Cu(OH)2 dùng để nhận biết alcohol đa chức có nhiều nhóm -OH liền kề.
Bài 20.12 trang 71 Sách bài tập Hóa học 11: Khi đốt cháy hoàn toàn ethanol, thu được tỉ lệ mol
A. 1 : 1.
B. 1 : 2.
C. 2 : 3.
D. 3 : 2.
Lời giải:
Đáp án đúng là: C
Tỉ lệ mol = 2 : 3.
A. Ethylene.
B. Acetylene.
C. Methane.
D. Tinh bột.
Lời giải:
Đáp án đúng là: D
Sơ đồ điều chế:
Vậy chất dùng để điều chế ethanol theo phương pháp sinh hoá là tinh bột.
A. Na.
B. CuSO4 khan.
C. CuO, to.
D. Cu(OH)2.
Lời giải:
Đáp án đúng là: B
Hiện tượng CuSO4 khan màu trắng sẽ hấp thụ nước có trong cồn 90o tạo thành CuSO4 màu xanh.
Bài 20.15 trang 71 Sách bài tập Hóa học 11: Hai ancol nào sau đây cùng bậc?
A. Methanol và ethanol.
B. Propan-1-ol và propan-2-ol.
C. Ethanol và propan-2-ol.
D. Propan-2-ol và 2-methylpropan-2-ol,
Lời giải:
Đáp án đúng là: A
Methanol (CH3OH) và ethanol (C2H5OH) đều là alcohol bậc I.
Bài 20.16 trang 71 Sách bài tập Hóa học 11: Alcohol CH3CH=CHCH2OH có danh pháp thay thế là
A. but-2-en-4-ol.
B. but-2-en-1-ol.
C. 4-hydroxybut-2-ene.
D. 1-hydroxybut-2-ene.
Lời giải:
Đáp án đúng là: B
Alcohol CH3CH=CHCH2OH có danh pháp thay thế là but-2-en-1-ol.
A. nước.
B. cồn 96o.
C. thùng rác.
D. dầu hoả.
Lời giải:
Đáp án đúng là: B
Mẩu Na dư sẽ phản ứng êm dịu với cồn 96o.
2C2H5OH + 2Na → 2C2H5ONa + H2
A. 18,75 mL.
B. 300 mL.
C. 400 mL.
D. 750 mL.
Lời giải:
Đáp án đúng là: B
Số mL ethanol nguyên chất (khan) có trong chai rượu đó là:
A. 50 mL.
B. 92 mL.
C. 46 mL.
D. 100 mL.
Lời giải:
Đáp án đúng là: D
Thể tích ethanol có trong lượng xăng trên là:
Bài 20.20 trang 72 Sách bài tập Hóa học 11: Cho các alcohol sau:
Số alcohol không hoà tan được Cu(OH)2 là
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án đúng là: C
Các alcohol không hoà tan được Cu(OH)2 là CH3OH, C2H5OH, CH2(OH)CH2CH2(OH).
Bài 20.21 trang 72 Sách bài tập Hóa học 11: Nhận xét nào sau đây không đúng?
A. Oxi hoá không hoàn toàn alcohol bậc I, thu được aldehyde.
B. Oxi hoá hoàn toàn alcohol bậc I, thu được aldehyde.
C. Oxi hoá alcohol bậc II, thu được ketone.
D. Alcohol bậc III không bị oxi hoá bởi tác nhân thông thường.
Lời giải:
Đáp án đúng là: B
Oxi hoá hoàn toàn alcohol bậc I, thu được CO2 và H2O.
A. 3-metylbut-1-ene.
B. 2-methylbut-2-ene.
C. 3-methylbut-2-ene.
D. 2-methylbut-3-ene.
Lời giải:
Đáp án đúng là: B
Sản phẩm chính có tên là 2-methylbut-2-ene.
Bài 20.23 trang 72 Sách bài tập Hóa học 11: Oxi hoá alcohol nào sau đây thu được sản phẩm là ketone?
A. C2H5OH.
B. CH3CH2CH2OH.
C. CH3CH(OH)CH3.
D. (CH3)2C(OH)CH3.
Lời giải:
Đáp án đúng là: C
Phương trình phản ứng:
A. Cho hỗn hợp khí ethylene và hơi nước đi qua tháp chứa H3PO4.
B. Cộng nước vào ethylene với xúc tác là H2SO4.
C. Lên men tinh bột.
D. Thuỷ phân dẫn xuất C2H5Br trong môi trường kiềm.
Lời giải:
Đáp án đúng là: C
Sản xuất ethanol sinh học bằng lên men tinh bột:
Sơ đồ điều chế:
Bài 20.25 trang 72 Sách bài tập Hóa học 11: Cho dãy chuyển hoá sau:
Biết X và Y đều là sản phẩm chính, công thức cấu tạo của X, Y lần lượt là
A. CH3CH=CHCH3 và CH3CH2CHBrCH3.
B. C4H9-O-C4H9 và CH3CH2CHBrCH3.
C. CH2=CHCH2CH3 và CH3CH2CHBrCH3.
D. CH2=CHCH2CH3 và CH3CH2CH2CH2Br.
Lời giải:
Đáp án đúng là: A
Phương trình phản ứng:
b) Đun nóng một trong các alcohol trên với H2SO4 đặc, thu được alkene có tên gọi là 3-methylbut-1-ene, xác định công thức của alcohol đó.
Lời giải:
a) C5H11OH có 4 đồng phân alcohol bậc I là:
CH3CH2CH2CH2CH2OH; (CH3)2CHCH2CH2OH;
HOCH2CH(CH3)CH2CH3; (CH3)3CCH2OH.
b)
Như vậy tách nước từ (CH3)2CHCH2CH2OH được 3-methylbut-1-ene
Lời giải:
2C2H5OH + 2Na → 2C2H5ONa + H2
Kết tủa trắng là C2H5ONa, khi thêm nước vào kết tủa tan do xảy ra phản ứng:
C2H5ONa + H2O→ C2H5OH + NaOH
Do có NaOH tạo thành làm phenolphtalein chuyển màu hồng.
a) Viết phương trình hoá học của phản ứng xảy ra.
b) Tại sao lại dùng phương pháp đẩy nước để thu khí ethylene.
c) Nêu tác dụng của bông tẩm dung dịch NaOH.
d) Đề xuất thí nghiệm để nhận biết khí tạo thành.
Lời giải:
a)
b) Khí ethylene hầu như không tan trong nước nên có thể sử dụng phương pháp đẩy nước để thu khí ethylene.
c) Bông tẩm dung dịch NaOH để hấp thụ các tạp chất tạo thành trong quá trình phản ứng như SO2, CO2.
d) Dẫn khí thoát ra sục vào ống nghiệm chứa nước bromine hoặc thuốc tím, các ống nghiệm này sẽ mất màu chứng tỏ có khí ethylene tạo thành.
Lời giải:
100 L cồn y tế 70o chứa 70 L ethanol nguyên chất, tương đương với:
70.0,789 = 55,23 (kg).
1mol 2 mol
Số mol ethanol tạo thành:
Số mol glucose cần thiết:
Khối lượng glucose cần thiết: 7,5.103.192 = 1 440.103 (g) = 1 440 (kg)
Lời giải:
100 mL cồn 90o chứa 90 mL cồn nguyên chất.
Số mol ethanol tương ứng:
Nhiệt lượng tỏa ra: 1,5437.1 371= 2 116,4 (kJ).
Lời giải:
Phổ IR của X có peak hấp thụ rộng ở vùng 3 300 cm-1: có nhóm –OH.
Phổ IR của Y có peak hấp thụ rộng ở vùng 1 700 cm-1: có nhóm C=O.
Vậy X là benzyl alcohol, Y là aldehyde benzoic.
Lời giải:
(C6H10O5)n + nH2O → nC6H12O6 (1)
C6H12O6 → 2C2H5OH + 2CO2 (2)
Khối lượng tinh bột = 106.0,75 = 75.104 (g)
Từ (1) và (2) ta có:
Do hiệu suất chung của cả quá trình là 70% nên thể tích ethanol thực tế thu được là:
Thể tích xăng E5 là:
Xem thêm các bài giải SBT Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác:
Lý thuyết Alcohol
1. Khái niệm, danh pháp
a. Khái niệm
Alcohol là những hợp chất hữu cơ trong phân tử có chứa nhóm hydroxy (–OH) liên kết với nguyên tử carbon no.
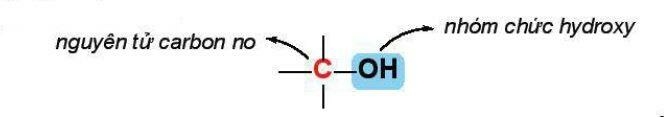
Alcohol no, đơn chức, mạch hở trong phân tử có một nhóm -OH liên kết với gốc alkyl, có công thức tổng quát là CnH2n+1OH (n≥1)
Nếu alcohol có hai hay nhiều nhóm –OH thì các alcohol đó được gọi là các alcohol đa chức (polyalcohol).
Bậc của alcohol là bậc của nguyên tử carbon liên kết với nhóm hydroxy. Ta có alcohol bậc 1, alcohol bậc II và alcohol bậc III.
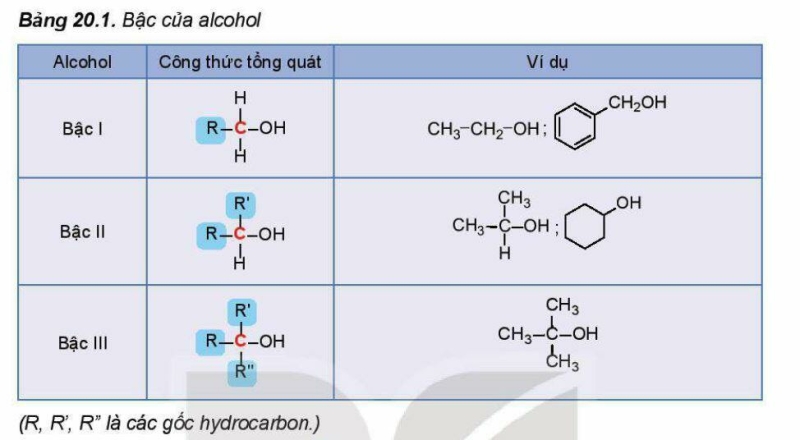
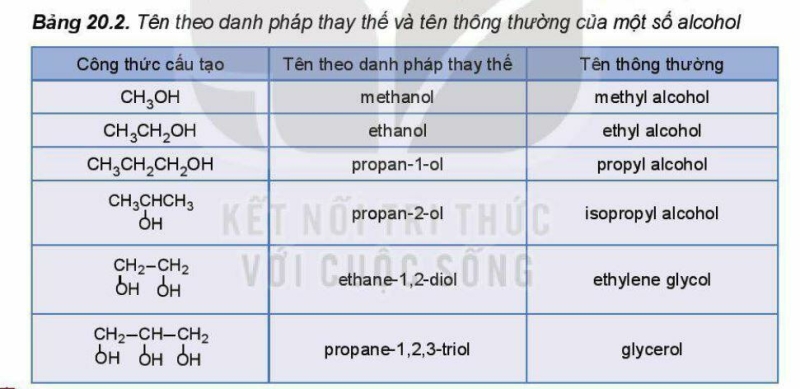
b. Danh pháp
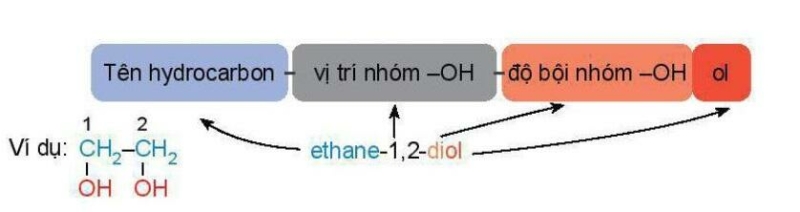
* Danh pháp thay thế:
Tên theo danh pháp thay thế của moncalcohol:
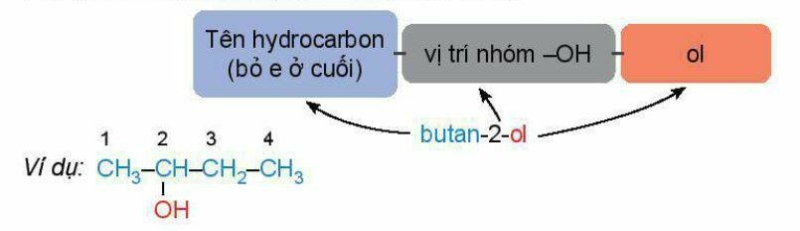
Tên theo danh pháp thay thế của polyalcohol:
2. Đặc điểm cấu tạo
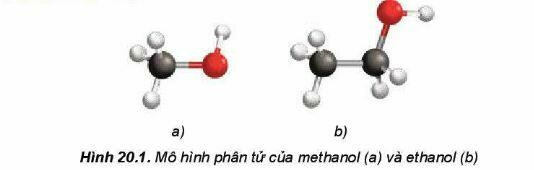
Trong phần tử alcohol, các liên kết O-H và C-O đều phân cực về phía nguyên tử oxygen do oxygen có độ âm điện lớn. Do đó, trong các phản ứng hoá học, alcohol thường bị phân cắt ở liên kết O-H hoặc liên kết C-O.
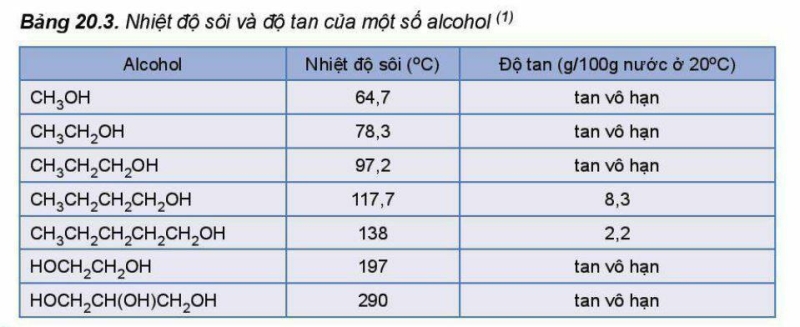
3. Tính chất vật lí
Ở điều kiện thường, các alcohol no, đơn chức từ C1 đến C12 ở trạng thái lỏng, các alcohol từ C13 trở lên ở trạng thái rắn.
Các polyalcohol như ethylene glycol, glycerol là chất lỏng sánh, nặng hơn nước và có vị ngọt.
Alcohol có nhiệt độ sôi cao hơn các hydrocarbon, dẫn xuất halogen có phân tử khối tương đương và dễ tan trong nước do các phân tử alcohol có thể tạo liên kết hydrogen với nhau và với nước.
4. Tính chất hóa học
a. Phản ứng thế nguyên tử H của nhóm -OH
Liên kết O-H phân cực nên trong một số phản ứng, nguyên tử hydrogen trong nhóm hydroxy có thể bị thay thế.
2R- OH + 2Na → 2RONa + H2
b. Phản ứng tạo ether
Khi đun nóng alcoho với H2SO4 đặc ở nhiệt độ thích hợp thì thu được ether.
c. Phản ứng tạo alkene
Khi cho hơi alcohol no, đơn chức, mạch hở đi qua bột Al2O3 nung nóng hoặc đun alcohol với H2SO4 đặc, H3PO4 đặc, alcohol bị tách nước tạo thành alkene.
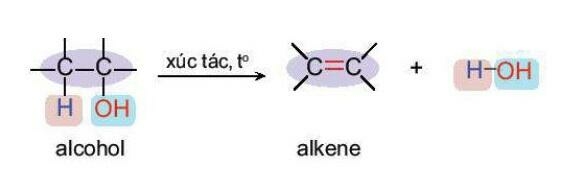
d. Phản ứng oxi hóa
* Oxi hoá không hoàn toàn
Khi phản ứng với các chất oxi hoá (ví dụ: CuO), các alcohol bị oxi hoá không hoàn toàn tạo thành các sản phẩm khác nhau tuỳ theo bác của alcohol: alcohol bậc I bị oxi hoa thành aldehyde, alcohol bậc II bị oxi hoá thành ketone, alcohol bậc III không bị oxi hoá trong điều kiện này.
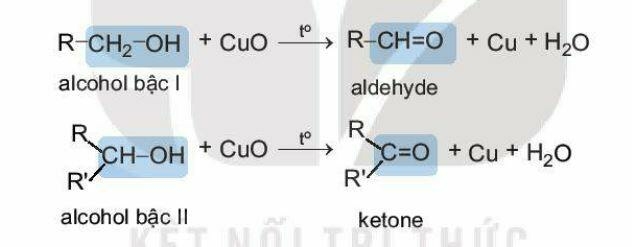
* Phản ứng cháy của alcohol
Các alcohol có thể bị đốt cháy trong không khí tạo thành carbon dioxide, hơi nước và toả nhiệt:
CnH2n+1OH + 3n/2 O2 → nCO2 + (n+1)H2O (điều kiện: t0)
e. Phản ứng riêng của polyalcahol với Cu(OH)2
Các polyalcohol có các nhóm -OH liền kề như ethylene glycol, glycerol có thể tác dụng với copper(||) hydroxide tạo dung dịch màu xanh lam đậm.
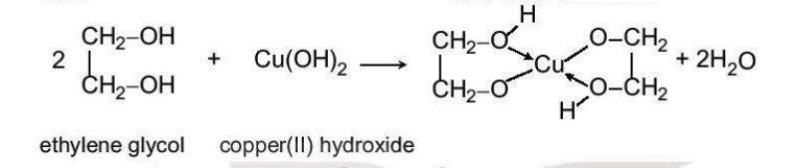
5. Ứng dụng
a. Ứng dụng của alcohol
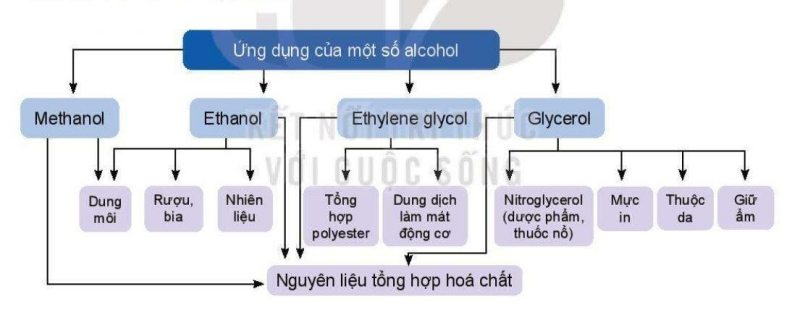
b. Ảnh hưởng của rượu, bia và đồ uống có cồn đến sức khỏe con người
Việc lạm dụng rượu, bia và đồ uống có cồn sẽ gây ảnh hưởng nghiêm trọng đến sức khỏe con người như tổn thương hệ thần kinh, rối loạn tâm thần, viêm gan, xơ gan,…
6. Điều chế
a. Hydrate hoá alkene
Các alcohol có thể được điều chế bằng phản ứng hydrate hóa alkene. Phương pháp này được sử dụng phổ biến trong công nghiệp để điều chế ethanol
CH2=CH2 + H2O → C2H5OH (điều kiện H3PO4, t0)
b. Điều chế ethanol bằng phương pháp sinh hoá
Khi lên men tinh bột, enzyme sẽ phân giải tinh bột thành glucose, sau đó giucose sẽ chuyển hoá thành ethanol.
Phương pháp sinh hóa được sử dụng phổ biến để sản xuất các đồ uống có cồn, điều chế ethanol làm nhiên liệu sinh học.
c. Điều chế glycerol
Trong công nghiệp, glycerol được tổng hợp từ propylene theo sơ đồ sau:
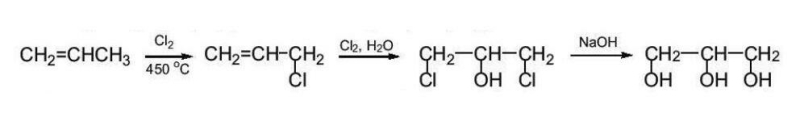
Ngoài ra, glycerol còn thu được khi thuỷ phân chất béo trong quá trình sản xuất xà phòng.