Tailieumoi.vn xin giới thiệu đến các quý thầy cô Giáo án Hóa học 12 tiết 1: ôn tập đầu năm mới nhất theo mẫu Giáo án môn hóa học chuẩn của Bộ Giáo dục. Hi vọng tài liệu này sẽ giúp thầy/cô dễ dàng biên soạn chi tiết Giáo án môn Hóa học lớp. Chúng tôi rất mong sẽ được thầy/cô đón nhận và đóng góp những ý kiến quý báu của mình.
Mời các quý thầy cô cùng tham khảo và tải về chi tiết tài liệu dưới đây:
Tiết 1: ÔN TẬP ĐẦU NĂM
I. MỤC TIÊU:
1. Kiến thức:
HS Biết được:
- Ôn tập, củng cố, hệ thống hoá các chương hoá học đại cương và vô cơ (sự điện li, nitơ-photpho, cacbon-silic); các chương về hoá học hữu cơ (Đại cương về hoá học hữu cơ, hiđrocacbon, dẫn xuất halogen –ancol – phenol , anđehit – xeton – axit cacboxylic).
- Rèn luyện kĩ năng dựa vào cấu tạo của chất để suy ra tính chất và ứng dụng của chất. Ngược lại, dựa vào tính chất của chất để dự đoán công thức của chất.
2. Năng lực
* Các năng lực chung
- Năng lực tự học
- Năng lực hợp tác
- Năng lực phát hiện và giải quyết vấn đề
- Năng lực giao tiếp
* Các năng lực chuyên biệt
- Năng lực sử dung ngôn ngữ
- Năng lực thực hành hóa học
- Năng lực tính toán
- Năng lực giải quyết vấn đề thông qua hóa học
- Năng lực vận dụng kiến thức hóa học vào cuộc sống
3. Phẩm chất
Yêu gia đình, quê hương đất nước; Nhân ái khoan dung; Trung thực, tự trọng, chí công, vô tư; Tự lập, tự tin, tự chủ; Có trách nhiệm với bản thân, cộng đồng, đất nước, nhân loại; Nghĩa vụ công dân.
II. THIẾT BỊ DẠY HỌC VÀ HỌC LIỆU
1. Giáo viên:
Yêu cầu HS lập bảng tổng kết kiến thức của từng chương theo sự hướng dẫn của GV trước khi học tiết ôn tập đầu năm.
2. Học sinh:
Chuẩn bị bài ở nhà.
III. TIẾN TRÌNH DẠY HỌC
A. HOẠT ĐỘNG KHỞI ĐỘNG: (10 phút)
a) Mục tiêu: Tạo không khí vui vẻ trong lớp học, khơi gợi hứng thú của HS vào tiết học. HS tiếp nhận kiến thức chủ động, tích cực ,hiệu quả.
b) Nội dung: Kiểm tra kiến thức
c) Sản phẩm: HS tham gia bốc thăm, bầu nhóm trưởng
d. Tổ chức thực hiện:
GV chia lớp thành 4 nhóm, tiến hành cho các lớp bốc thăm chủ đề ứng với các chương ở lớp 11.
B. HOẠT ĐỘNG HÌNH THÀNH KIẾN THỨC MỚI
HOẠT ĐỘNG CỦA GIÁO VIÊN VÀ HỌC SINH SẢN PHẨM DỰ KIẾN
Hoạt động 1: Sự điện li
a) Mục tiêu: Học sinh hiểu được sự điện li
b) Nội dung: Làm việc với sách giáo khoa, thảo luận nhóm.
c) Sản phẩm: Khái niệm điện li
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ:
GV lưu ý HS:
- Ở đây chỉ xét dung môi là nước.
- Sự điện li còn là quá trình phân li các chất thành ion khi nóng chảy.
- Chất điện li là chất khi nóng chảy phân li thành ion.
- Không nói chất điện li mạnh là chất khi tan vào nước phân li hoàn toàn thành ion.
Thí dụ: H2SO4 là chất điện li mạnh, nhưng:
H2SO4 → H+ +
↔ H+ +
Bước 2: Thực hiện nhiệm vụ:
HS lắng nghe và trả lời câu hỏi
Bước 3: Báo cáo thảo luận
HS trình bày kết quả
Bước 4: Kết luận, nhận định:
GV nhận xét, chốt kiến thức.
I – SỰ ĐIỆN LI
1. Sự điện li
Hoạt động 2: Axit, bazo và muối
a) Mục tiêu: Học sinh hiểu được khái niệm Axit, bazo và muối
b) Nội dung: Làm việc với sách giáo khoa, thảo luận nhóm.
c) Sản phẩm: Khái nhiệm Axit, bazo và muối
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ:
GV có thể lấy một số thí dụ nếu cần thiết.
Bước 2: Thực hiện nhiệm vụ:
HS nhắc lại các khái niệm axit, bazơ, muối, hiđroxit lưỡng tính.
Bước 3: Báo cáo thảo luận
HS trình bày kết quả
Bước 4: Kết luận, nhận định:
GV nhận xét, chốt kiến thức. 2. Axit, bazơ và muối
Hoạt động 3: Phản ứng trao đổi ion trong dung dịch các chất điện li
a) Mục tiêu: Học sinh hiểu được khái niệm, định nghĩa và các kiến thức liên quan
b) Nội dung: Làm việc với sách giáo khoa, thảo luận nhóm.
c) Sản phẩm: Học sinh nắm chắc được kiến thức.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ:
GV : Bản chất của phản ứng trao đổi ion là gì?
Bước 2: Thực hiện nhiệm vụ:
HS nhắc lại điều kiện để xảy ra phản ứng trao đổi ion.
Bước 3: Báo cáo thảo luận
HS trình bày kết quả
Bước 4: Kết luận, nhận định:
GV nhận xét, chốt kiến thức. 3.
Hoạt động 4: Nitơ, Photpho – Cacbon, Silic
a) Mục tiêu: Học sinh hiểu được khái niệm, định nghĩa và các kiến thức liên quan
b) Nội dung: Làm việc với sách giáo khoa, thảo luận nhóm.
c) Sản phẩm: Học sinh nắm chắc được kiến thức.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ:
HS nghiên cứu sgk, thảo luận nhóm để hoàn thành phiếu học tập.
Bước 2: Thực hiện nhiệm vụ:
HS lắng nghe và trả lời câu hỏi
Bước 3: Báo cáo thảo luận
HS trình bày kết quả
Bước 4: Kết luận, nhận định:
GV nhận xét, chốt kiến thức. I. Nitơ
Cấu hình electron: 1s22s22p3
Độ âm điện: 3,04
Cấu tạo phân tử: N ≡ N (N2)
Các số oxi hoá: -3, 0, +1, +2, +3, +4, +5
HNO3 là axit mạnh, có tính oxi hoá mạnh.
2. Photpho
Cấu hình electron: 1s22s22p63s23p3
Độ âm điện: 2,19
Cấu tạo phân tử: P4 (photpho trắng); Pn (photpho đỏ)
Các số oxi hoá: -3, 0, +3, +5
H3PO4 là axit 3 nấc, độ mạnh trung bình, không có tính oxi hoá như HNO3.
3. Cacbon
Cấu hình electron: 1s22s22p2
Các dạng thù hình: Kim cương, than chì, fuleren
Đơn chất: Cacbon thể hiện tính khử là chủ yếu, ngoài ra còn thể hiện tính oxi hoá.
Hợp chất: CO, CO2, axit cacbonic, muối cacbonat.
CO: Là oxit trung tính, có tính khử mạnh.
CO2: Là oxit axit, có tính oxi hoá.
H2CO3: Là axit rất yếu, không bền, chỉ tồn tại trong dung dịch.
4. Silic
Cấu hình electron: 1s22s22p63s23p2
Các dạng tồn tại: Silic tinh thể và silic vô định hình.
Đơn chất: Silic vừa thể hiện tính khử, vừa thể hiện tính oxi hoá.
Hợp chất: SiO2, H2SiO3, muối silicat.
SiO2: Là oxit axit, không tan trong nước.
H2SiO3: Là axit, ít tan trong nước (kết tủa keo), yếu hơn cả axit cacbonic
Hoạt động 5: Đại cương hóa hữu cơ
a) Mục tiêu: Học sinh hiểu được khái niệm, định nghĩa và các kiến thức liên quan
b) Nội dung: Làm việc với sách giáo khoa, thảo luận nhóm.
c) Sản phẩm: Học sinh nắm chắc được kiến thức.
d) Tổ chức thực hiện:
Bước 1: Chuyển giao nhiệm vụ:
GV yêu cầu HS cho biết các loại hợp chất hữu cơ đã được học.
Bước 2: Thực hiện nhiệm vụ:
HS lắng nghe và trả lời câu hỏi
Bước 3: Báo cáo thảo luận
HS trình bày kết quả
Bước 4: Kết luận, nhận định:
GV nhận xét, chốt kiến thức.
SẢN PHẨM DỰ KIẾN
IV – ĐẠI CƯƠNG HOÁ HỮU CƠ
Hoạt động 5:
- Đồng đẳng: Những hợp chất hữu cơ có thành phần phân tử hơn kém nhau một hay nhiều nhóm CH2 nhưng có tính chất hoá học tương tự nhau là những chất đồng đẳng, chúng hợp thành dãy đồng đẳng.
- Đồng phân: Những hợp chất hữu cơ khác nhau có cùng CTPT gọi là các chất đồng phân.
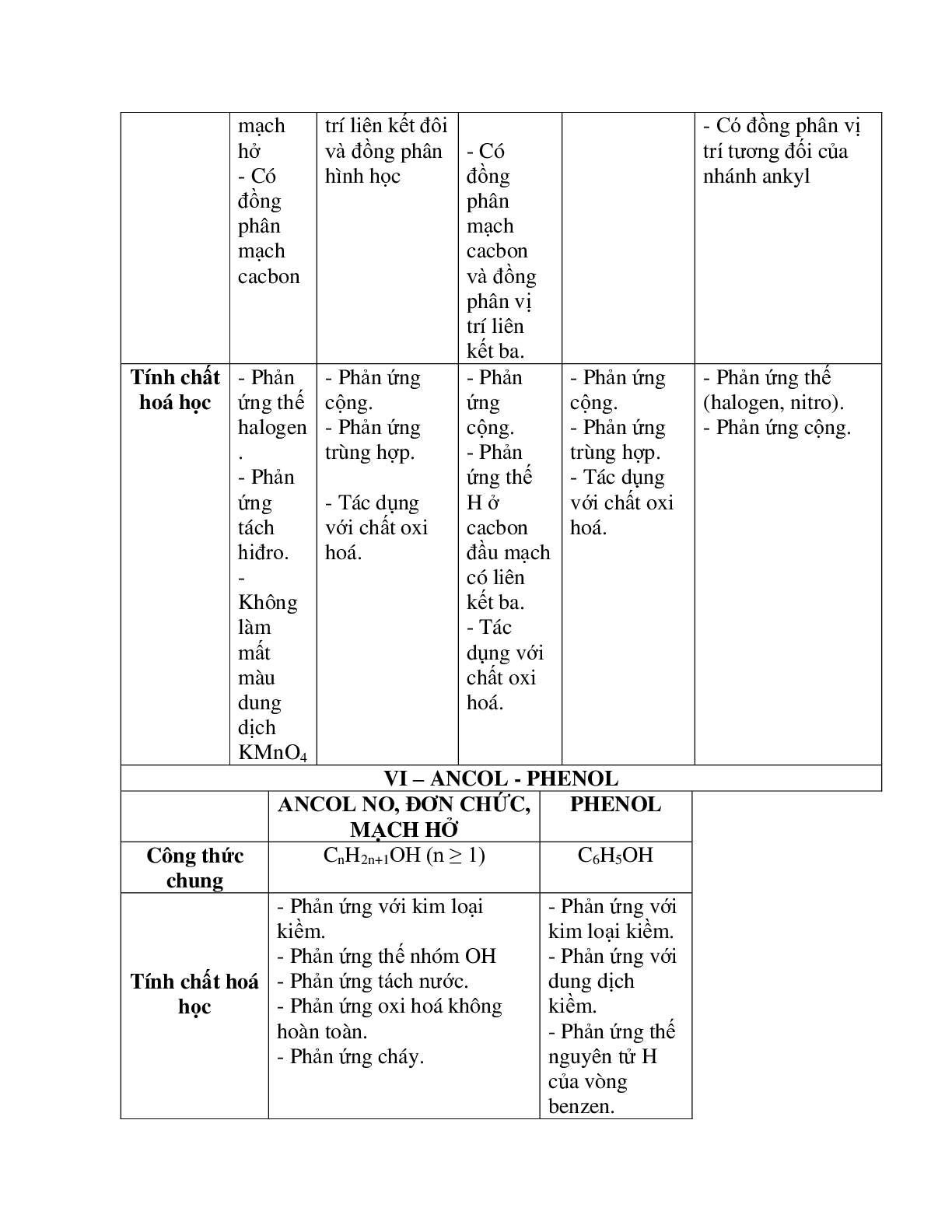
V – HIĐROCACBON
ANKAN ANKEN ANKIN ANKAĐIEN ANKYLBEZEN
Công thức chung CnH2n+2 (n ≥ 1) CnH2n (n ≥ 2) CnH2n-2 (n ≥ 2) CnH2n-2 (n ≥ 3) CnH2n-6 (n ≥ 6)
Đặc
Điểm cấu tạo
- Chỉ có liên kết đơn chức, mạch hở
- Có đồng phân mạch cacbon
- Có 1 liên kết đôi, mạch hở
- Có đp mạch cacbon, đf vị trí liên kết đôi và đồng phân hình học
- Có 1 liên kết ba, mạch hở
- Có đồng phân mạch cacbon và đồng phân vị trí liên kết ba.
- Có 2 liên kết đôi, mạch hở
- Có vòng benzen
- Có đồng phân vị trí tương đối của nhánh ankyl
Tính chất hoá học - Phản ứng thế halogen.
- Phản ứng tách hiđro.
- Không làm mất màu dung dịch KMnO4 - Phản ứng cộng.
- Phản ứng trùng hợp.
- Tác dụng với chất oxi hoá. - Phản ứng cộng.
- Phản ứng thế H ở cacbon đầu mạch có liên kết ba.
- Tác dụng với chất oxi hoá. - Phản ứng cộng.
- Phản ứng trùng hợp.
- Tác dụng với chất oxi hoá. - Phản ứng thế (halogen, nitro).
- Phản ứng cộng.
VI – ANCOL - PHENOL
ANCOL NO, ĐƠN CHỨC,
MẠCH HỞ PHENOL
Công thức chung CnH2n+1OH (n ≥ 1) C6H5OH
Tính chất hoá học
- Phản ứng với kim loại kiềm.
- Phản ứng thế nhóm OH
- Phản ứng tách nước.
- Phản ứng oxi hoá không hoàn toàn.
- Phản ứng cháy. - Phản ứng với kim loại kiềm.
- Phản ứng với dung dịch kiềm.
- Phản ứng thế nguyên tử H của vòng benzen.
Điều chế Từ dẫn xuất halogen hoặc anken. Từ benzen hay cumen.
VII – ANĐEHIT – AXIT CACBOXYLIC
ANĐEHIT NO, ĐƠN CHỨC, MẠCH HỞ AXIT CACBOXYLIC NO, ĐƠN CHỨC, MẠCH HỞ
CTCT CnH2n+1−CHO (n ≥ 0) CnH2n+1−COOH (n ≥ 0)
Tính chất hoá học - Tính oxi hoá
- Tính khử - Có tính chất chung của axit (tác dụng với bazơ, oxit bazơ, kim loại hoạt động)
- Tác dụng với ancol
Điều chế - Oxi hoá ancol bậc I
- Oxi hoá etilen để điều chế anđehit axetic - Oxi hoá anđehit
- Oxi hoá cắt mạch cacbon.
- Sản xuất CH3COOH
+ Lên men giấm.
+ Từ CH3OH.
C. HOẠT ĐỘNG LUYỆN TẬP
a. Mục tiêu: Củng cố, luyện tập kiến thức vừa học.
b. Nội dung: Dạy học trên lớp, hoạt động nhóm, hoạt động cá nhân.
c. Sản phẩm: HS vận dụng các kiến thức vào giải quyết các bài tập
d. Tổ chức thực hiện:
D. HOẠT ĐỘNG VẬN DỤNG
a) Mục tiêu: Luyện tập, vận dụng các kiến thức giải quyết các vấn đề thực tiễn.
b. Nội dung: Dạy học trên lớp, hoạt động nhóm, hoạt động cá nhân.
c. Sản phẩm: Bài làm của học sinh, kĩ năng tính toán hóa học
d. Tổ chức thực hiện:
- Giáo viên cho hs tự trao đổi các câu hỏi về nội dung bài học liên quan đến thực tiễn xung quanh hs. ( Ghi lại những câu hay của hs để tích lũy)
* HƯỚNG DẪN VỀ NHÀ
Hướng dẫn HS tìm hiểu thêm các nội dung liên quan đến bài học. HD học sinh tự học, tự tìm hiểu về bài cũ và bài mới, đưa ra các câu hỏi mở rộng cho học sinh tham khảo