Với giải Hoạt động 1 trang 99 Hóa học lớp 11 Kết nối tri thức chi tiết trong Bài 16: Hydrocarbon không no giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 11 Bài 16: Hydrocarbon không no
Hoạt động 1 trang 99 Hóa học 11: Điều chế và thử tính chất hoá học của ethylene
Chuẩn bị: cồn 96o, dung dịch sulfuric acid đặc, đá bọt; bình cầu có nhánh 250 mL, ống nghiệm (1) chứa khoảng 2 mL dung dịch KMnO4 loãng, ống nghiệm (2) chứa khoảng 2 mL nước Br2 loãng, ống dẫn thuỷ tinh hình chữ L, ống dẫn thuỷ tinh đầu vuốt nhọn, giá để ống nghiệm, nguồn nhiệt, que đóm, lưới tản nhiệt, bình thuỷ tinh chứa dung dịch NaOH.
Tiến hành:
- Cho vài viên đá bọt, 20 mL cồn 96° vào bình cầu. Rót 40 mL dung dịch H2SO4 đặc vào ống đong, sau đó rót từ từ H2SO4 đặc từ ống đong qua phễu vào bình cầu để tránh sự toả nhiệt quá mạnh.
- Lắp bộ dụng cụ như Hình 16.5.
- Đun nóng đến khi ethylene sinh ra và sục ngay vào các ống nghiệm (1) và (2).
- Thay ống dẫn khí thuỷ tinh hình chữ L bằng ống dẫn thuỷ tinh có đầu vuốt nhọn.
Dùng que đóm đang cháy để đốt ethylene ở đầu ống dẫn khí.
Lưu ý: Dung dịch sulfuric acid đặc rơi vào da sẽ gây bỏng nặng, cần cẩn thận khi sử dụng.
Hãy giải thích hiện tượng và viết phương trình hoá học của phản ứng xảy ra.
Lời giải:
Đun cồn 96o với sulfuric acid đặc sinh ra khí ethylene (có lẫn tạp chất như CO2, SO2…).
Khí sinh ra được dẫn qua bình (1) để loại tạp chất; dẫn tiếp qua bình (2) thấy dung dịch Br2 (hoặc dung dịch KMnO4) nhạt dần đến mất màu do liên kết pi ở liên kết đôi của ethylene kém bền vững.
Đốt ethylene ở đầu ống dẫn khí, khí ethylene cháy và toả nhiều nhiệt.
Phương trình hoá học:
C2H5OH CH2 = CH2 + H2O
CH2 = CH2 + Br2 → CH2Br – CH2Br
3CH2 = CH2 + 2KMnO4 + 4H2O → 3HO – CH2 – CH2 – OH + 2MnO2 + 2KOH
C2H4 + 3O2 2CO2 + 2H2O.
Lý thuyết Tính chất hoá học của alkene, alkyne
a. Phản ứng cộng
* Phản ứng cộng hydrogen
Hydrogen hóa alkyne, tuỳ vào điều kiện áp suất, nhiệt độ và xúc tác, có thể nhận được sản phẩm là alkene, alkane.
* Phản ứng cộng halogen
Khi cho alkene hoặc alkyne phản ứng với dung dịch bromine, dung dịch sẽ bị mất màu.
* Phản ứng cộng nước (hydrate hoá)
Phản ứng cộng nước vào alkene hay còn gọi là Hydrate hóa alkene tạo ra từ alcohol, Phản ứng thường sử dụng xúc tác phosphoric acid hoặc sulfuric acid.
CH2 = CH2 + H2O → CH3-CH2OH (điều kiện to, H3PO4)
b. Phản ứng trùng hợp của alkene
Phản ứng trùng hợp alkene là quá trình cộng hợp liên tiếp nhiều phân tử alkene giống nhau hoặc tương tự nhau (gọi là monomer) tạo thành phân tử có phân tử khối lớn (gọi là polymer).
c. Phản ứng của alk-1-yne với AgNO3, trong NH3
Các alkyne có liên kết ba ở đầu mạch (alk-1-yne) có khả năng tham gia phản ứng với dung dịch AgNO3, trong NH, tạo thành kết tủa.
d. Phản ứng oxi hóa
* Phản ứng oxi hoá không hoàn toàn
Các alkene và alkyne có khả năng làm mất màu dung dịch thuốc tím, đây là phản ứng ox hóa không hoàn toàn.
* Phản ứng cháy
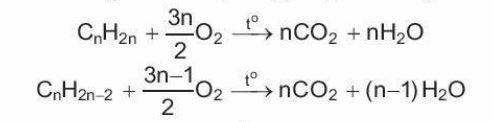
Alkene và alkyne đều dễ cháy khi có mặt oxygen, phản ứng toả nhiều nhiệt:
Xem thêm lời giải bài tập Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác:
Hoạt động 1 trang 93 Hóa học 11: Điều kiện để có đồng phân hình học của alkene 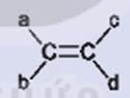
Hoạt động 2 trang 93 Hóa học 11: Alkene 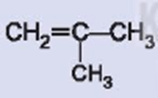
Câu hỏi 2 trang 94 Hóa học 11: Trong các chất sau, chất nào có đồng phân hình học?…
Câu hỏi 3 trang 98 Hóa học 11: Viết phương trình hoá học của các phản ứng:…
Hoạt động 1 trang 99 Hóa học 11: Điều chế và thử tính chất hoá học của ethylene…
Hoạt động 2 trang 99 Hóa học 11: Điều chế và thử tính chất hoá học của acetylene…
Câu hỏi 6 trang 100 Hóa học 11: Viết phương trình hoá học của các phản ứng:…
Xem thêm các bài giải SGK Hóa lớp 11 Kết nối tri thức hay, chi tiết khác: