Với lời giải SBT Hóa học 11 trang 21 chi tiết trong Bài 5: Ammonia. Muối ammonium sách Kết nối tri thức giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 5: Ammonia. Muối ammonium
Bài 5.19 trang 21 Sách bài tập Hóa học 11: Hỗn hợp gồm N2 và H2 có tỉ lệ mol tương ứng là 1 : 4. Nung nóng X trong bình kín ở nhiệt độ khoảng 450oC có bột Fe xúc tác, thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 4. Hiệu suất của phản ứng tổng hợp NH3 là
A. 20%.
B. 25%.
C. 30%.
D. 10%.
Lời giải:
Đáp án đúng là: B
Giả sử có 1 mol N2 và 4 mol H2.
Phương trình hoá học: N2 + 3H2 ⇌ 2NH3
Ban đầu: 1 4 0 mol
Phản ứng: x 3x 2x mol
Sau phản ứng: (1 – x) (4 – 3x) 2x mol
Tổng số mol khí sau phản ứng: nsau = (1 – x) + (4 – 3x) + 2x = 5 – 2x (mol).
Áp dụng định luật bảo toàn khối lượng có:
mtrước = msau ⇔ 28.1 + 2.4 = (5 – 2x).4.2 Þ x = 0,25.
Giả sử H = 100% thì N2 hết, do đó hiệu xuất phản ứng tính theo N2.
Ta có: H = = 25%.
Bài 5.20 trang 21 Sách bài tập Hóa học 11: Hỗn hợp khí X gồm N2 và H2 có tỉ khối đối với H2 bằng 3,6. Nung nóng X trong bình kín có bột Fe xúc tác, thu được hỗn hợp khí Y có số mol giảm 8% so với ban đầu. Hiệu suất của phản ứng tổng hợp NH3 là
A. 25%.
B. 23%.
C. 16%.
D. 20%.
Lời giải:
Đáp án đúng là: D
Giả sử ban đầu có x mol N2 và y mol H2.
Ta có:
Giả sử có 1 mol N2 và 4 mol H2. Vậy số mol ban đầu là 5 mol.
Phương trình hoá học: N2 + 3H2 ⇌ 2NH3
Ban đầu: 1 4 0 mol
Phản ứng: x 3x 2x mol
Sau phản ứng: (1 – x) (4 – 3x) 2x mol
Tổng số mol khí sau phản ứng: nsau = (1 – x) + (4 – 3x) + 2x = 5 – 2x (mol).
Số mol Y giảm 8% so với ban đầu
Giả sử H = 100% thì N2 hết, do đó hiệu xuất phản ứng tính theo N2.
Ta có: H = = 20%.
Bài 5.21 trang 21 Sách bài tập Hóa học 11: a) Viết phương trình hoá học xảy ra khi cho dung dịch (NH4)2CO3 lần lượt tác dụng với lượng dư các dung dịch: HCl, Ba(OH)2.
b) Trình bày phương pháp hoá học phân biệt ba dung dịch: NH4NO3, KNO3, NH4Cl.
Lời giải:
a) Các phản ứng xảy ra:
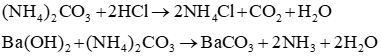
b) Sử dụng lần lượt hai dung dịch thuốc thử là NaOH và AgNO3
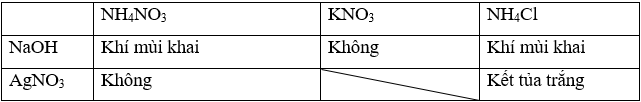
Các phương trình hóa học:
Bài 5.22 trang 21 Sách bài tập Hóa học 11: Sự phụ thuộc của độ tan khí ammonia trong nước vào nhiệt độ được mô tả ở hình bên.
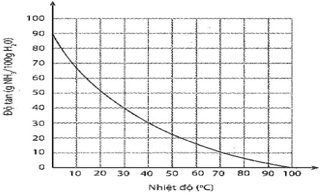
Sự phụ thuộc của độ tan khi ammonia vào nhiệt độ
Dựa vào đồ thị ở hình bên, hãy xác định:
a) Độ tan của ammonia ở 30oC. Nhận xét về tính tan của ammonia ở nhiệt độ này.
b) Nồng độ phần trăm của dung dịch ammonia bão hoà ở 30oC.
c) Độ tan của ammonia ở 60oC. So sánh với độ tan của ammonia ở 30oC. Giải thích.
Lời giải:
a) Ở 30 °C, độ tan của ammonia là 40 g NH3/100g nước. Nhận xét: Ở nhiệt độ này, ammonia tan tốt trong nước.
b) Nồng độ phần trăm của ammonia bão hoà:
c) Độ tan của ammonia ở 60 °C là 15 g /100 g nước.
Nhận xét: Độ tan của ammonia ở 60 °C đã giảm mạnh so với ở 30 °C.
Giải thích: Ở nhiệt độ cao hơn, các phân tử ammonia chuyển động nhiệt mạnh hơn, thoát khỏi dung dịch nhiều hơn, dẫn đến độ tan giảm.
Bài 5.23 trang 21 Sách bài tập Hóa học 11: Trong công nghiệp, nitrogen được sản xuất từ nguồn nguyên liệu dồi dào là không khí. Giả thiết không khí chứa 78% N2, 21% O2 và 1% Ar về thể tích. Cho biết nhiệt độ sôi của các chất trên lần lượt là -196oC, -183oC và -186oC. Em hãy nêu nguyên tắc sản xuất N2 từ không khí.
Lời giải:
Nguyên tắc sản xuất nitrogen từ không khí là chưng cất phân đoạn không khí lỏng. Đầu tiên sẽ hoá lỏng không khí bằng cách tăng áp suất và làm lạnh xuống dưới –196 °C. Sau đó, tăng dần nhiệt độ, đến –196 °C thì nitrogen sôi và thoát ra; –186 °C thì argon sôi và thoát ra; chất lỏng còn lại là oxygen.
Bài 5.24 trang 21 Sách bài tập Hóa học 11: Xét cân bằng của dung dịch NH3 0,1 M 25oC:
Bỏ qua sự phân li của nước. Xác định giá trị pH của dung dịch trên.
Lời giải:
Kc
Ban đầu: 0,1 (mol/L)
Cân bằng: 0,1 - x x x (mol/L)
Bài 5.25 trang 21 Sách bài tập Hóa học 11: Xét cân bằng trong dung dịch gồm NH4Cl 0,1 M và NH3 0,05 M ở 25oC:
Bỏ qua sự phân li của nước. Xác định giá trị pH của dung dịch trên.
Lời giải:
Ban đầu: 0,05 0,10 (mol/L)
Cân bằng: 0,05 - x 0,10 + x x (mol/L)
Xem thêm lời giải Sách bài tập Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 5.1 trang 18 Sách bài tập Hóa học 11: Ở trạng thái lỏng nguyên chất, phân tử chất nào sau đây tạo được liên kết hydrogen với nhau?...
Bài 5.2 trang 18 Sách bài tập Hóa học 11: Khí nào sau đây dễ tan trong nước do tạo được liên kết hydrogen với nước?...
Bài 5.3 trang 18 Sách bài tập Hóa học 11: Nhận định nào sau đây về phân tử ammonia không đúng?...
Bài 5.4 trang 18 Sách bài tập Hóa học 11: Khi tác dụng với nước và hydrochloric acid, ammonia đóng vai trò là....
Bài 5.5 trang 19 Sách bài tập Hóa học 11: Trong phương pháp Ostwald, ammonia bị oxi hoá bởi oxygen không khí tạo thành sản phẩm chính là...
Bài 5.6 trang 19 Sách bài tập Hóa học 11: Cho dung dịch NH3 vào dung dịch chất nào sau đây thu được kết tủa trắng?....
Bài 5.7 trang 19 Sách bài tập Hóa học 11: Cho vài giọt dung dịch phenolphthalein vào dung dịch NH3, phenolphthalein chuyển sang màu nào sau đây?....
Bài 5.8 trang 19 Sách bài tập Hóa học 11: Nhiệt phân hoàn toàn muối nào sau đây thu được sản phẩm chỉ gồm khí và hơi?...
Bài 5.9 trang 19 Sách bài tập Hóa học 11: Phân biệt được đung dịch NH4Cl và NaCl bằng thuốc thử là dung dịch....
Bài 5.10 trang 19 Sách bài tập Hóa học 11: Trong nước, phân tử/ion nào sau đây thể hiện vai trò là acid Bronsted?....
Bài 5.11 trang 19 Sách bài tập Hóa học 11: Cho các nhận định sau: Phân tử ammonia và ion ammonium đều: (1) chứa liên kết cộng hoá trị; (2) là base Brønsted trong nước; (3) là acid Brønsted trong nước; (4) chứa nguyên tử N có số oxi hoá là -3.....
Bài 5.12 trang 19 Sách bài tập Hóa học 11: Các chất khí được thu vào bình theo đúng nguyên tắc bằng cách đầy không khí (X, Y, Z) và đẩy nước (T) như sau..
Bài 5.13 trang 20 Sách bài tập Hóa học 11: Phát biểu nào sau đây không đúng?.....
Bài 5.14 trang 20 Sách bài tập Hóa học 11: Tiến hành thí nghiệm trộn từng dung dịch sau: (a) NH3 và AlCl3; (b) (NH4)2SO4 và Ba(OH)2; (c) NH4Cl và AgNO3; (d) NH3 và HCl. Sau khi phản ứng kết thúc, số thí nghiệm thu được kết tủa là....
Bài 5.15 trang 20 Sách bài tập Hóa học 11: Xét cân bằng hoá học:...
Bài 5.16 trang 20 Sách bài tập Hóa học 11: Xét cân bằng hoá học:...
Bài 5.17 trang 20 Sách bài tập Hóa học 11: Xét cân bằng hoá học:....
Bài 5.18 trang 20 Sách bài tập Hóa học 11: Xét cân bằng hoá học:.....
Bài 5.19 trang 21 Sách bài tập Hóa học 11: Hỗn hợp gồm N2 và H2 có tỉ lệ mol tương ứng là 1 : 4. Nung nóng X trong bình kín ở nhiệt độ khoảng 450oC có bột Fe xúc tác, thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 4. Hiệu suất của phản ứng tổng hợp NH3 là...
Bài 5.20 trang 21 Sách bài tập Hóa học 11: Hỗn hợp khí X gồm N2 và H2 có tỉ khối đối với H2 bằng 3,6. Nung nóng X trong bình kín có bột Fe xúc tác, thu được hỗn hợp khí Y có số mol giảm 8% so với ban đầu. Hiệu suất của phản ứng tổng hợp NH3 là....
Bài 5.21 trang 21 Sách bài tập Hóa học 11: a) Viết phương trình hoá học xảy ra khi cho dung dịch (NH4)2CO3 lần lượt tác dụng với lượng dư các dung dịch: HCl, Ba(OH)2......
Bài 5.22 trang 21 Sách bài tập Hóa học 11: Sự phụ thuộc của độ tan khí ammonia trong nước vào nhiệt độ được mô tả ở hình bên....
Bài 5.23 trang 21 Sách bài tập Hóa học 11: Trong công nghiệp, nitrogen được sản xuất từ nguồn nguyên liệu dồi dào là không khí. Giả thiết không khí chứa 78% N2, 21% O2 và 1% Ar về thể tích. Cho biết nhiệt độ sôi của các chất trên lần lượt là -196oC, -183oC và -186oC. Em hãy nêu nguyên tắc sản xuất N2 từ không khí....
Bài 5.24 trang 21 Sách bài tập Hóa học 11: Xét cân bằng của dung dịch NH3 0,1 M 25oC:....
Bài 5.25 trang 21 Sách bài tập Hóa học 11: Xét cân bằng trong dung dịch gồm NH4Cl 0,1 M và NH3 0,05 M ở 25oC:....
Bài 5.26 trang 22 Sách bài tập Hóa học 11: Tại một nhà máy phân bón, ammophos được sản xuất từ ammonia và phosphoric acid, thu được NH4H2PO4 và (NH4)2HPO4 tỉ lệ mol là 1:1.....
Xem thêm các bài giải SBT Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 4: Nitrogen
Bài 5: Ammonia. Muối ammonium
Bài 6: Một số hợp chất của nitrogen với oxygen
Bài 7: Sulfur và sulfur dioxide
Bài 8: Sulfuric acid và muối sulfate
Bài 9: Ôn tập chương 2