Với giải Bài 3.8 trang 17 SBT Hóa Học lớp 11 Chân trời sáng tạo chi tiết trong Bài 3: Đơn chất nitrogen giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa Học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 3: Đơn chất nitrogen
Bài 3.8 trang 17 SBT Hóa học 11: Tại sao ở điều kiện thường (25 °C, 1 bar), nitrogen tồn tại ở dạng phân tử N2 trong khi đó phosphorus lại tồn tại ở dạng P4 mà không xảy ra trường hợp ngược lại? Biết:
– Năng lượng liên kết ba N≡N là 941 kJ/mol.
– Năng lượng liên kết ba P≡P là 490 kJ/mol.
– Năng lượng liên kết đơn N-N là 160 kJ/mol.
– Năng lượng liên kết đơn P-P là 209 kJ/mol.
Lời giải:
+ Xét 4 nguyên tử P tạo thành:
- Phân tử P4 gồm 4 nguyên tử P liên kết với nhau bằng 6 liên kết đơn P-P.
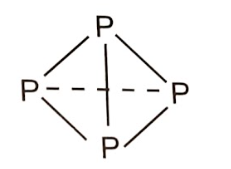
Năng lượng được giải phóng khi tạo một phân tử P4: 6 × 209 = 1254 (kJ).
- Phân tử P2 gồm 2 phân tử P≡P. Năng lượng được giải phóng khi tạo hai phân tử P2: 2 × 490 = 980 (kJ).
→ Phân tử P4 bền hơn P2 nên ở điều kiện thường, phosphorus trắng tồn tại ở dạng phân tử P4.
+ Xét 4 nguyên tử N tạo thành:
- Phân tử N4 gồm 4 nguyên tử N liên kết với nhau bằng 6 liên kết đơn N-N. Năng lượng được giải phóng khi tạo một phân tử N4: 6×160 = 960 (kJ).
- Phân tử N2 gồm 2 phân tử N≡N. Năng lượng được giải phóng khi tạo hai phân tử N2: 2 × 941 = 1882 (kJ).
=> Phân tử N2 bền hơn N4 ở điều kiện thường.
Xem thêm lời giải Sách bài tập Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Bài 3.1 trang 16 SBT Hóa học 11: Ở trạng thái tự nhiên, nitrogen...
Bài 3.2 trang 16 SBT Hóa học 11: Cấu hình electron nguyên tử của nitrogen là...
Bài 3.3 trang 16 SBT Hóa học 11: Tính chất nào sau đây của nitrogen không đúng?...
Bài 3.4 trang 16 SBT Hóa học 11: Nitrogen trong không khí có vai trò nào sau đây?...
Xem thêm các bài giải SBT Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Bài 4: Ammonia và một số hợp chất ammonium