Với giải sách bài tập Khoa học tự nhiên 8 Bài 8: Acid hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Khoa học tự nhiên 8. Mời các bạn đón xem:
Giải SBT Khoa học tự nhiên 8 Bài 8: Acid
Lời giải:
Công thức hoá học của các chất:
Sulfuric acid: H2SO4;
Hydrochloric acid: HCl;
Acetic acid: CH3COOH;
Carbonic acid: H2CO3.
Bài 8.2 trang 26 Sách bài tập KHTN 8: Dung dịch/chất lỏng nào sau đây làm đổi màu quỳ tím thành đỏ?
A. Nước đường. B. Nước cất.
C. Giấm ăn. D. Nước muối sinh lí.
Lời giải:
Đáp án đúng là: C
Thành phần của giấm ăn chứa acetic acid với nồng độ 2 – 5% làm quỳ tím chuyển sang màu đỏ.
Bài 8.3 trang 26 Sách bài tập KHTN 8: Dung dịch nào sau đây không làm đổi màu quỳ tím thành đỏ?
A. Nước muối. B. Giấm ăn.
C. Nước chanh. D. Nước ép quả khế.
Lời giải:
Đáp án đúng là: A
Dung dịch nước muối không làm đổi màu quỳ tím thành đỏ.
Các dung dịch giấm ăn, nước chanh, nước ép quả khế có tính acid làm quỳ tím chuyển sang màu đỏ.
A. HNO3, H2O, H3PO4. B. CH3COOH, HCl, HNO3.
C. HBr, H2SO4, H2O. D. HCl, NaCl, KCl.
Lời giải:
Đáp án đúng là: B
Các dung dịch CH3COOH; HCl; HNO3 là các dung dịch acid làm quỳ tím chuyển sang màu đỏ.
Bài 8.5 trang 26 Sách bài tập KHTN 8: Chất nào sau đây không phản ứng với sắt?
A. NaCl. B. CH3COOH. C. H2SO4. D. HCl.
Lời giải:
Đáp án đúng là: A
NaCl + Fe: không phản ứng;
2CH3COOH + Fe → (CH3COO)2Fe + H2
H2SO4 + Fe → FeSO4 + H2
2HCl + Fe → FeCl2 + H2.
Lời giải:
|
Acid |
H2S |
HCl |
HNO3 |
H2SO4 |
CH3COOH |
|
Gốc acid |
S2- |
Cl- |
NO3- |
SO42- |
CH3COO- |
|
Hoá trị của gốc acid |
II |
I |
I |
II |
I |
Lời giải:
Thí nghiệm chứng minh:
Khi cho hydrochloric acid phản ứng với kim loại như Mg, Zn, Fe,... sinh ra khí hydrogen.
2HCl + Fe → FeCl2 + H2
Lời giải:
Cho hai kim loại vào dung dịch HCl (hoặc H2SO4 loãng).
Kim loại nào phản ứng, thấy có khí thoát ra là nhôm (aluminium):
6HCl + 2Al → 2AlCl3 + 3H2
Còn lại là bạc (silver) không phản ứng với acid HCl (hoặc H2SO4 loãng).
Lời giải:
Cho hai mẫu vật liệu vào dung dịch acid như HCl (hoặc H2SO4 loãng).
Vật liệu nào phản ứng, thấy có khí thoát ra là sắt:
2HCl + Fe → FeCl2 + H2
Còn lại là nhựa không phản ứng với acid.
Bài 8.10 trang 27 Sách bài tập KHTN 8: Hoàn thành các phản ứng sau đây và cân bằng PTHH:
a) Mg + H2SO4 → c) Zn + HCl →
b) Fe + HCl → d) Mg + CH3COOH →
Lời giải:
a) Mg + H2SO4 → MgSO4 + H2
b) Fe + 2HCl → FeCl2 + H2
c) Zn + 2HCl → ZnCl2 + H2
d) Mg + 2CH3COOH → Mg(CH3COO)2 + H2
a) Viết PTHH của phản ứng xảy ra.
b) Tính thể tích khí thoát ra (ở 25 °C, 1 bar).
c) Tính nồng độ MgCl2 trong dung dịch thu được. Coi thể tích dung dịch không đổi sau phản ứng.
Lời giải:
a) Phương trình hoá học:
Mg + 2HCl → MgCl2 + H2
b)
Ta có: nên sau phản ứng HCl hết, Mg dư.
Số mol sản phẩm sinh ra tính theo HCl.
Mg + 2HCl → MgCl2 + H2
0,1 → 0,05 0,05 mol
Thể tích khí thoát ra (ở 25 °C, 1 bar): 0,05.24,79 = 1,2395 (L)
c) Nồng độ MgCl2 trong dung dịch thu được:
Coi thể tích dung dịch không đổi sau phản ứng.
a) Viết PTHH của phản ứng xảy ra.
b) Tính phần trăm về khối lượng mỗi kim loại trong hợp kim.
Lời giải:
a) Đồng (copper) không phản ứng với H2SO4 loãng.
Phương trình hoá học xảy ra:
Fe + H2SO4 → FeSO4 + H2.
b) Chất rắn không tan sau phản ứng là đồng (Cu).
a) Viết PTHH của phản ứng xảy ra.
b) Tính phần trăm về khối lượng mỗi kim loại trong hỗn hợp đầu.
Lời giải:
a) Phản ứng xảy ra:
2Al + 6HCl→ 2AlCl3+ 3H2
Fe + 2HCl→ FeCl2 + H2
b) Đặt số mol Al và Fe lần lượt là x và y.
Ta có: 2Al + 6HCl→ 2AlCl3+ 3H2
Số mol: xxmol
Fe + 2HCl → FeCl2 + H2
Số mol: yymol
Tổng khối lượng kim loại: 27x + 56y = 5,5(1)
Tổng khối lượng muối: 133,5x + 127y = 19,7(2)
Để tính x và y ta dùng phương pháp khử. Cách làm như sau:
Nhân cả 2 vế của (1) với 133,5 ta được: 3604,5x + 7476y = 734,25(1')
Nhân cả 2 vế của (2) với 27 ta được:3604,5x + 3429y = 531,9(29
Trừ từng vế của (1') cho (2'), ta được: 4 047y = 202,35. Tính ra y = 0,05.
Thay y = 0,05 vào (1) tính ra x = 0,1.
Vậy:
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Tính thể tích tối thiểu dung dịch HCl 1 M cẩn dùng để phản ứng hết với 4 g gỉ sắt (coi hiệu suất phản ứng là 100%).
Lời giải:
Phương trình hoá học:
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
0,025 → 0,15 mol
Thể tích dung dịch HCl tối thiểu cần dùng là:
= 0,15(L).
a) Viết PTHH của phản ứng xảy ra.
b) Tính khối lượng dung dịch H2SO4 cần dùng.
c) Tính nồng độ C% của dung dịch ZnSO4 thu được sau phản ứng.
Lời giải:
a) Phương trình hoá học:
Zn + H2SO4 → ZnSO4 + H2
b) Số mol H2 cần điều chế:
Zn + H2SO4 → ZnSO4 + H2
Theo PTHH: 1 1 mol
Phản ứng: 0,1 ← 0,1 mol
Vậy khối lượng H2SO4 có trong dung dịch: 0,1.98 = 9,8 gam.
Khối lượng dung dịch H2SO4 9,8% cần dùng là:
= 100gam.
c) Khối lượng dung dịch sau phản ứng:
= 100 + 65.0,1-2.0,1 = 106,3gam.
Khôí lượng ZnSO4 có trong dung dịch sau phản ứng: mct = 0,1.161 = 16,1 gam.
Nồng độ phần trăm của dung dịch ZnSO4 thu được sau phản ứng là:
Lời giải:
Có thể dùng giấm ăn (là dung dịch của CH3COOH) để làm sạch cặn. Do xảy ra phản ứng hoá học:
2CH3COOH + CaCO3 → (CH3COO)2Ca + H2O + CO2
CaCO3 bị tan trong giấm nên sẽ bị loại bỏ.
b) Hãy giải thích tại sao mưa acid gây phá huỷ nghiêm trọng các công trình xây dựng.
Lời giải:
a) Đều thấy có phản ứng xảy ra, hiện tượng sủi bọt khí: đá vôi tạo bọt khí CO2, còn sắt và nhôm tạo bọt khí H2.
b) Các công trình xây dựng hầu hết đều làm từ các vật liệu đá vôi, sắt, nhôm. Do đó, mưa acid sẽ phản ứng với các vật liệu này, phá huỷ công trình xây dựng.
a) Nêu một phương pháp hoá học để phân biệt sữa chua và sữa tươi.
b) Hãy giải thích tại sao sữa chua thường được đựng trong các hộp nhựa hoặc hộp giấy chứ không đựng trong hộp kim loại.
Lời giải:
a) Dùng quỳ tím để phân biệt sữa chua và sữa tươi: sữa chua làm quỳ tím đổi thành màu đỏ.
b) Sữa chua không được đựng trong hộp kim loại vì acid trong sữa chua phản ứng được với kim loại, gây hoà tan hộp đựng và có thể gây ngộ độc kim loại khi uống sữa.
Xem thêm các bài giải SBT Khoa học tự nhiên 8 Kết nối tri thức hay, chi tiết khác:
Bài 7: Tốc độ phản ứng và chất xúc tác
Lý thuyết KHTN 8 Bài 8: Acid
I. Khái niệm Acid
- Acid ban đầu được biết đến là những chất có vị chua như acetic acid có trong giấm ăn, citric acid có trong quả chanh, malic acid có trong quả táo.
-Từ acid xuất phát từ tiếng Latin là acidus – nghĩa là vị chua.
- Khái niệm về acid được phát biểu như sau: Acid là những hợp chất trong phân tử có nguyên tử hydrogen liên kết với gốc acid. Khi tan trong nước, acid tạo ra ion H+.
- Gốc acid trong các acid sau là: H (Hydrogen), H2SO4 (Sulfuric acid), HCl (Hydrochloric acid), HNO3 (Nitric acid).
- Acid thường tan được trong nước, dung dịch acid làm đổi màu giấy quỳ từ tim sang đồ. Khi dung dịch acid phản ứng với một số kim loại như magnesium, cắt, kẽm... nguyên tử hydrogen của acid được thay thế bằng nguyên tử kim loại để tạo thành muối và giải phóng ra khí hydrogen.
- Tính chất của dung dịch hydrochloric acid:
+ Chuẩn bị: dung dịch HCl 1 M, giấy quỳ tím; hai ống nghiệm mỗi ống đựng một trong các kim loại Fe, Zn, ông hút nhỏ giọt.
+ Thực hiện: Nhỏ 1 – 2 giọt dung dịch HCl vào máu giấy quỳ tím. Cho khoảng 3 mL dung dịch HCl vào mỗi ống nghiệm đã chuẩn bị ở trên.
+ Mô tả hiện tượng xảy ra và viết phương trình hoá học
+ Phản ứng giữa dung dịch HCl và kim loại Mg: Mg + 2HCl → MgCl2 + H2.
- Sulfuric acid (H2SO4) là chất lỏng không màu, không bay hơi, snh như dầu ăn, nặng gần gấp hai lần nước. Sulfuric acid tan vô hạn trong nước và toả rất nhiều nhiệt.
- Lưu ý: Tuyệt đối không tự ý pha loãng dung dịch sulfuric acid đặc.
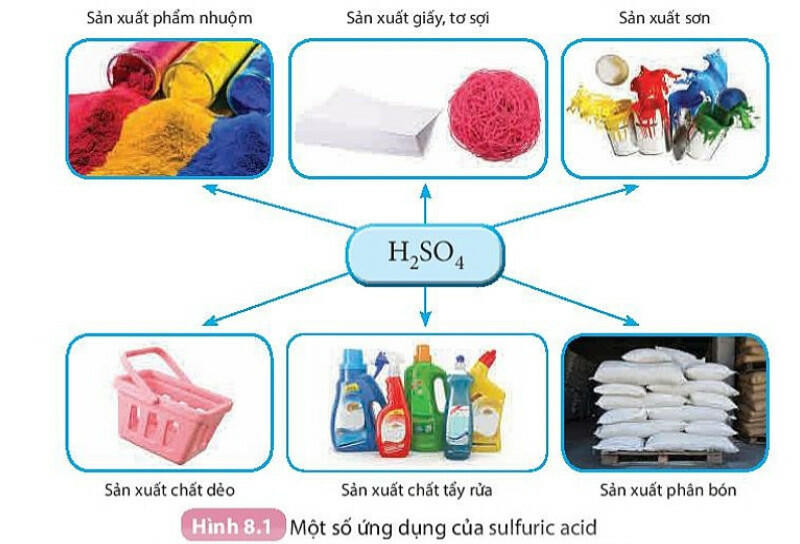
- Sulfuric acid là một trong các hoá chất được sử dụng nhiều trong các ngành công nghiệp (Hình 8.1) và là hoá chất được tiêu thụ nhiều nhất trên thế giới.
- Dung dịch hydrochloric acid (HCl) là chất lỏng không màu.
- Hydrochloric acid được sử dụng nhiều trong các ngành công nghiệp (Hình 8.2)

- Acetic acid (CH3COOH) là chất lỏng không màu, có vị chua. Trong giấm ăn có chứa acetic acid với nồng độ 2 – 5%.