Khi một phản ứng thuận nghịch đạt đến trạng thái cân bằng thì hệ các chất phản ứng
A. không xảy ra biến đổi hoá học nào nữa.
B. vẫn tiếp tục diễn ra các biến đổi hoá học.
C. chỉ phản ứng theo chiều thuận.
D. chỉ phản ứng theo chiều nghịch.
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án B
Khi một phản ứng thuận nghịch đạt đến trạng thái cân bằng thì hệ các chất phản ứng vẫn tiếp tục diễn ra các biến đổi hoá học.
Lý thuyết Mở đầu về cân bằng hoá học
I. Khái niệm phản ứng thuận nghịch và trạng thái cân bằng
- Phản ứng thuận nghịch là phản ứng trong đó ở cùng điều kiện, xảy ra đồng thời sựu chuyển chất phản ứng thành chất sản phẩm và sự chuyển chất sản phẩm thành chất phản ứng.
- Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái mà tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
II. Biểu thức hằng số cân bằng và ý nghĩa
1. Biểu thức hằng số cân bằng
- Xét phản ứng thuận nghịch tổng quát: aA + bB cC + dD.
Ở trạng thái cân bằng, hằng số cân bằng (KC) được xác định theo biểu thức:
Trong đó:
+ [A], [B], [C], [D] là nồng độ mol của các chất A, B, C, D ở trạng thái cân bằng.
+ a, b, c, d là hệ số tỉ lượng của các chất trong phương trình hóa học của phản ứng.
- Ví dụ: Xét phản ứng: C(s) + CO2(g) 2CO(g)
2. Ý nghĩa của biểu thức hằng số cân bằng
- Hằng số cân bằng KC phụ thuộc vào bản chất của phản ứng và nhiệt độ.
- KC càng lớn thì phản ứng thuận càng chiếm ưu thế và ngược lại.
III. Ảnh hưởng của nhiệt độ, nồng độ và áp suất đến cân bằng hóa học
1. Ảnh hưởng của nhiệt độ tới cân bằng hóa học
- Khi nhiệt độ tăng, cân bằng chuyển dịch theo chiều làm giảm nhiệt độ, tức là chiều phản ứng thu nhiệt, nghĩa là chiều làm giảm tác động của tăng nhiệt độ và ngược lại.
2. Nguyên lí chuyển dịch cân bằng Le Chatelier
- Khi tăng nồng độ một chất trong phản ứng thì cân bằng hóa học bị phá vỡ và chuyển dịch theo chiều làm giảm nồng độ của chất đó và ngược lại.
- Khi tăng áp suất chung của hệ, thì cân bằng chuyển dịch theo chiều làm giảm áp suất, tức là chiều làm giảm số mol khí và ngược lại.
- Nguyên lí chuyển dịch cân bằng Le Chatelier: Một phản ứng thuận nghịch đang ở trạng thái cân bằng, khi chịu một tác động bên ngoài như biến đổi nồng độ, nhiệt độ, áp suất thì cân bằng sẽ chuyển dịch theo chiều làm giảm tác động bên ngoài đó.
Sơ đồ tư duy Mở đầu về cân bằng hoá học
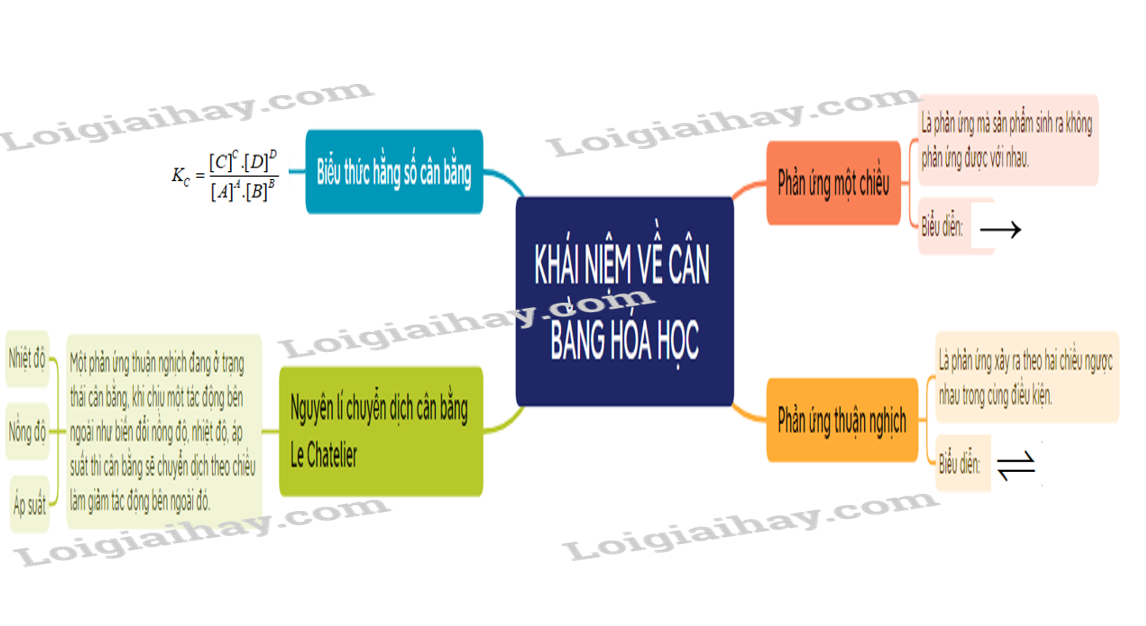
Xem thêm một số kiến thức liên quan:
15 câu Trắc nghiệm Mở đầu về cân bằng hoá học (Cánh diều) có đáp án – Hóa học lớp 11
Lý thuyết Mở đầu về cân bằng hoá học (Cánh diều) hay, chi tiết | Hóa học 11
Nguyên tử vàng có 79 electron ở vỏ nguyên tử. Điện tích hạt nhân của nguyên tử vàng là
Một nguyên tử (X) có 13 proton trong hạt nhân. Khối lượng proton trong hạt nhân nguyên tử X là:
Nguyên tố hóa học cần thiết cho sự phát triển chiều cao của cơ thể người là:
Mối quan hệ giữa tốc độ phản ứng thuận vt và tốc độ phản ứng nghịch vn ở trạng thái cân bằng được biểu diễn như thế nào?
Đối tượng nghiên cứu của hóa học là sự biến đổi chất, hãy lấy 5 ví dụ về sự biến đổi hóa học.
Tính chất của các nguyên tố và đơn chất, cũng như thành phần và tính chất của các hợp chất tạo nên từ các nguyên tố đó
Các nguyên tố thuộc cùng một nhóm A trong bảng tuần hoàn sẽ có cùng
Ngâm hoa quả làm siro thuộc loại phản ứng tách biệt và tinh chế nào?
Cho este có công thức cấu tạo: CH2 = C(CH3)COOCH3. Tên gọi của este đó là
Cho cân bằng sau trong bình kín: 2NO2(màu nâu đỏ)N2O4 (không màu). Biết khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần. Phản ứng thuận có