Các nguyên tố thuộc cùng một nhóm A trong bảng tuần hoàn sẽ có cùng
A. số electron hóa trị.
B. số hiệu nguyên tử.
C. số lớp electron.
D. số khối.
 Giải bởi Vietjack
Giải bởi Vietjack
Đáp án đúng là: A
Các nguyên tố thuộc cùng một nhóm A trong bảng tuần hoàn sẽ có cùng số electron hóa trị.
Cấu tạo của bảng tuần hoàn
1. Ô nguyên tố
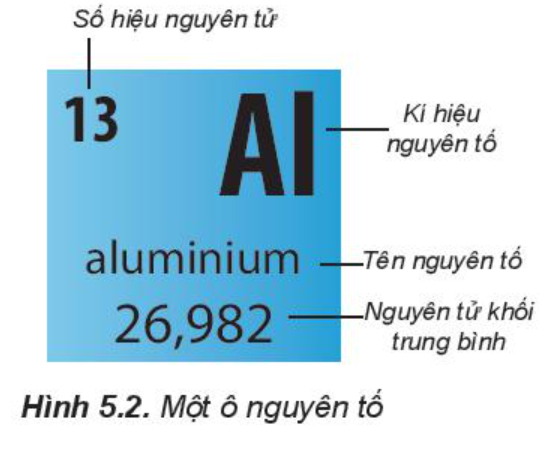
Trong bảng tuần hoàn, mỗi nguyên tố được xếp vào một ô, gọi là ô nguyên tố. Số thứ tự của ô là số hiệu nguyên tử của nguyên tố đó.
Tùy theo từng loại bảng, các thông tin của một ô nguyên tố có thể là số hiệu nguyên tử, kí hiệu nguyên tố, tên nguyên tố, nguyên tử khối trung bình, …
Ví dụ: Nguyên tử nguyên tố sodium có Z = 11. Nguyên tố sodium ở ô 11 trong bảng tuần hoàn.
2. Chu kì
Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được xếp theo chiều điện tích hạt nhân tăng dần.
Bảng tuần hoàn hiện nay có 7 chu kì. Số thứ tự chu kì bằng số lớp electron của nguyên tử các nguyên tố trong chu kì.
Ví dụ: Cấu hình electron của nguyên tử nguyên tố oxygen (Z = 8): 1s22s22p4.
Nguyên tử oxygen có 2 lớp electron.
Số thứ tự chu kì = số lớp electron = 2.
Nguyên tố oxygen thuộc chu kì 2 trong bảng tuần hoàn.
3. Nhóm nguyên tố
Nhóm nguyên tố gồm các nguyên tố mà nguyên tử của chúng có cấu hình electron tương tự nhau, do đó có tính chất hóa học gần giống nhau và được xếp thành một cột.
Bảng tuần toàn hiện nay có 18 cột, chia thành 8 nhóm A (IA đến VIIIA) và 8 nhóm B (IB đến VIIIB). Mỗi nhóm là một cột, riêng nhóm VIIIB gồm 3 cột.
Ví dụ: Nhóm kim loại kiềm – nhóm IA, nhóm halogen – nhóm VIIA.
Nguyên tử các nguyên tố trong cùng một nhóm A có số electron hóa trị bằng nhau và bằng số thứ tự của nhóm (trừ He).
4. Phân loại nguyên tố
a) Theo cấu hình electron
Các nguyên tố s, p, d, f là những nguyên tố mà nguyên tử có electron cuối cùng được điền vào phân lớp s, p, d, f tương ứng.
Ví dụ: 11Na: 1s22s22p63s1 (nguyên tố s).
Các nhóm A: gồm các nguyên tố s và nguyên tố p.
Các nhóm B: gồm các nguyên tố d và nguyên tố f.
b) Theo tính chất hóa học
Các nhóm IA, IIA, IIIA: gồm các nguyên tố s và p là kim loại (trừ H và B).
Các nhóm VA, VIA, VIIA: gồm các nguyên tố p, thường là phi kim.
Nhóm VIIIA: gồm các nguyên tố khí hiếm.
Các nhóm B: gồm các nguyên tố d và f đều là kim loại chuyển tiếp.
Ví dụ: Nguyên tố chlorine có Z = 17. Xác định vị trí của nguyên tố chlorine trong bảng tuần hoàn và cho biết chúng thuộc loại nguyên tố s, p hay d; là kim loại, phi kim hay khí hiếm.
Hướng dẫn giải:
Cấu hình electron của nguyên tử nguyên tố chlorine (Z = 17): 1s22s22p63s23p5.
Số thứ tự ô = số electron = 17.
Số thứ tự chu kì = số lớp electron = 3.
Nguyên tử chlorine có electron cuối cùng điền vào phân lớp p nên chlorine là nguyên tố p và thuộc nhóm A.
Số thứ tự nhóm A = số electron hóa trị = 7 nhóm VIIA.
Vậy, nguyên tố chlorine thuộc ô 17, chu kì 3, nhóm VIIA.
Nguyên tố chlorine thuộc nhóm VIIA Chlorine là nguyên tố phi kim
Xem thêm một số kiến thức liên quan:
Nguyên tử vàng có 79 electron ở vỏ nguyên tử. Điện tích hạt nhân của nguyên tử vàng là
Khi một phản ứng thuận nghịch đạt đến trạng thái cân bằng thì hệ các chất phản ứng
Một nguyên tử (X) có 13 proton trong hạt nhân. Khối lượng proton trong hạt nhân nguyên tử X là:
Nguyên tố hóa học cần thiết cho sự phát triển chiều cao của cơ thể người là:
Mối quan hệ giữa tốc độ phản ứng thuận vt và tốc độ phản ứng nghịch vn ở trạng thái cân bằng được biểu diễn như thế nào?
Đối tượng nghiên cứu của hóa học là sự biến đổi chất, hãy lấy 5 ví dụ về sự biến đổi hóa học.
Tính chất của các nguyên tố và đơn chất, cũng như thành phần và tính chất của các hợp chất tạo nên từ các nguyên tố đó
Ngâm hoa quả làm siro thuộc loại phản ứng tách biệt và tinh chế nào?
Cho este có công thức cấu tạo: CH2 = C(CH3)COOCH3. Tên gọi của este đó là
Cho cân bằng sau trong bình kín: 2NO2(màu nâu đỏ)N2O4 (không màu). Biết khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần. Phản ứng thuận có