Với giải Câu hỏi 2 trang 31 Hóa học lớp 11 Kết nối tri thức chi tiết trong Bài 4: Nitrogen giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 11. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 11 Bài 4: Nitrogen
Câu hỏi 2 trang 31 Hóa học 11: Trong phương trình hoá học của phản ứng tổng hợp ammonia, hãy xác định các nguyên tử có sự thay đổi số oxi hoá và vai trò của nitrogen.
Lời giải:
Phương trình hoá học:
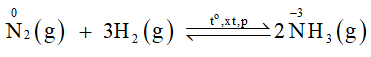
Số oxi hoá của nitrogen giảm từ 0 xuống -3 nên trong phản ứng này đơn chất nitrogen đóng vai trò là chất oxi hoá.
Lý thuyết Tính chất hoá học
Nitrogen khá trơ ở nhiệt độ thường, ở nhiệt độ cao, nitrogen trở nên hoạt động hơn. Nitrogen thể hiện cả tính oxi hoá và tính khử.
a. Tác dụng với hydrogen
Quy trì Ở nhiệt độ cao, áp suất cao và có xúc tác, nitrogen hóa hợp trực tiếp với hydrogen, tạo thành ammonia.
Phản ứng tổng hợp ammonia là quá trình trung gian quan trọng để sản xuất nitric acid, thuốc nổ, đạm nitrate, urea, ammophos....
b. Tác dụng với oxygen
Ở nhiệt độ cao trên 3000°C hoặc có tia lửa điện, nitrogen kết hợp với oxygen, tạo ra nitrogen monoxide (NO)
N2(g) + O2(g) ⇌ 2NO(g) (điều kiện nhiệt độ)
Trong thực tế, phản ứng hoá hợp giữa nitrogen với oxygen thường xảy ra đồng thời với quá trình đốt cháy nhiên liệu ở nhiệt độ cao bằng không khi. Các hoạt động giao thông vận tải và sản xuất công nghiệp là nguyên nhân chính gây phát thải các oxide của nitrogen vào khí quyển.
Xem thêm lời giải bài tập Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác:
Mở đầu trang 29 Hóa học 11: Trong công nghiệp, đơn chất nitrogen kết hợp với hydrogen tạo thành ammonia là một hợp chất quan trọng trong sản xuất phân bón, hoá chất.....
Hoạt động trang 29 Hóa học 11: Nêu ứng dụng thực tiễn của khí nitrogen và diêm tiêu Chile mà em biết.....
Hoạt động 1 trang 30 Hóa học 11: Sắp xếp các hợp chất sau vào vị trí tương ứng trong trục biểu diễn số oxi hoá của nitrogen: NO, N2O, NO2, NH3, HNO2, HNO3, NH4Cl, KNO2, NaNO3.....
Hoạt động 2 trang 30 Hóa học 11: Dựa vào trục biểu diễn số oxi hoá của nitrogen để giải thích nitrogen có cả tính oxi hoá và tính khử. Viết một quá trình oxi hoá và một quá trình khử để minh hoạ.....
Hoạt động 1 trang 30 Hóa học 11: Viết công thức electron, công thức Lewis và công thức cấu tạo của phân tử nitrogen......
Hoạt động 2 trang 30 Hóa học 11: Từ cấu tạo phân tử, hãy cho biết tại sao phân tử N2 có năng lượng liên kết lớn. Dự đoán về khả năng hoạt động hoá học của nitrogen ở nhiệt độ thường.....
Câu hỏi 1 trang 30 Hóa học 11: Dựa vào sự tương tác van der Waals, hãy giải thích tại sao đơn chất N2 khó hoá lỏng và ít tan trong nước.....
Câu hỏi 2 trang 31 Hóa học 11: Trong phương trình hoá học của phản ứng tổng hợp ammonia, hãy xác định các nguyên tử có sự thay đổi số oxi hoá và vai trò của nitrogen.....
Câu hỏi 3 trang 31 Hóa học 11: Trong phương trình hoá học của phản ứng giữa nitrogen với oxygen:....
Câu hỏi 4 trang 31 Hóa học 11: Viết các phương trình hoá học minh hoạ quá trình hình thành đạm nitrate trong tự nhiên xuất phát từ nitrogen......
Hoạt động trang 32 Hóa học 11: Sưu tầm một số hình ảnh để báo cáo, thuyết trình về ứng dụng của nitrogen trong thực tiễn. Sử dụng các tính chất vật lí và hoá học để giải thích cơ sở khoa học của các ứng dụng này.....
Câu hỏi 5 trang 32 Hóa học 11: a) Tại sao nitrogen lỏng được dùng để bảo quản mẫu vật phẩm trong y học?....
Em có thể trang 32 Hóa học 11: - Giải thích quá trình tạo và cung cấp ion nitrate cho đất từ nước mưa.....
Xem thêm các bài giải SGK Hóa lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 3: Ôn tập chương 1
Bài 4: Nitrogen
Bài 5: Ammonia. Muối ammonium
Bài 6: Một số hợp chất của nitrogen với oxygen
Bài 7: Sulfur và sulfur dioxide