Tailieumoi.vn xin giới thiệu đến các quý Thầy/Cô Giáo án điện tử Hóa học lớp 11 Kết nối tri thức theo mẫu Giáo án POWERPOINT chuẩn của Bộ GD&ĐT. Hi vọng tài liệu này sẽ giúp Giáo viên dễ dàng biên soạn giáo án PPT Hóa học 11.
Chỉ từ 400k mua trọn bộ Giáo án Hóa học 11 Kết nối tri thức bản POWERPOINT trình bày đẹp mắt, thiết kế hiện đại (chỉ từ 30k cho 1 bài Giáo án lẻ bất kì):
B1: Gửi phí vào tài khoản0711000255837 - NGUYEN THANH TUYEN - Ngân hàng Vietcombank (QR)
B2: Nhắn tin tới zalo Vietjack Official - nhấn vào đây
Xem thử tài liệu tại đây: Link tài liệu
Bài giảng điện tử Hóa 11 Bài 4: Nitrogen







................................................
................................................
................................................
Tài liệu có 24 trang, trên đây trình bày tóm tắt 10 trang của Giáo án POWERPOINT Hóa 11 Kết nối tri thức Bài 4: Nitrogen.
Giáo án Bài 4: Nitrogen
I. Mục tiêu
1. Kiến thức
Trình bày được:
- Trạng thái tự nhiên; cấu tạo nguyên tử, phân tử của nguyên tố nitrogen.
- Tính chất vật lý và tính chất hóa học của nitrogen.
- Ứng dụng của nitrogen trong thực tiễn.
2. Năng lực:
2.1. Năng lực chung
- Năng lực tự chủ tự học: HS nghiêm túc thực hiện nhiệm vụ, trả lời câu hỏi tìm hiểu về nguyên tố nitrogen.
- Năng lực giải quyết vấn đề và sáng tạo: Từ kiến thức đã học HS vận dụng giải quyết các nhiệm vụ học tập và câu hỏi bài tập.
- Năng lực giao tiếp và hợp tác: Sử dụng ngôn ngữ hóa học đọc tên nguyên tố và hợp chất của nitrogen. Biết chủ động giao tiếp khi có vấn đề thắc mắc. Thông qua làm việc nhóm nâng cao khả năng trình bày ý kiến của bản thân, tự tin thuyết trình trước đám đông.
2.2. Năng lực Hóa học
- Năng lực nhận thức kiến thức hóa học:
+ Phát biểu được trạng thái tự nhiên của nguyên tố nitrogen.
+ Trình bày được sự hoạt động của đơn chất nitrogen ở nhiệt độ cao đối với hydrogen, oxygen.
Liên hệ quá trình tạo và cung cấp nitrate cho đất từ nước mưa.
- Năng lực vận dụng kiến thức, kĩ năng đã học:
+ Giải thích được tính trơ của đơn chất nitrogen ở nhiệt độ thường thông qua liên kết và giá trị năng lượng liên kết.
+ Giải thích được các ứng dụng của đơn chất nitrogen khí và lỏng trong sản xuất, trong hoạt động nghiên cứu.
+ Viết được phương trình hóa học của nitrogen với hydrogen, oxygen.
- Năng lực tìm hiểu thế giới tự nhiên dưới góc độ hóa học
+ Được thực hiện thông qua hoạt động thảo luận nhóm về nội dung liên hệ quá trình tạo và cung cấp nitrate cho đất từ nước mưa.
2. Phẩm chất
- Trung thực: Thật thà, ngay thẳng trong kết quả làm việc nhóm.
- Trách nhiệm: Có tinh thần trách nhiệm cao để hoàn thành tốt nhiệm vụ được phân công.
II. Thiết bị dạy học và học liệu
1. Giáo viên:
- Kế hoạch dạy học.
- Bài giảng powerpoint.
- Dụng cụ thí nghiệm: Trình chiếu TN ảo (Nittrogen cháy trong oxi)
- Phiếu bài tập
- Video, hình ảnh liên quan.
2. Học sinh:
- Sách giáo khoa.
- Đọc trước bài ở nhà.
III. Tiến trình dạy học
1. Hoạt động 1: Khởi động ( 5 phút)
a) Mục tiêu:
- Tạo hứng thú cho HS học tập, tạo sự tò mò cho hs có nhu cầu tìm hiểu kiến thức mới, tạo tâm thế thoải mái cho tiết học.
- Cho HS thông tin bước đầu về nguyên tố nitrogen.
b) Nội dung: Tìm hiểu vị trí và cấu hình electron của nguyên tử N
c) Sản phẩm, đánh giá kết quả của hoạt động
-Sản phẩm hoạt động
X thuộc ô 7; chu kì 2; nhóm VA.
-Đánh giá kết quả hoạt động
+ Thông qua quan sát: Trong quá trình HS cá nhân, GV cần quan sát kĩ tất cả các nhóm, kịp thời phát hiện những khó khăn, vướng mắc của HS và có giải pháp hỗ trợ hợp lí
+ Thông qua kết quả của một số cá nhân HS và sự góp ý, bổ sung của các HS khác, GV biết được HS đã có được những kiến thức nào, những kiến thức nào cần phải điều chỉnh, bổ sung các HĐ tiếp theo.
d) Phương thức tổ chức hoạt động
-HĐ cá nhân: GV yêu cầu HS dựa vào các câu thơ sau xác định vị trí của nguyên tố X.
“Nhà em ở chu kì hai.
Có năm điện tử lớp ngoài bao che.
Mùa đông cho đến mùa hè.
Nhớ ô thứ bảy anh về thăm em”.
-HĐ chung: GV gọi một số HS lên trình bày kết quả, các HS khác góp ý bổ sung. GV giúp HS nhận ra những sai sót, chỉnh sửa và chuẩn hóa kiến thức.
- Dự kiến khó khăn, vướng mắc của HS và giải pháp hỗ trợ:
HS có thể lung túng khi xã định nhóm của nguyên tố X. GV có thể gợi ý vào vị trí của ô để khẳng định X thuộc nhóm A và dựa vào số e lớp ngoài cùng để xác định thứ tự nhóm
2. Hoạt động: Hình thành kiến thức
Hoạt động 1: Trạng thái tự nhiên (5 phút)
a. Mục tiêu
- Trình bày được trạng thái tự nhiên của nguyên tố nitrogen.
b. Nội dung
- Sử dụng phương pháp đàm thoại gợi mở, nhóm để tìm hiểu về trạng thái tự nhiên của nitrogen.
c. Sản phẩm
- Phát biểu được trạng thái tự nhiên của nguyên tố nitrogen:
+ Trong khí quyển Trái Đất, nitrogen là nguyên tố phổ biến nhất, chiếm 75,5% khối lượng, 78,1% thể tích.
+ Trong vỏ trái đất, nguyên tố nitrogen tồn tại ở một số mỏ khoáng dưới dạng sodium nitrate (thường gọi là diêm tiêu Chile). Ngoài ra còn co trong cơ thể động vật và thực vật.
+ Nguyên tố nitrogen tồn tại trong tự nhiên với 2 đồng vị bền là 14N (99,63%) và 15N (0,37%).
d) Tổ chức thực hiện
+ HĐ chất vấn HS về trạng thái tự nhiên của nitrogen.
Hoạt động 2: Cấu tạo nguyên tử, phân tử (5 phút)
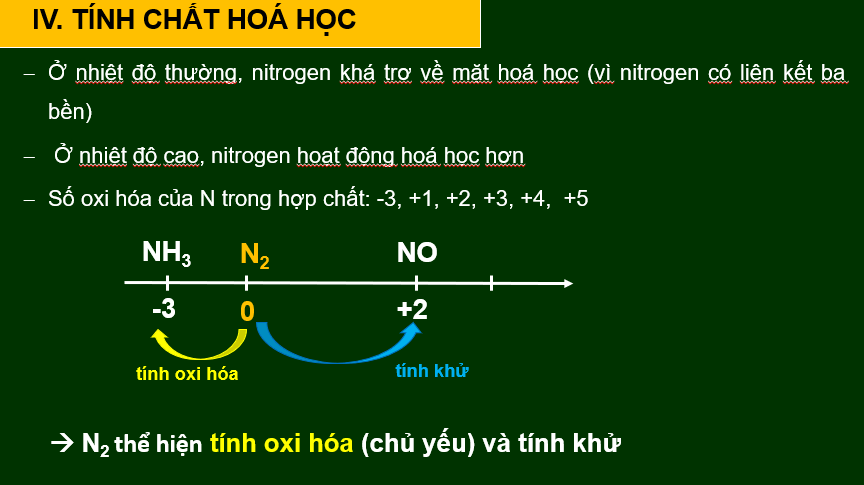
- Dự đoán về khả năng hoạt động hoá học của nitrogen ở nhiệt độ thường.
|
Mục tiêu: - Nêu được vị trí của của nitrogen trong bảng tuần hoàn - Viết được cấu hình e ntử của nitrogen, công thức electron, công thức Lewis và công thức cấu tạo của phân tử nitrogen. |
|
|
HOẠT ĐỘNG CỦA GV VÀ HS SẢN PHẨM DỰ KIẾN |
|
|
Giao nhiệm vụ học tập: HS kết hợp kết quả trong hoạt động khởi động và nghiên cứu SGK trả lời các câu hỏi sau: 1. Xác định vị trí của nguyên tố nitrogen trong bảng tuần hoàn. Viết cấu hình electron của nguyên tử? 2. Viết công thức phân tử và công thức electron, công thức Lewis, công thức cấu tạo của phân tử nitrogen? Nhận xét về liên kết trong phân tử N2? Dự đoán về khả năng hoạt động hoá học của nitrogen ở nhiệt độ thường. Thực hiện nhiệm vụ: - Sử dụng phương pháp đàm thoại gợi mở, phương pháp trực quan, hoạt động nhóm để tìm hiểu về cấu tạo nguyên tử, phân tử nitrogen. - HĐ cá nhân: GV cho HS quan sát Bảng hệ thống tuần hoàn, mô hình phân tử nitrogen
BHTTH Mô hình phân tử nitrogen - HĐ nhóm: GV cho HS hoạt động nhóm nhằm trao đổi, bổ sung trong kết quả hoạt động cá nhân và ghi kết quả chung vào bảng phụ. Báo cáo, thảo luận: GV gọi một số HS lên trình bày kết quả, các HS khác góp ý bổ sung. GV giúp HS nhận ra những sai sót, chỉnh sửa và chuẩn hóa kiến thức Kết luận, nhận định: GV nhận xét và kết luận + Thông qua quan sát: Trong quá trình HS cá nhân, GV cần quan sát kĩ để kịp thời phát hiện những khó khăn, vướng mắc của HS và có giải pháp hỗ trợ hợp lí + Thông qua kết quả của một số HS và sự góp ý, bổ sung của các HS khác, GV biết được HS đã có được những kiến thức nào, những kiến thức nào cần phải điều chỉnh, bổ sung. - Dự kiến khó khăn, vướng mắc của HS và giải pháp hỗ trợ. HS có thể gặp khó khăn khi xác định loại liên kết giữa hai nguyên tử nitrogen. GV kết nối từ kiến thức đã học liên kết cộng hóa trị không cực. HS cũng có thể gặp khó khăn viết công thức electron, công thức Lewis và công thức cấu tạo của N2. GV gợi ý HS nhắc lại sự hình thành liên kết cộng hóa trị. |
II. CẤU TẠO NGUYÊN TỬ, PHÂN TỬ:
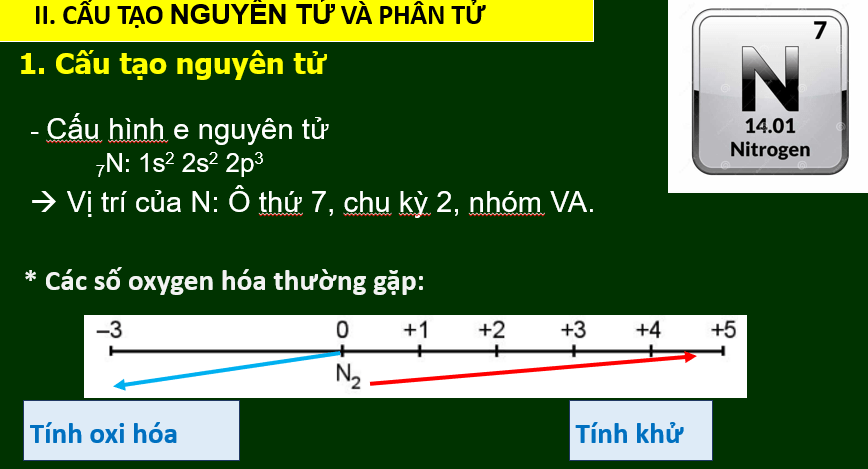
1. Cấu tạo nguyên tử - Cấu hình e của N (Z = 7) 1s22s22p3 có 5e ở lớp ngoài cùng. - Vị trí của N trong bảng tuần hoàn: Ô thứ 7, nhóm VA, chu kì 2. 2. Cấu tạo phân tử: - CT electron, công thức Lewis: Phân tử nitrogen gồm 2 nguyên tử N, liên kết với nhau bằng 3 liên kết cộng hóa trị không cực. - CTCT: N - CTPT: N2; CTCT: N
|
................................................
................................................
................................................
Xem thêm các bài giảng điện tử Hóa 11 Kết nối tri thức hay, chi tiết khác:
Bài 6: Một số hợp chất của nitrogen với oxygen
Bài 7: Sulfur và sulfur dioxide
Bài 8: Sulfuric acid và muối sulfate
Để mua Giáo án PPT Hóa học 11 Kết nối tri thức năm 2024 mới nhất, mời Thầy/Cô liên hệ Mua tài liệu hay, chọn lọc