Với giải Bài 14.6 trang 56 SBT Hóa học lớp 10 Chân trời sáng tạo chi tiết trong Bài 14: Tính biến thiên enthalpy của phản ứng hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 10. Mời các bạn đón xem:
Giải sách bài tập Hóa học lớp 10 Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Bài 14.6 trang 57 SBT Hóa học 10. Phosgene là chất khí không màu, mùi cỏ mục, dễ hóa lỏng; khối lượng riêng 1,420 g/cm3 (ở 0oC); ts = 8,2 oC. Phosgene ít tan trong nước; dễ tan trong các dung môi hữu cơ, bị thủy phân chậm bằng hơi nước; không cháy; là sản phẩm công nghiệp quan trọng; dùng trong tổng hợp hữu cơ để sản xuất sản phẩm nhuộm, chất diệt cỏ, polyurethane, …
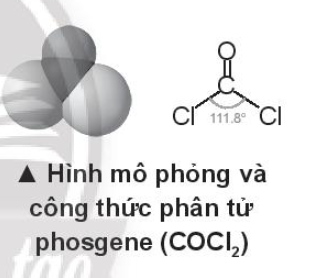
Phosgene là một chất độc. Ở nồng độ 0,005 mg/L đã nguy hiểm đối với người; trong khoảng 0,1 – 0,3 mg/L, gây tử vong sau khoảng 15 phút.
Phosgene được điều chế bằng cách cho hỗn hợp CO và Cl2 đi qua than hoạt tính. Biết: Eb(Cl-Cl) = 243 kJ/mol; Eb(C-Cl) = 339 kJ/mol; Eb(C=O) = 745 kJ/mol;
Eb(C ≡ O) = 1075 kJ/mol.
Hãy tính biến thiên enthalpy của phản ứng tạo thành phosgene từ CO và Cl2.
Lời giải:
Phản ứng hoá học: (Phosgene)
Áp dụng công thức:
= 1075 + 243 – 2.339 - 745 = - 105 kJ
Xem thêm các bài giải SBT Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 14.1 trang 56 SBT Hóa học 10. Trình bày cách tính enthalpy của phản ứng hóa học dựa vào năng lượng liên kết và dựa vào enthalpy tạo thành của các chất.
Bài 14.2 trang 56 SBT Hóa học 10. Cho phản ứng tổng quát: . Hãy chọn các phương án tính đúng ...
Bài 14.3 trang 56 SBT Hóa học 10. Thành phần chính của đa số các loại đá dùng trong xây dựng là CaCO3, chúng vừa có tác dụng chịu nhiệt, vừa chịu được lực. Dựa vào bảng 13.1 SGK trang 84, tính ...
Bài 14.4 trang 56 SBT Hóa học 10. Propene là nguyên liệu cho sản xuất nhựa polypropylene (PP). PP được sử dụng để sản xuất các sản phẩm ống, màng, dây cách điện, kéo sợi, đồ gia dụng và các sản phẩm tạo hình khác.
Bài 14.5 trang 57 SBT Hóa học 10. Tính nhiệt tạo thành chuẩn của HF và NO dựa vào năng lượng liên kết (Bảng 14.1 SGK), của F2, H2, HF, N2, O2, NO. Giải thích sự khác nhau về nhiệt tạo thành của HF và NO.
Bài 14.6 trang 57 SBT Hóa học 10. Phosgene là chất khí không màu, mùi cỏ mục, dễ hóa lỏng; khối lượng riêng 1,420 g/cm3 (ở 0oC); ts = 8,2 oC. Phosgene ít tan trong nước; dễ tan trong các dung môi hữu cơ, bị thủy phân chậm bằng hơi nước; không cháy; là sản phẩm công nghiệp quan trọng; dùng trong tổng hợp hữu cơ để sản xuất sản phẩm nhuộm, chất diệt cỏ, polyurethane, …
Bài 14.7 trang 57 SBT Hóa học 10. Kim loại nhôm có thể khử được oxide của nhiều nguyên tố. Dựa vào nhiệt tạo thành chuẩn của các chất (Bảng 13.1 SGK), tính biến thiên enthalpy của phản ứng nhôm khử 1 mol mỗi oxide sau:
Bài 14.8* trang 58 SBT Hóa học 10. Cho 3 hydrocarbon X, Y, Z đều có 2 nguyên tử C trong phân tử. Số nguyên tử H trong các phân tử tăng dần theo thứ tự X, Y, Z.
Bài 14.9 trang 58 SBT Hóa học 10. Cho các phản ứng:
Bài 14.10 trang 58 SBT Hóa học 10. Lactic acid hay acid sữa là hợp chất hóa học đóng vai trò quan trọng trong nhiều quá trình sinh hóa, lần đầu tiên được phân tách vào năm 1780 bởi nhà hóa học Thụy Điển Carl Wilhelm Scheele. Lactic acid có công thức phân tử C3H6O3, công thức cấu tạo CH3-CH(OH)-COOH.
Bài 14.11 trang 59 SBT Hóa học 10. Chloromethane (CH3Cl), còn được gọi là methyl chloride, Refrigerant-40 hoặc HCC 40. CH3Cl từng được sử dụng rộng rãi như một chất làm lạnh. Hợp chất khí này rất dễ cháy, có thể không mùi hoặc mùi thơm nhẹ.
Bài 14.12* trang 59 SBT Hóa học 10. Một xe tải đang vận chuyển đất đèn (thành phần chính là CaC2 và CaO) gặp mưa xảy ra sự cố, xe tải đã bốc cháy.
Bài 14.13 trang 59 SBT Hóa học 10. Cho phương trình hóa học của phản ứng:
Bài 14.14* trang 59 SBT Hóa học 10. Cho phản ứng phân hủy hydrazine:
Bài 14.15 trang 59 SBT Hóa học 10. Quá trình hòa tan calcium chloride trong nước:
Xem thêm các bài giải SBT Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Ôn tập chương 5
Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
