Với giải sách bài tập Hoá học 10 Bài 14: Tính biến thiên enthalpy của phản ứng hóa học sách Chân trời sáng tạo hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hoá học 10. Mời các bạn đón xem:
Giải SBT Hoá học lớp 10 Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Lời giải:
Cho phản ứng tổng quát ở điều kiện chuẩn:
aA (g) + bB (g) → mM (g) + nN (g)
- Tính của phản ứng khi biết các giá trị năng lượng liên kết (Eb) theo công thức:
Hay tổng quát:
Với ∑Eb (cđ); ∑Eb (sp): tổng năng lượng liên kết trong phân tử chất đầu và sản phẩm của phản ứng.
- Có thể tính được biến thiên enthalpy chuẩn của một phản ứng hóa học () khi biết các giá trị của tất cả các chất đầu và sản phẩm theo công thức sau:
Tổng quát:
Với : tổng enthalpy tạo thành ở điều kiện chuẩn tương ứng của sản phẩm và chất đầu của phản ứng.
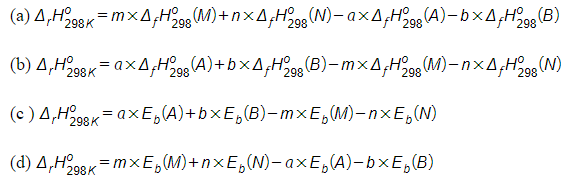
Lời giải:
Các phương án đúng là (a) và (c).
Giải thích:
- Cách tính enthalpy của phản ứng hoá học dựa vào năng lượng liên kết:
Với : tổng năng lượng liên kết trong phân tử chất đầu và sản phẩm của phản ứng.
- Cách tính enthalpy của phản ứng hoá học dựa vào enthalpy tạo thành:
Với : tổng enthalpy tạo thành ở điều kiện chuẩn của sản phẩm và chất đầu của phản ứng
Phản ứng có xảy ra thuận lợi ở điều kiện thường không?
Lời giải:
Phản ứng:
= - 635,1 + (-393,5) - (-1 206,9) = +178,3 kJ/mol
Phản ứng không xảy ra ở điều kiện thường, do > 0.
Phản ứng tạo thành propene từ propyne:
a) Hãy xác định số liên kết trong hợp chất (propyne)
Lời giải:
a) Công thức cấu tạo đầy đủ của propyne:
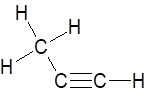
Trong hợp chất số liên kết C-H là 4; C-C là 1; C≡C là 1.
b) Biên thiên enthalpy của phản ứng:
= 839 kJ/mol, Eb(H-H) = 432 kJ/mol.
![]()
= 839 + 347 + 4.413 + 432 – 614 – 347 – 6.413 = -169 kJ.
Lời giải:
Áp dụng công thức:
= 945 kJ/mol,
Eb(O=O) = 498 kJ/mol; Eb(N≡O) = 631 kJ/mol;
Nhiệt tạo thành 1 mol HF:
432 + 159 – 2.565 = -539 kJ < 0
⇒ Phản ứng xảy ra.
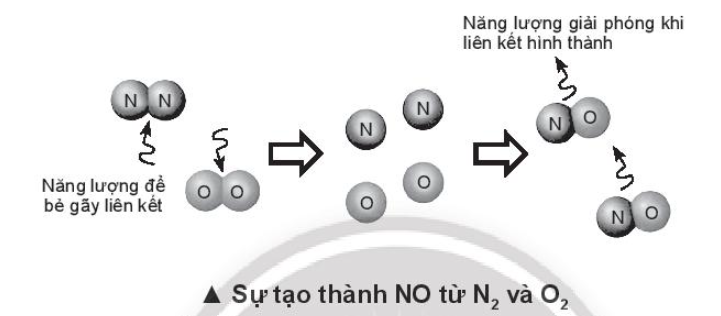
Nhiệt tạo thành 1 mol NO:
(NO) = 945 + 498 – 2.631 = +181 kJ > 0
⇒ Phản ứng không xảy ra
Hãy tính biến thiên enthalpy của phản ứng tạo thành phosgene từ CO và Cl2.
Lời giải:
Phản ứng hoá học: (Phosgene)
Áp dụng công thức:
= 1075 + 243 – 2.339 - 745 = - 105 kJ
Lời giải:
Áp dụng công thức:
a)
(1) = 4.(-1 676,00) – 3.(-1 121,00) = -3 341,00 kJ
Biến thiên enthalpy của phản ứng nhôm khử 1 mol Fe3O4 là
b)
(2)= -1 676,00 - (-1 128,60) = -547,4 kJ
Biến thiên enthalpy của phản ứng nhôm khử 1 mol Cr2O3 là
1. (2) = -547,4 kJ
a) Viết công thức cấu tạo của X, Y, Z.
b) Viết phương trình đốt cháy hoàn toàn X, Y, Z với hệ số nguyên tối giản.
c) Tính biến thiên enthalpy của mỗi phản ứng dựa vào enthalpy tạo thành tiêu chuẩn trong bảng sau.
d) Từ kết quả tính toán đưa ra kết luận về ứng dụng của phản ứng đốt cháy X, Y, Z trong thực tiễn.
Lời giải:
a) Ba hydrocarbon X, Y, Z lần lượt là HC≡CH (ethyne hay acetylene),
H2C=CH2 (ethene hay ethylene), H3C-CH3 (ethane).
b) Phản ứng hoá học xảy ra:
c)
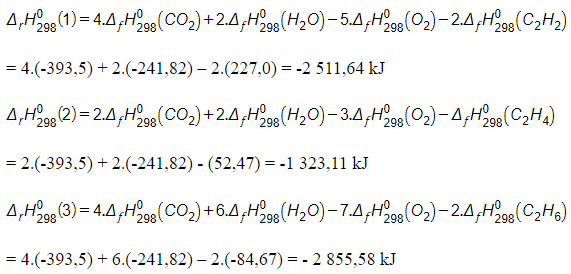
d) Kết quả tính toán của phản ứng đốt cháy acetylene; ethylene; ethane giá trị lớn và < 0 (giải phóng năng lượng lớn) nên trong thực tiễn được sử dụng làm nhiên liệu. Riêng C2H2 trong thực tiễn làm đèn xì acetylene vì đèn xì acetylene có nhiệt độ cao nhất.
Bài 14.9 trang 58 SBT Hóa học 10. Cho các phản ứng:
a) Phản ứng nào có thể tự xảy ra (sau giai đoạn khơi mào ban đầu), phản ứng nào không thể tự xảy ra?
Lời giải:
a) Phản ứng nung vôi không tự xảy ra do > 0 nên cần nguồn nhiệt ngoài.
Hai phản ứng còn lại có thể tự xảy ra sau giai đoạn khơi mào do < 0.
b) Lượng nhiệt cần đề thu được 0,1 mol CaO là 0,1.178,49 = +17,849 kJ. Vậy:
Lượng C(graphite,s) cần dùng :
Lời giải:
Tính khối lượng lactic acid tạo ra từ quá trình chạy bộ. Năng lượng của sự chuyển hoá glucose thành lactic acid trong quá trình chạy bộ chiếm
2% . 300 kcal = 6 kcal = 6 000 cal ⟺ 25 104 J = 25,104 kJ.
C6H12O6 → 2C3H6O3
0,335 mol ← -25,104 kJ
Khối lượng lactic acid được tạo ra trong quá trình chuyển hoá:
0,335.90 = 30,15 g.
CH4 (g) + Cl2 (g) → CH3Cl (g) + HCl (g)
Lời giải:
Dựa vào công thức tính theo năng lượng liên kết cho phản ứng:
CH4 (g) + Cl2 (g) → CH3Cl (g) + HCl (g)
= 4.Eb(C-H) + Eb(Cl-Cl) - [3. Eb(C-H) + Eb(C-Cl)] – Eb(H-Cl)
= 4.413 + 243 - (3.413 + 339) - 427 = -110 kJ.
Phản ứng có < 0 nên thuận lợi về mặt nhiệt nên có thể tự xảy ra.
Kết quả tính hoàn toàn phù hợp với thực tế phản ứng xảy ra dễ dàng.
a. Viết phản ứng của CaC2 và CaO với nước.
b. Xe tải bốc cháy do các phản ứng trên tỏa nhiệt kích thích phản ứng cháy của acetylene:
Lời giải:
a) Các phản ứng xảy ra:
b) Phản ứng cháy:
![]()
= 2.(-393,50) + (-241,82) - (+227,00)- .0 = -1 255,82 kJ
Do < 0 nên phản ứng toả nhiệt.
Bài 14.13 trang 59 SBT Hóa học 10. Cho phương trình hóa học của phản ứng:
Tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành chuẩn của các chất (Bảng 13.1 SGK)
Lời giải:
Phản ứng:
Biến thiên enfhalpy của phản ứng tính theo nhiệt tạo thành chuẩn:
= - 277,63 - (+52,47) - (-285,84) = -44,26 kJ
Do < 0 nên phản ứng toả nhiệt.
Bài 14.14* trang 59 SBT Hóa học 10. Cho phản ứng phân hủy hydrazine:
a. Tính theo năng lượng liên kết của phản ứng trên.
Lời giải:
a) Hydrazine có công thức cấu tạo: H2N-NH2. Một phân tử hydrazine có 1liên kết đơn N-N (Eb = 160 kJ/mol); 4 liên kết đơn N-H (Eb = 391 kJ/mol). N2 có1 liên kết ba N≡N (Eb = 945 kJ/mol), H2 có 1 liên kết đơn H-H (Eb = 432 kJ/mol).
Áp dụng công thức tính. theo năng lượng liên kết:
= Eb(N-N) + 4.Eb(N-H) – Eb(N≡N) – 2.E(H-H)
= 160 + 4.391 - 945 – 2.432 = -85 kJ
b) Lí do N2H4 được sử dụng làm nhiên liệu trong động cơ tên lửa:
– N2H4 là chất lỏng ở điều kiện thường nên dễ bảo quản (nếu là chất khí cần nén ở áp suất cao gây nguy hiểm).
- Khối lượng riêng nhỏ nên nhẹ, phù hợp với nhiên liệu động cơ tên lửa (nếu nặng sẽ gây tốn năng lượng). = - 85 kJ < 0 nên phản ứng có thẻ tự xảy ra mà không cần nguồn nhiệt ngoài.
- Giả sử 1 mol N2H4 lỏng phản ứng (có thẻ tích khá nhỏ) sẽ sinh ra 3 mol khí có thể tích lớn hơn rất nhiều nên sẽ tạo được luồng khí đây tên lửa đi.
Bài 14.15 trang 59 SBT Hóa học 10. Quá trình hòa tan calcium chloride trong nước:
Tính biến thiên enthapy của quá trình.
Lời giải:
Enthalpy của quá trình:
= - 542,83 - 167,16 - (-795,00) = 85,01 kJ.
Xem thêm các bài giải SBT Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng
Bài 16: Các yếu tố ảnh hưởng đến tốc độ phản ứng hóa học
Lý thuyết Tính biến thiên enthalpy của phản ứng hóa học
I. Xác định biến thiên enthalpy của phản ứng dựa vào năng lượng liên kết
- Phản ứng hóa học xảy ra khi có sự phá vỡ các liên kết hóa học của chất đầu (cđ) và hình thành các liên kết hóa học của sản phẩm (sp). Sự phá vỡ các liên kết cần cung cấp năng lượng, sự hình thành các liên kết lại giải phóng năng lượng.
- Cho phản ứng tổng quát ở điều kiện chuẩn:
aA (g) + bB (g) → mM (g) + nN (g)
Tính của phản ứng khi biết các giá trị năng lượng liên kết (Eb) theo công thức:
Hay tổng quát:
Với ∑Eb (cđ); ∑Eb (sp): tổng năng lượng liên kết trong phân tử chất đầu và sản phẩm của phản ứng.
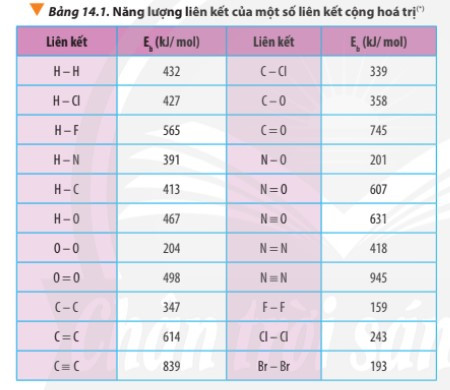
- Ví dụ: Dựa vào bảng năng lượng liên kết (phía trên) tính biến thiên enthalpy của phản ứng: 3H2(g) + N2(g) → 2NH3(g)
= 3.Eb(H2) + Eb(N2) – 2.Eb(NH3)
= 3.Eb(H-H) + Eb(N≡N) – 2.3.Eb(N-H)
= 3.432 + 945 – 2.3.391
= -105 kJ < 0 ⇒ Phản ứng tỏa nhiệt
Chú ý: Tính biến thiên enthalpy của phản ứng dựa vào năng lượng liên kết được áp dụng cho phản ứng trong đó các chất đều có liên kết cộng hóa trị ở thể khí khi biết giá trị năng lượng liên kết của tất cả các chất trong phản ứng.
II. Xác định biến thiên enthalpy của phản ứng dựa vào enthalpy tạo thành
- Cho phương trình hóa học tổng quát:
aA + bB → mM + nN
- Tổng quát:
Với : tổng enthalpy tạo thành ở điều kiện chuẩn tương ứng của sản phẩm và chất đầu của phản ứng.
- Ví dụ: Tính ∆r phản ứng đốt cháy hoàn toàn benzene C6H6(l) trong khí oxygen.
C6H6(l) + O2(g) 6CO2(g) + 3H2O(l)
∆ r = 6.∆ f(CO2) + 3. ∆ f(H2O) - ∆ f(C6H6) - ∆ f(O2)
∆ r = 6.(-393,50) + 3.(-285,84) – (+49,00) - .0
∆ r = -3267,52 kJ