Với giải Bài 14.5 trang 57 SBT Hóa học lớp 10 Chân trời sáng tạo chi tiết trong Bài 14: Tính biến thiên enthalpy của phản ứng hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 10. Mời các bạn đón xem:
Giải sách bài tập Hóa học lớp 10 Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
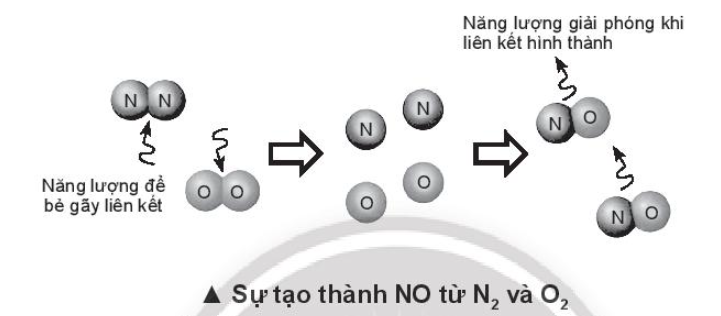
Bài 14.5 trang 57 SBT Hóa học 10. Tính nhiệt tạo thành chuẩn của HF và NO dựa vào năng lượng liên kết (Bảng 14.1 SGK), của F2, H2, HF, N2, O2, NO. Giải thích sự khác nhau về nhiệt tạo thành của HF và NO.
Lời giải:
Áp dụng công thức:
= 945 kJ/mol,
Eb(O=O) = 498 kJ/mol; Eb(N≡O) = 631 kJ/mol;
Nhiệt tạo thành 1 mol HF:
432 + 159 – 2.565 = -539 kJ < 0
⇒ Phản ứng xảy ra.
Nhiệt tạo thành 1 mol NO:
(NO) = 945 + 498 – 2.631 = +181 kJ > 0
⇒ Phản ứng không xảy ra
Xem thêm các bài giải SBT Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 14.2 trang 56 SBT Hóa học 10. Cho phản ứng tổng quát: . Hãy chọn các phương án tính đúng ...
Bài 14.9 trang 58 SBT Hóa học 10. Cho các phản ứng:
Bài 14.13 trang 59 SBT Hóa học 10. Cho phương trình hóa học của phản ứng:
Bài 14.14* trang 59 SBT Hóa học 10. Cho phản ứng phân hủy hydrazine:
Bài 14.15 trang 59 SBT Hóa học 10. Quá trình hòa tan calcium chloride trong nước:
Xem thêm các bài giải SBT Hoá học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học
Bài 14: Tính biến thiên enthalpy của phản ứng hóa học
Bài 15: Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng