Với giải Bài 14.14 trang 37 SBT Hóa học lớp 10 Kết nối tri thức chi tiết trong Bài 14: Ôn tập chương 3 giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 10. Mời các bạn đón xem:
Giải sách bài tập Hóa học lớp 10 Bài 14: Ôn tập chương 3
Bài 14.14 trang 38 SBT Hóa học 10: Dựa vào giá trị của độ âm điện ở Bảng 6.2 trong sách giáo khoa Hóa học 10, hãy nêu bản chất liên kết trong các phân tử và ion sau: HClO, KHS, HCO3-, K2SO4.
Lời giải
Bản chất các liên kết phụ thuộc vào hiệu độ âm điện giữa hai nguyên tử của hai nguyên tố tạo liên kết. Viết công thức cấu tạo các phân tử và tính hiệu độ âm điện để suy ra bản chất liên kết.
H-Cl=O có hiệu độ âm điện H-Cl là 0,96 ⇒ Liên kết cộng hóa trị phân cực;
Cl-O là 0,28 ⇒ Liên kết cộng hóa trị không phân cực.
K+ và [S-H]- có hiệu độ âm điện K và S là 1,76 ⇒ liên kết ion;
S-H là 0,38 ⇒ liên kết cộng hóa trị phân cực.
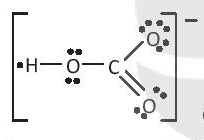 có hiệu độ âm điện H và O là 1,24 ⇒ liên kết cộng hóa trị phân cực;
có hiệu độ âm điện H và O là 1,24 ⇒ liên kết cộng hóa trị phân cực;
C-O có hiệu độ âm điện là 0,89 ⇒ liên kết cộng hóa trị phân cực.
* K+ và 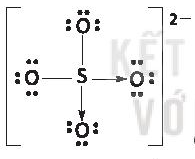 có hiệu độ âm điện K-O là 2,62 ⇒ liên kết ion;
có hiệu độ âm điện K-O là 2,62 ⇒ liên kết ion;
S-O là 1,54 ⇒ liên kết cộng hóa trị phân cực.
Xem thêm các bài giải SBT Hoá học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 14.1 trang 36 SBT Hóa học 10: Quy tắc octet không đúng với trường hợp phân tử chất nào sau đây?
Bài 14.2 trang 36 SBT Hóa học 10: Phát biểu nào sau đây không đúng về liên kết có trong phân tử HCl?
Bài 14.3 trang 36 SBT Hóa học 10: Liên kết ion khác với liên kết cộng hóa trị ở điểm nào sau đây?
Bài 14.4 trang 36 SBT Hóa học 10: Cho chất hữu cơ A có công thức cấu tạo sau:
Bài 14.5 trang 36 SBT Hóa học 10: Cho giá trị độ âm điện của một số nguyên tố sau: Na (0,93); Li (0,98); Mg (1,31); Al (1,61); P (2,19); S (2,58); Br (2,96) và Cl (3,16).
Bài 14.6 trang 36 SBT Hóa học 10: Cho hai chất hữu cơ X và Y có công thức cấu tạo sau:
Bài 14.7 trang 37 SBT Hóa học 10: Nguyên tố X ở nhóm IA và nguyên tố Y ở nhóm VIIA của bảng tuần hoàn. X và Y có thể tạo thành hợp chất R. Liên kết giữa các nguyên tử trong R thuộc loại liên kết nào sau đây?
Bài 14.8 trang 37 SBT Hóa học 10: X, Y, Z là những nguyên tố có số hiệu nguyên tử lần lượt là 8, 19, 16. Các cặp nguyên tố có thể tạo thành liên kết ion và cộng hóa trị phân cực lần lượt là
Bài 14.9 trang 37 SBT Hóa học 10: Cho các chất sau: N2, H2, NH3, NaCl, HCl, H2O
Bài 14.10 trang 37 SBT Hóa học 10: Cho các chất sau:
Bài 14.11 trang 37 SBT Hóa học 10: Dùng công thức Lewis để biểu diễn phân tử SO3 sao cho phù hợp với quy tắc octet. Chỉ rõ các liên kết trong phân tử thuộc loại liên kết nào.
Bài 14.12 trang 37 SBT Hóa học 10: Hợp chất NaClO là thành phần của chất tẩy rửa, sát trùng có tên gọi là ‘Nước Javen”. Áp dụng quy tắc octet để giải thích sự hình thành các liên kết trong hợp chất đó.
Bài 14.13 trang 38 SBT Hóa học 10: Tính số liên kết σ và liên kết π trong các phân tử sau:
Bài 14.14 trang 38 SBT Hóa học 10: Dựa vào giá trị của độ âm điện ở Bảng 6.2 trong sách giáo khoa Hóa học 10, hãy nêu bản chất liên kết trong các phân tử và ion sau: HClO, KHS, HCO3-, K2SO4.
Bài 14.15 trang 38 SBT Hóa học 10: Cho dãy các chất kèm theo nhiệt độ sôi (oC) sau:
Bài 14.16 trang 38 SBT Hóa học 10: Cho biết tổng số electron trong anion là 42. Trong các hạt nhân A cũng như B có số proton bằng số neutron.
Bài 14.17 trang 38 SBT Hóa học 10: Hợp chất X được sử dụng làm thuốc pháo, ngòi nổ, thuốc đầu diêm, thuốc giúp nhãn ra hoa, … X có khối lượng mol bằng 122,5 g/mol, chứa ba nguyên tố, trong đó nguyên tố s có 7 electron s, nguyên tố p có 11 electron p và nguyên tố p có 4 electron p. Thành phần phần trăm khối lượng nguyên tố có 4 electron p trong X bằng 39,19%.
Xem thêm các bài giải SBT Hoá học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 13: Liên kết hydrogen và tương tác van der Waals