Với giải sách bài tập Hoá học 10 Bài 15: Phản ứng oxi hóa – khử sách Kết nối tri thức hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hoá học 10. Mời các bạn đón xem:
Giải SBT Hoá học lớp 10 Bài 15: Phản ứng oxi hóa – khử
Nhận biết
Bài 15.1 trang 39 SBT Hóa học 10: Số oxi hóa là một số đại số đặc trưng cho đại lượng nào sau đây của nguyên tử trong phân tử?
A. Hóa trị
B. Điện tích
C. Khối lượng
D. Số hiệu
Lời giải
Đáp án đúng là: B
Số oxi hóa là điện tích quy ước của nguyên tử trong phân tử khi coi tất cả các electron liên kết đều chuyển hoàn toàn về nguyên tử có độ âm điện lớn hơn.
Bài 15.2 trang 39 SBT Hóa học 10: Trong hợp chất SO3, số oxi hóa của sulfur (lưu huỳnh) là
A. +2
B. +3
C. +5
D. +6
Lời giải
Đáp án đúng là: D
Số oxi hóa của O thường là -2
Đặt x là số oxi hóa của S
⇒ x.1 + (-2).3 = 0 ⇒ x = +6
Vậy số oxi hóa của S là +6
Bài 15.3 trang 39 SBT Hóa học 10: Fe2O3 là thành phần chính của quặng hematite đỏ, dùng để luyện gang. Số oxi hóa của iron (sắt) trong Fe2O3 là:
A. + 3
B. 3+
C. 3
D. -3
Lời giải
Đáp án đúng là: A
Số oxi hóa được viết ở dạng đại số, dấu viết trước, số viết sau ⇒ B sai.
Đặt x là số oxi hóa của Fe. O thường có số oxi hóa là -2
⇒ Ta có: x.2 + (-2).3 = 0
⇒ x = +3
Bài 15.4 trang 39 SBT Hóa học 10: Ammonia (NH3) là nguyên liệu để sản xuất nitric acid và nhiều loại phân bón. Số oxi hóa của nitrogen trong ammonia là
A. 3
B. 0
C. +3
D. -3
Lời giải
Đáp án đúng là: D
Đặt x là số oxi hóa của N. H thường có số oxi hóa là +1
⇒ Ta có: x.1 + (+1).3 = 0
⇒ x = -3
Bài 15.5 trang 39 SBT Hóa học 10: Chromium có số oxi hóa +2 trong hợp chất nào sau đây?
A. Cr(OH)3
B. Na2CrO4
C. CrCl2
D. Cr2O3
Lời giải
Đáp án đúng là: C
, , ,
Bài 15.6 trang 39 SBT Hóa học 10: Phản ứng oxi hóa – khử là phản ứng có sự nhường và nhận
A. electron
B. neutron
C. proton
D. cation
Lời giải
Đáp án đúng là: A
Phản ứng oxi hóa – khử là phản ứng có sự nhường và nhận electron.
Bài 15.7 trang 39 SBT Hóa học 10: Dấu hiệu để nhận ra một phản ứng oxi hóa – khử là dựa trên sự thay đổi đại lượng nào sau đây của nguyên tử?
A. Số khối
B. Số oxi hóa
C. Số hiệu
D. Số mol
Lời giải
Đáp án đúng là: B
Dấu hiệu để nhận ra một phản ứng oxi hóa – khử là dựa trên sự thay đổi số oxi hóa của các nguyên tử.
Bài 15.8 trang 39 SBT Hóa học 10: Trong phản ứng oxi hóa – khử, chất oxi hóa là chất
A. nhường electron
B. nhận electron
C. nhận proton
D. nhường proton
Lời giải
Đáp án đúng là: B
Trong phản ứng oxi hóa – khử, chất oxi hóa là chất nhận electron, chất khử là chất nhường electron.
Bài 15.9 trang 39 SBT Hóa học 10: Dẫn khí H2 đi qua ống sứ đựng bột CuO nung nóng để thực hiện phản ứng hóa học sau:
CuO + H2 Cu + H2O
Trong phản ứng trên, chất đóng vai trò chất khử là
A. CuO
B. Cu
C. H2
D. H2O
Lời giải
Đáp án đúng là: C
Chất khử là chất nhường electron (số oxi hóa tăng).
Chất oxi hóa là chất nhận electron (số oxi hóa giảm).
⇒ H2 là chất khử, CuO là chất oxi hóa.
Bài 15.10 trang 40 SBT Hóa học 10: Phản ứng nào sau đây là phản ứng oxi hóa – khử?
A. 2Ca + O2 2CaO
B. CaCO3 CaO + CO2
C. CaO + H2O → Ca(OH)2
D. Ca(OH)2 + CO2 → CaCO3 + H2O
Lời giải
Đáp án đúng là: A
Phản ứng:
Là phản ứng oxi hóa khử vì có xảy ra quá trình nhường, nhận electron (có sự thay đổi số oxi hóa của các chất trong phản ứng).
Thông hiểu
Bài 15.11 trang 40 SBT Hóa học 10: Cho các chất sau: Cl2, HCl, NaCl, KClO3, HClO4
Số oxi hóa của nguyên tử Cl trong phân tử các chất trên lần lượt là
A. 0; +1; +1; +5; +7
B. 0; -1; -1; +5; +7
C. 1; -1; -1; -5; -7
D. 0; 1; 1; 5; 7
Lời giải
Đáp án đúng là: B
Bài 15.12 trang 40 SBT Hóa học 10: Thuốc tím chứa ion penmanganate (MnO4-) có tính oxi hóa mạnh, được dùng để sát trùng, diệt khuẩn trong y học, đời sống và nuôi trồng thủy sản. Số oxi hóa của manganse trong ion permanganate là
A. +2
B. +3
C. +7
D. +6
Lời giải
Đáp án đúng là: C
Đặt số oxi hóa của manganse trong ion permanganate là x
Số oxi hóa của O thường là -2. Ta có:
x.1 + (-2).4 = -1 ⇒ x = +7
Bài 15.13 trang 40 SBT Hóa học 10: Cho các phân tử có công thức cấu tạo sau:
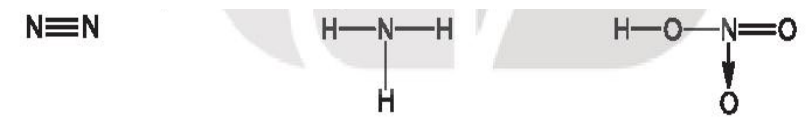
Số oxi hóa của nguyên tử N trong các phân tử trên lần lượt là
A. 0; -3; -4
B. 0; +3; +5
C. -3; -3; +4
D. 0; -3; +5
Lời giải
Đáp án đúng là: D
Bài 15.14 trang 40 SBT Hóa học 10: Carbon đóng vai trò chất oxi hóa ở phản ứng nào sau đây?
A. C + O2 CO2
B. C + CO2 2CO
C. C + H2O CO + H2
D. C + 2H2 CH4
Lời giải
Đáp án đúng là: D
Số oxi hóa của C giảm từ 0 xuống -4 trong phản ứng
C + 2H2 CH4
⇒ C là chất oxi hóa.
Bài 15.15 trang 40 SBT Hóa học 10: Thực hiện các phản ứng hóa học sau:
(a) S + O2 SO2
(b) Hg + S → HgS
(c) H2 + S H2S
(d) S + 3F2 SF6
Số phản ứng sulfur đóng vai trò chất oxi hóa là
A. 4
B. 2
C. 3
D. 1
Lời giải
Đáp án đúng là: B
Sulfur đóng vai trò chất oxi hóa trong phản ứng (b) và (c) vì có số oxi hóa giảm từ 0 xuống -2.
Bài 15.16 trang 40 SBT Hóa học 10: Khi tham gia các phản ứng đốt cháy nhiên liệu, oxygen đóng vai trò là
A. chất khử
B. acid
C. chất oxi hóa.
D. base
Lời giải
Đáp án đúng là: C
Các phản ứng đốt cháy nhiên liệu oxygen dạng O2 tạo thành H2O và CO2.
Số oxi hóa giảm từ 0 xuống -2 ⇒ Oxygen đóng vai trò là chất oxi hóa.
Bài 15.17 trang 41 SBT Hóa học 10: Chlorine vừa đóng vai trò là chất oxi hóa, vừa đóng vai trò chất khử trong phản ứng nào sau đây?
A. 2Na + Cl2 → 2NaCl
B. H2 + Cl2 → 2HCl
C. 2FeCl2 + Cl2 → 2FeCl3
D. 2NaOH + Cl2 → NaCl + NaClO + H2O
Lời giải
Đáp án đúng là: D
Số oxi hóa của chlorine vừa tăng, vừa giảm sau phản ứng:
Bài 15.18 trang 41 SBT Hóa học 10: Cho các phản ứng hóa học sau:
(a) CaCO3 CaO + CO2
(b) CH4 C + 2H2
(c) 2Al(OH)3 Al2O3 + 3H2O
(d) 2NaHCO3 Na2CO3 + CO2 + H2O
Số phản ứng có kèm theo sự thay đổi số oxi hóa của các nguyên tử là
A. 2
B. 3
C. 1
D. 4
Lời giải
Đáp án đúng là: C
Chỉ có phản ứng (b) có kèm theo sự thay đổi số oxi hóa của các nguyên tử.
Xét phản ứng đốt cháy methane trong buồng động cơ xe buýt sử dụng nhiên liệu CNG:
a) Xác định các nguyên tử có sự thay đổi số oxi hóa. Viết quá trình oxi hóa, quá trình khử.
b) Lập phương trình hóa học của phản ứng theo phương pháp thăng bằng electron.
Lời giải
a)
Chất khử: CH4
Chất oxi hóa: O2
Quá trình oxi hóa:
Quá trình khử:
b)
Xác định được hệ số của CH4 và CO2 đều là 1, hệ số của O2 là 2, sau đó cân bằng nguyên tố H tìm được hệ số của H2O là 2
CH4 + 2O2 CO2 + 2H2O
Bài 15.20 trang 41 SBT Hóa học 10: Xét phản ứng sản xuất Cl2 trong công nghiệp:
a) Xác định các nguyên tử có sự thay đổi số oxi hóa. Chỉ rõ chất oxi hóa, chất khử.
b) Lập phương trình hóa học của phản ứng theo phương pháp thăng bằng electron.
Lời giải
a)
NaCl là chất khử, H2O là chất oxi hóa.
Quá trình oxi hóa:
Quá trình khử:
b)
Xác định được hệ số của NaCl và NaOH đều là 2, hệ số của Cl2 và H2 đều là 1, sau đó cân bằng nguyên tố H tìm được hệ số của H2O là 2:
2NaCl + 2H2O 2NaOH + Cl2 + H2
Vận dụng
a) Xác định các nguyên tử có sự thay đổi số oxi hóa. Viết các quá trình oxi hóa, quá trình khử.
b) Lập phương trình hóa học của phản ứng theo phương pháp thăng bằng electron.
Lời giải
a)
Quá trình oxi hóa:
Quá trình khử:
b) Lập phương trình hóa học của phản ứng theo phương pháp thăng bằng electron:
Xác định được hệ số của ZnS, ZnO và SO2 đều là 2, hệ số của O2 là 3:
2ZnS + 3O2 2ZnO + 2SO2
a) Xác định các nguyên tố có sự thay đổi số oxi hóa. Chỉ rõ chất oxi hóa, chất khử.
b) Lập phương trình hóa học của phản ứng theo phương pháp thăng bằng electron.
Lời giải
C4H10 là chất khử, O2 là chất oxi hóa
Quá trình oxi hóa:
Quá trình khử:
b)
Xác định được hệ số của C4H10 là 2, hệ số của CO2 là 8, hệ số của O2 là 13, hệ số của H2O là 10:
2C4H10 + 13O2 8CO2 + 10H2O
FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + K2SO4 + MnSO4 + H2O
a) Lập phương trình hóa học của phản ứng theo phương pháp thăng bằng electron. Chỉ rõ chất oxi hóa, chất khử.
b) Tính thể tích dung dịch KMnO4 0,02M để phản ứng vừa đủ với 20 mL dung dịch FeSO4 0,10M.
Lời giải
a)
FeSO4 là chất khử, KMnO4 là chất oxi hóa
Quá trình oxi hóa:
Quá trình khử:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Lời giải
Lưu ý: 1 mol khí ở điều kiện chuẩn có thể tích là 24,79 L
Sơ đồ phản ứng:
Phương trình phản ứng: 2M + 2nH2SO4 → M2(SO4)n + nSO2 + 2nH2O
Theo phương trình phản ứng ta có:
⇒
Với n = 1 ⇒ MM = 9 loại
Với n = 2 ⇒ MM = 18 loại
Với n = 3 ⇒ MM = 27 (Al)
Vậy kim loại M là Al (Aluminium)
Xem thêm các bài giải SBT Hoá học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 15: Phản ứng oxi hóa - khử
Bài 17: Biến thiên enthalpy trong các phản ứng hóa học
Lý thuyết Phản ứng oxi hóa - khử
I. Số oxi hóa
1. Khái niệm
Số oxi hóa là điện tích quy ước của nguyên tử trong phân tử khi coi tất cả các electron liên kết đều chuyển hoàn toàn về nguyên tử có độ âm điện lớn hơn.
Số oxi hóa được viết ở dạng số đại số, dấu viết trước, số viết sau.
Ví dụ 1: Xét phân tử NaCl.
Nguyên tử Na nhường 1 electron cho nguyên tử Cl, khi đó nguyên tử Na trở thành ion dương mang điện tích 1+ (số oxi hóa của Na là +1) và nguyên tử Cl nhận 1 electron của nguyên tử Na trở thành ion âm mang điện tích 1– (số oxi hóa của Cl là –1): .
Ví dụ 2: Xét phân tử H2O.

Độ âm điện của nguyên tử O lớn hơn độ âm điện của nguyên tử H, nếu các cặp electron liên kết chuyển hoàn toàn về nguyên tử O thì nguyên tử O có thêm 2 electron và trở thành ion âm có điện tích 2– (số oxi hóa của O là –2); mỗi nguyên tử H mất đi 1 electron và trở thành ion dương có điện tích 1+ (số oxi hóa của H là +1): .
Ví dụ 3: Xét phân tử H2.
H : H
Do hai nguyên tử H giống nhau nên cặp electron liên kết không lệch về nguyên tử nào. Do vậy, mỗi nguyên tử H đều trung hòa điện, có điện tích bằng 0 và số oxi hóa là 0: .
2. Quy tắc xác định số oxi hóa
Thông thường, số oxi hóa của nguyên tử được xác định trực tiếp từ công thức phân tử theo các quy tắc sau:
Quy tắc 1: Trong đơn chất, số oxi hóa của nguyên tử bằng 0.
Ví dụ: .
Quy tắc 2: Trong phân tử các hợp chất, thông thường số oxi hóa của hydrogen là +1, của oxygen là – 2, các kim loại điển hình có số oxi hóa dương và có giá trị bằng số electron hóa trị.

Quy tắc 3: Trong hợp chất, tổng số oxi hóa của các nguyên tử trong phân tử bằng 0.
Quy tắc 4: Trong ion đơn nguyên tử, số oxi hóa của nguyên tử bằng điện tích ion; trong ion đa nguyên tử, tổng số oxi hóa của các nguyên tử bằng điện tích ion.
Ví dụ 1: Xác định số oxi hóa của S trong phân tử Na2SO4.
Hướng dẫn:
Trong hợp chất, số oxi hóa của Na là +1, số oxi hóa của O là –2.
Số oxi hóa của từng nguyên tử: .
Áp dụng quy tắc 3, ta có: (+1)×2 + x + (–2)×4 = 0 ® x = +6.
Ví dụ 2: Xác định số oxi hóa của C trong ion .
Hướng dẫn:
Số oxi hóa của O là – 2.
Gọi số oxi hóa của C trong ion đa nguyên tử là x.
Áp dụng quy tắc 4, ta có: x + (–2)×3 = –2 x = +4.
II. Chất oxi hóa, chất khử, phản ứng oxi hóa – khử
1. Chất oxi hóa, chất khử
Chất khử là chất nhường electron, chất oxi hóa là chất nhận electron.
Quá trình oxi hóa là quá trình chất khử nhường electron, quá trình khử là quá trình chất oxi hóa nhận electron.
Ví dụ: Đưa mẩu than gỗ nóng đỏ vào bình đựng khí O2, mẩu than cháy sáng.
Trong phản ứng trên, nguyên tử C nhường 4 electron, là chất khử; phân tử O2 nhận 4 electron, là chất oxi hóa.
(quá trình oxi hóa)
(quá trình khử)
2. Phản ứng oxi hóa – khử
Phản ứng oxi hóa – khử là phản ứng hóa học xảy ra đồng thời quá trình quá trình nhường electron và quá trình nhận electron.
Dấu hiệu để nhận biết phản ứng oxi hóa – khử là có sự thay đổi số oxi hóa của các nguyên tử.
Ví dụ: Phản ứng nào sau đây là phản ứng oxi hóa – khử?
(a) CaCO3 CaO + CO2.
(b) BaCl2 + Na2SO4 BaSO4¯ + 2NaCl.
(c) 4Al + 3O2 2Al2O3.
Hướng dẫn giải:
(a) Không phải là phản ứng oxi hóa – khử vì không có sự thay đổi số oxi hóa của các nguyên tố.
(b) Không phải là phản ứng oxi hóa – khử vì không có sự thay đổi số oxi hóa của các nguyên tố.
(c) : có sự thay đổi số oxi hóa của nguyên tố Al, O Đây là phản ứng oxi hóa – khử.
III. Lập phương trình hóa học của phản ứng oxi hóa – khử
Phương pháp thăng bằng electron đường dùng để lập phương trình hóa học của phản ứng oxi hóa – khử theo nguyên tắc: “Tổng số electron chất khử nhường bằng tổng số electron chất oxi hóa nhận”.
Ví dụ: Cân bằng phương trình hóa học của phản ứng sau theo phương pháp thăng bằng electron: NH3 + O2NO + H2O.
Bước 1: Xác định các nguyên tử có sự thay đổi số oxi hóa, từ đó xác định chất oxi hóa, chất khử:
NH3: chất khử; O2: chất oxi hóa.
Bước 2: Biểu diễn quá trình oxi hóa, quá trình khử:
Bước 3: Tìm hệ số thích hợp cho chất khử và chất oxi hóa dựa trên nguyên tắc: Tổng số electron chất khử nhường bằng tổng số electron chất oxi hóa nhận.
Bước 4: Đặt hệ số của chất oxi hóa và chất khử vào sơ đồ phản ứng, từ đó tính ra hệ số của các chất khác có mặt trong phương trình hóa học. Kiểm tra sự cân bằng số nguyên tử của các nguyên tố ở hai vế.
4NH3 + 5O2 4NO + 6H2O
IV. Phản ứng oxi hóa – khử trong thực tiễn
1. Sự cháy
Phản ứng cháy là phản ứng oxi hóa – khử xảy ra ở nhiệt độ cao giữa chất cháy và chất oxi hóa. Chất cháy thường là nhiên liệu (than đá, khí thiên nhiên, xăng dầu, …), còn chất oxi hóa thường là oxygen.
Ví dụ: Phản ứng oxi hóa – khử xảy ra khi đốt cháy carbon trong than đá và butane trong khí gas:
C + O2 CO2
2C4H10 + 13O2 8CO2 + 10H2O
2. Sự han gỉ kim loại
Sau một thời gian sử dụng, nhiều thiết bị, máy móc, vật dụng bằng kim loại thường bị han gỉ, do sự oxi hóa bởi oxygen trong không khí.
Ví dụ: Trong không khí ẩm, các vật dụng bằng thép bị oxi hóa tạo gỉ sắt.
4Fe + 3O2 + xH2O 2Fe2O3.xH2O
3. Sản xuất hóa chất
Trong công nghiệp, phần lớn các phản ứng hóa học xảy ra trong các quy trình sản xuất là phản ứng oxi hóa – khử.
Ví dụ: Sulfuric acid là hóa chất quan trọng trong công nghiệp, được sản xuất chủ yếu từ sulfur hoặc quặng pyrite.
Sơ đồ phản ứng;
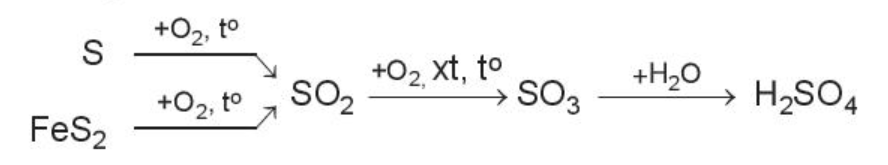
4. Chuyển hóa các chất trong tự nhiên
Trong tự nhiên cũng xảy ra rất nhiều quá trình kèm theo phản ứng oxi hóa – khử.
Ví dụ: Tia sét tạo tia lửa điện, là điều kiện cho nitrogen phản ứng với oxygen:
N2 + O2 2NO
Khí NO sinh ra nhanh chóng chuyển hóa thành NO2, sau đó tiếp tục bị oxi hóa thành HNO3:
2NO + O2 2NO2
4NO2 + O2 + 2H2O 4HNO3
Nitric acid tan vào nước mưa và chuyển hóa thành gốc nitrate () , cung cấp chất đạm cho cấy lúa. Nhờ quá trình trên, hàng năm một lượng lớn phân đạm tự nhiên được bổ sung cho đất.
5. Xác định nồng độ của một chất dựa vào phản ứng oxi hóa – khử
- Trong thực tế, dung dịch thuốc tím (KMnO4) được sử dụng phổ biến như một tác nhân oxi hóa mạnh để xác định hàm lượng các chất khử như iron(II); hydrogen peroxide, oxalic acid, …
Ví dụ: Trong quá trình bảo quản, một mẫu iron (II) sulfate bị oxi hóa một phần thành hợp chất iron (III). Hàm lượng iron (II) sulfate còn lại trong mẫu được xác định thông qua phản ứng với dung dịch thuốc tím có nồng độ đã biết:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O