Lời giải bài tập Hóa học lớp 10 Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì sách Kết nối tri thức ngắn gọn, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi Hóa học 10 Bài 7 từ đó học tốt môn Hóa 10.
Giải bài tập Hóa học lớp 10 Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì
Video giải Hóa học 10 Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì - Kết nối tri thức
Giải hóa học 10 trang 40 Kết nối tri thức
Phương pháp giải:
Khi đi từ trái sang phải, đầu chu kì là một kim loại mạnh, kết thúc chu kì là một phi kim mạnh
=> Các nguyên tố nhóm A trong hợp chất với oxide và hydroxide biến đổi tuần hoàn. Tính base của oxide và hydroxide tương ứng giảm dần và tính acid của chúng tăng dần.
Lời giải:
- Đầu chu kì là một kim loại mạnh => tạo oxide có tính base và hydroxide mạnh.
- Kết thúc chu kì là một phi kim mạnh => tạo oxide có tính acid và acid mạnh ( hydroxide yếu)
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide tương ứng giảm dần và tính acid của chúng tăng dần.
I. Thành phần của các Oxide và Hydroxide
Phương pháp giải:
- Công thức tổng quát của 1 nguyên tố ( có hóa trị cao nhất) trong hợp chất oxide có dạng: M2On – với n là hóa trị cao nhất của nguyên tố M.
- Công thức tổng quát của 1 nguyên tố ( có hóa trị cao nhất) trong hợp chất oxide có dạng: M(OH)n – với n là hóa trị cao nhất của nguyên tố M.
Lời giải:
- Công thức tổng quát của oxide M2On - với n là hóa trị cao nhất của nguyên tố M.
- Công thức tổng quát của oxide M(OH)n - với n là hóa trị cao nhất của nguyên tố M.
- Gallium thuộc thuộc nhóm IIIA => Ga có hóa trị III
=> Công thức hóa học của oxide là Ga2O3
- Công thức hóa học của hydroxide là Ga(OH)3
- Selenium thuộc thuộc nhóm VIA => Se có hóa trị VI
=> Công thức hóa học của oxide là SeO3
- Công thức hóa học của hydroxide là H2SeO4
Giải hóa học 10 trang 42 Kết nối tri thức
II. Tính chất của Oxide và Hydroxide
Câu 2 trang 42 Hóa học 10: Trong các chất dưới đây, chất nào có tính acid yếu nhất
A. H2SO4
B. HClO4
C. H3PO4
D. H2SiO3
Phương pháp giải:
Các nguyên tố trong các hợp chất acid đã cho thuộc cùng 1 chu kì. Trong 1 chu kì, theo chiều tăng của điện tích hạt nhân, tính acid tăng dần.
Lời giải:
|
Tên nguyên tố |
Si |
P |
S |
Cl |
|
Z |
14 |
15 |
16 |
17 |
Trong một chu kì, tính acid của các hydroxide tăng dần theo chiều tăng dần của điện tích hạt nhân.
=> Đáp án B
Câu 3 trang 42 Hóa học 10: Dãy gồm các chất có tính base tăng dần là
A. Al(OH)3, Mg(OH)2, NaOH
B. NaOH, Mg(OH)2, Al(OH)3
C. Mg(OH)2, Al(OH)3, NaOH
D. Al(OH)3, NaOH, Mg(OH)2
Phương pháp giải:
Các nguyên tố trong các hợp chất base đã cho thuộc cùng 1 chu kì. Trong 1 chu kì, theo chiều tăng của điện tích hạt nhân, tính base giảm dần.
Lời giải:
|
Tên nguyên tố |
Na |
Mg |
Al |
|
Z |
11 |
12 |
13 |
Trong một chu kì, tính base của các hydroxide giảm dần theo chiều tăng dần của điện tích hạt nhân.
=> Đáp án A
A. Tính kim loại và phi kim
B. Tính acid – base của các hydroxide
C. Khối lượng nguyên tử.
D. Cấu hình electron lớp ngoài cùng của nguyên tử.
Phương pháp giải:
Những đại lượng và tính chất của nguyên tố hóa học biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân:
+ Tính kim loại và phi kim
+ Tính acid – base của các hydroxide
+ Cấu hình electron lớp ngoài cùng
Lời giải:
Các đại lượng biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân:
+ Tính kim loại và phi kim
+ Tính acid – base của các hydroxide
+ Cấu hình electron lớp ngoài cùng
=> Đáp án C
Lý thuyết Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì
I. Thành phần của các oxide và hydroxide
Hóa trị cao nhất của các nguyên tố nhóm A trong hợp chất với oxygen tăng từ I đến VII khi đi từ trái qua phải trong một chu kì (trừ chu kì 1 và nguyên tố fluorine ở chu kì 2), do đó thành phần của các oxide và hydroxide có sự lặp lại theo chu kì.
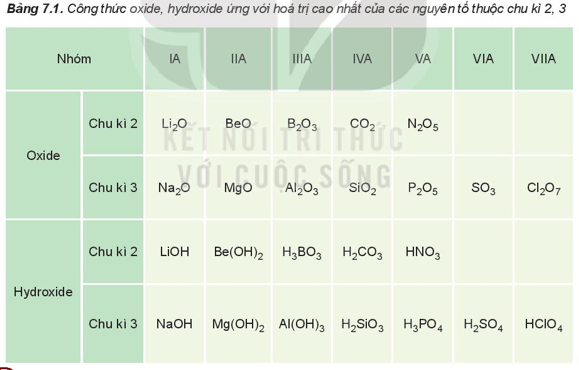
Ví dụ: Nguyên tố calcium thuộc nhóm IIA của bảng tuần hoàn. Viết công thức hóa học của oxide, hydroxide (ứng với hóa trị cao nhất) của nguyên tố trên.
Hướng dẫn giải:
Nguyên tố calcium (Ca) thuộc nhóm IIA.
Hóa trị cao nhất của Ca là II.
Công thức hóa học của oxide là CaO, của hydroxide là Ca(OH)2.
II. Tính chất của oxide và hydroxide
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide tương ứng giảm dần, đồng thời tính acid của chúng tăng dần.
Nhận xét:
Hydroxide của các nguyên tố nhóm IA thể hiện tính base mạnh, hydroxide ứng với hóa trị cao nhất của các nguyên tố nhóm VIIA (trừ fluorine) thể hiện tính acid mạnh.
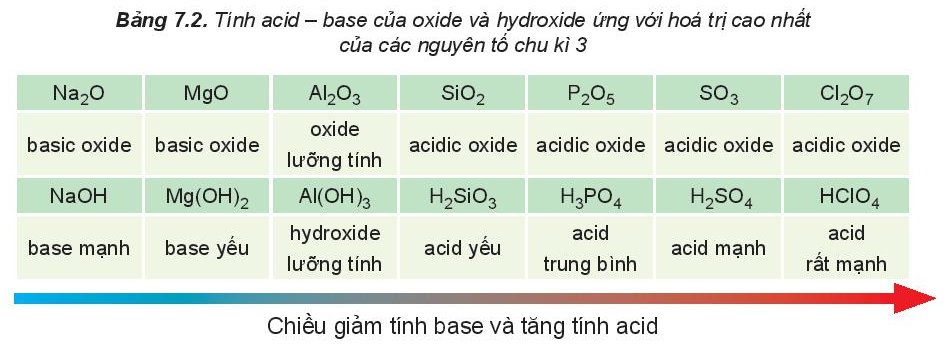
Ví dụ: Cho các nguyên tố P (Z = 15), S (Z = 16), Cl (Z = 17). So sánh tính acid của hydroxide (ứng với hóa trị cao nhất) của các nguyên tố trên.
Hướng dẫn giải:
P (Z = 15): [Ne]3s23p3 P thuộc chu kì 3, nhóm VA.
Hóa trị cao nhất của P là V Công thức hydroxide (ứng với hóa trị cao nhất) là H3PO4.
S (Z = 16): [Ne]3s23p4 S thuộc chu kì 3, nhóm VIA.
Hóa trị cao nhất của S là VI Công thức hydroxide (ứng với hóa trị cao nhất) là H2SO4.
Cl (Z = 17): [Ne]3s23p5 Cl thuộc chu kì 3, nhóm VA.
Hóa trị cao nhất của Cl là VII Công thức hydroxide (ứng với hóa trị cao nhất) là HClO4.
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide tương ứng giảm dần, đồng thời tính acid của chúng tăng dần.
So sánh tính acid: H3PO4 < H2SO4 < HClO4.
Bài giảng Hóa học 10 Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì - Kết nối tri thức
Xem thêm các bài giải SGK Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 7: Xu hướng biến đổi thành phần và một số tính chất của hợp chất trong một chu kì
Bài 8: Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học