Lời giải bài tập Hóa học lớp 10 Bài 9: Ôn tập chương 2 sách Kết nối tri thức ngắn gọn, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi Hóa học 10 Bài 9 từ đó học tốt môn Hóa 10.
Giải bài tập Hóa học lớp 10 Bài 9: Ôn tập chương 2
I. Hệ thống hóa kiến thức
Giải hóa học 10 trang 46 Kết nối tri thức
II. Luyện tập

Có các nhận xét sau:
(1) Thứ tự giảm dần tính kim loại Y, E, X.
(2) Thứ tự tăng dần độ âm điện là Y, X, Z, T.
(3) Thứ tự giảm dần tính phi kim là T, Z, Q.
(4) Thứ tự giảm dần bán kính nguyên tử là Y, E, X, T.
Số nhận xét đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Phương pháp giải:
- Tính chất và các đại lượng biến đổi tuần hoàn theo chu kì và nhóm.
- Trong một chu kì, tính kim loại giảm và bán kình nguyên tử giảm dần theo chiều tăng dần điện tích hạt nhân.
- Trong một nhóm, tính phi kim giảm theo chiều tăng dần điện tích hạt nhân.
- Độ âm điện giảm dần trong một nhóm và tăng dần trong một chu kì.
Lời giải:
(1) Thứ tự giảm dần tính kim loại Y, E, X. => Đúng
(2) Thứ tự tăng dần độ âm điện là Y, X, Z, T. => Đúng
(3) Thứ tự giảm dần tính phi kim là T, Z, Q. => Đúng
(4) Thứ tự giảm dần bán kính nguyên tử là Y, E, X, T. => Đúng
Đáp án D.
Giải hóa học 10 trang 47 Kết nối tri thức
(1) Nguyên tử S có 3 lớp electron và có 10 electron p.
(2) Nguyên tử S có 5 electron hóa trị và 6 electron s.
(3) Công thức oxide cao nhất của S có dạng SO3 và là acidic oxide.
(4) Nguyên tố S có tính phi kim mạnh hơn so với nguyên tố có số hiệu nguyên tử là 8.
(5) Hydroxide cao nhất của S có dạng H2SO4 và có tính acid.
Số phát biểu đúng là
A. 2.
B. 3.
C. 4.
D. 5.
Phương pháp giải:
Chu kì 3 => có 3 lớp electron
Nhóm VIA => có 6 electron lớp ngoài cùng (6 electron hóa trị)
=> Cấu hình electron của S: 1s22s22p63s23p4; Z = 16
=> Có 10 electron p.
- S thuộc nhóm VIA, nguyên tố p nên oxide và hydroxide có tính acid. Công thức oxide cao nhất là SO3, hydroxide cao nhất là H2SO4.
- Tính phi kim trong một nhóm giảm dần => Tính phi kim của S yếu hơn nguyên tố có Z = 8
Lời giải:
(1) Nguyên tử S có 3 lớp electron và có 10 electron p. => Đ
(2) Nguyên tử S có 5 electron hóa trị và 6 electron s. => S
(3) Công thức oxide cao nhất của S có dạng SO3 và là acidic oxide. => Đ
(4) Nguyên tố S có tính phi kim mạnh hơn so với nguyên tố có số hiệu nguyên tử là 8. => S
(5) Hydroxide cao nhất của S có dạng H2SO4 và có tính acid. =>Đ
Đáp án B
(1) X và Y thuộc 2 nhóm A kế tiếp nhau.
(2) X là kim loại, Y là phi kim
(3) X2O3 là basic oxide và YO3 là acidic oxid.
(4) Hydroxide cao nhất của Y có dạng Y(OH)6 và có tính baso.
Số phát biểu đúng là:
A. 2.
B. 3.
C. 4.
D. 1.
Phương pháp giải:
- Từ công thức oxide cao nhất => thứ tự nhóm của X và Y.
Lời giải:
- Oxide cao nhất của X và Y có dạng XO và YO3
=> X thuộc nhóm IIA, Y thuộc nhóm VIA
Các nguyên tố nhóm IIA thường là kim loại và VIA thường là phi kim
- Trong hợp chất X2O3, X có hóa trị III => trái với giả thiết
- Y là phi kim nên hydroxide cao nhất của Y có tính acid.
(1) X và Y thuộc 2 nhóm A kế tiếp nhau. => S
(2) X là kim loại, Y là phi kim. => Đ
(3) X2O3 là basic oxide và YO3 là acidic oxid. => S
(4) Hydroxide cao nhất của Y có dạng Y(OH)6 và có tính baso. => S
Đáp án D.
a) Nêu vị trí trong bảng tuần hoàn của mỗi nguyên tố có trong thành phần của borax và viết cấu hình electron của nguyên tử các nguyên tố đó.
b) Sắp xếp các nguyên tố trên theo chiều bán kính nguyên tử tăng dần.
c) Sắp xếp các nguyên tố trên theo chiều độ âm điện giảm dần.
Giải thích dựa vào quy luật biến thiên trong bảng tuần hoàn.
Phương pháp giải:
a) Trong borax gồm nguyên tố Na, B, O, H.
b) Bán kính tăng dần trong một nhóm và giảm dần trong một chu kì.
c) Độ âm điện giảm dần trong một nhóm và tăng dần trong một chu kì
Lời giải:
a)
Na nằm ở ô số 11, chu kì 3, nhóm IA, có cấu hình electron 1s22s22p63s1
B nằm ở ô số 5, chu kì 2, nhóm IIIA, có cấu hình electron 1s22s22p1
O nằm ở ô số 8, chu kì 2, nhóm VIA, có cấu hình electron 1s22s22p4
H nằm ở ô số 1, chu kì 1, nhóm IA, có cấu hình electron 1s1
b)
Trong chu kì 2 gồm các nguyên tố Li, B, O => bán kính nguyên tử O < B < Li
Trong nhóm IA gồm các nguyên tố H, Li, Na => Bán kính nguyên tử H < Li < Na
=> Các nguyên tố theo chiều bán kính nguyên tử tăng dần là H, O, B, Na.
c)
Trong chu kì 2 gồm các nguyên tố Li, B, O => độ âm điện O > B > Li
Trong nhóm IA gồm các nguyên tố H, Li, Na => độ âm điện H > Li > Na
=> Các nguyên tố theo chiều độ âm điện giảm dần là O, H, B, Na.
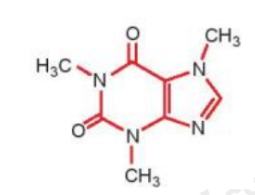
a) Nêu vị trí của các nguyên tố tạo nên cafein trong bảng tuần hoàn.
b) So sánh tính phi kim, bán kính nguyên tử và độ âm điện của các nguyên tố đó và giải thích.
Phương pháp giải:
a) Các nguyên tố tạo nên cafein gồm; N, C, H, O
b)
- Bán kính tăng dần trong một nhóm và giảm dần trong một chu kì.
- Độ âm điện giảm dần trong một nhóm và tăng dần trong một chu kì.
- Tính phi kim giảm dần trong một nhóm và tăng dần trong một chu kì.
- Do H nằm ở một chu kì khác nên dựa vào sự biến đổi trong nhóm I, có nguyên tố Li để làm yếu tố trung gian.
Lời giải:
a)
Nguyên tố H nằm ở ô số 1, chu kì 1, nhóm IA trong bảng tuần hoàn.
Nguyên tố C nằm ở ô số 6, chu kì 2, nhóm IVA trong bảng tuần hoàn.
Nguyên tố N nằm ở ô số 7, chu kì 2, nhóm VA trong bảng tuần hoàn.
Nguyên tố O nằm ở ô số 8, chu kì 2, nhóm VIA trong bảng tuần hoàn.
b)
- Tính phi kim
Trong nhóm IA, tính phi kim giảm dần => tính phi kim H > Li
Trong chu kì 2, tính phi kim tăng dần => O > N > C > Li
=> Tính phi kim của các nguyên tố giảm dần theo thứ tự O, N, C, H
- Bán kính nguyên tử
Trong nhóm IA, bán kính nguyên tử tăng dần => bán kính nguyên tử H < Li
Trong chu kì 2, bán kính nguyên tử giảm dần => O < N < C < Li
=> Bán kính nguyên tử của các nguyên tố tăng dần theo thứ tự H, O, N, C
- Độ âm điện
Trong nhóm IA, độ âm điện giảm dần => độ âm điện H > Li
Trong chu kì 2, độ âm điện tăng dần => O > N > C > Li
=> Độ âm điện của các nguyên tố giảm dần theo thứ tự O > N > C > H
a) Viết cấu hình electron, từ đó xác định vị trí của hai nguyên tố A và B trong bảng tuần hoàn.
b) So sánh tính chất hóa học của A với B và giải thích
Phương pháp giải:
a) Tổng điện số đơn vị điện tích hạt nhân của A và B là 25 => ZA + ZB = 25.
=> Biện luận ZA và ZB chỉ hơn kém nhau 1 đơn vị.
b) Sự biến đổi tính chất hóa học trong một chu kì: tính acid tăng và base giảm.
Lời giải:
a)
Theo giải thiết ta có ZA + ZB = 25
Giả sử ZA > ZB => ZA = ZB + 1
Ta có ZB + 1 + ZB = 25
=> ZB = 12 => ZA = 13
- Cấu hình electron của nguyên tố B (Z = 12): 1s22s22p63s2. B nằm ở ô số 12, chu kì 3, nhóm IIA.
- Cấu hình electron của nguyên tố A (Z = 13): 1s22s22p63s23p1. A nằm ở ô số 13, chu kì 3, nhóm IIIA.
b) Do B và A nằm trong cùng một chu kì, ZB < ZA => Tính kim loại của B mạnh hơn A
Bài giảng Hóa học 10 Bài 9: Ôn tập chương 2 - Kết nối tri thức
Xem thêm các bài giải SGK Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 8: Định luật tuần hoàn. Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học