Với Giải hóa học lớp 10 trang 89 Chân trời sáng tạo chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải hóa học 10 trang 89 Chân trời sáng tạo
Câu hỏi 2 trang 89 Hóa học 10: Tính biến thiên enthalpy của phản ứng dựa vào năng lượng liên kết phải viết được công thức cấu tạo của tất cả các chất trong phản ứng để xác định số lượng và loại liên kết. Xác định số lượng mỗi loại liên kết trong các phân tử sau: CH4, CH3Cl, NH3, CO2.
Phương pháp giải:
- Viết công thức cấu tạo của các chất
=> Xác định được các loại liên kết
Lời giải:
- CH4:
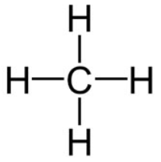
=> Có 4 liên kết C-H
- CH3Cl:
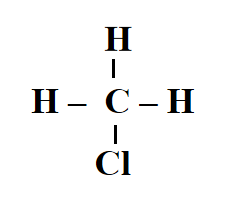
=> Có 3 liên kết C-H, 1 liên kết C-Cl
- NH3
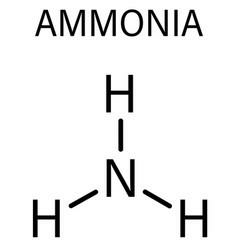
=> Có 3 liên kết N-H
- CO2
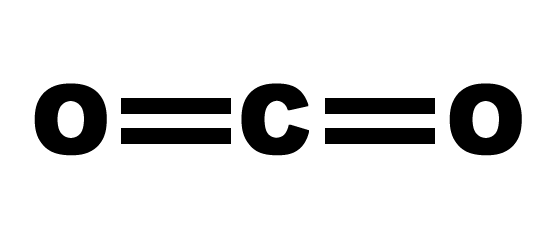
=> Có 2 liên kết C=O
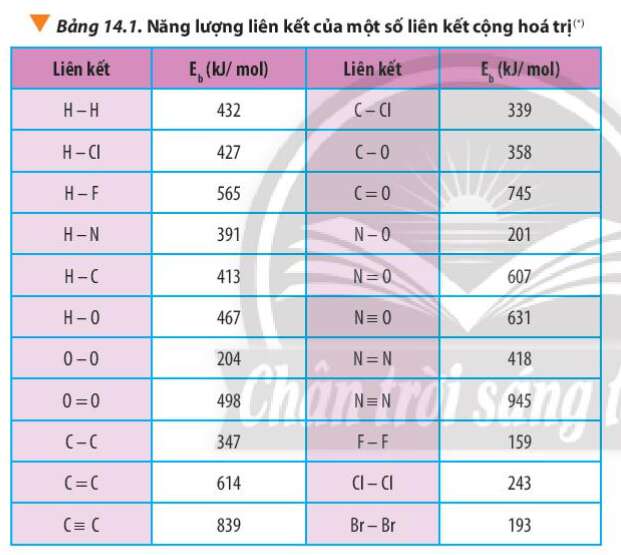
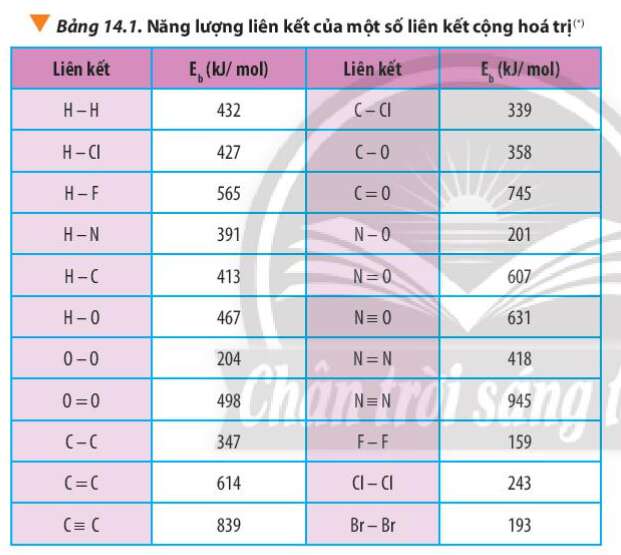
Câu hỏi 3 trang 89 Hóa học 10: Dựa vào năng lượng liên kết ở Bảng 14.1, tính biến thiên enthalpy của phản ứng và giải thích vì sao nitrogen (NN) chỉ phản ứng với oxygen (O=O) ở nhiệt độ cao hoặc có tia lửa điện để tạo thành nitrogen monoxide (N=O).
N2(g) + O2(g) 2NO(g)
Phương pháp giải:
= Eb(cđ) - Eb(sp)
Lời giải:
N2(g) + O2(g) 2NO(g)
=> Phản ứng trên có 1 liên kết NN, 1 liên kết O=O và 2 liên kết N=O
Ta có:
+ N2 có 1 liên kết NN với Eb = 945 kJ/mol
+ O2 có 1 liên kết O=O với Eb = 498 kJ/mol
+ NO có 1 liên kết N=O với Eb = 607 kJ/mol
Mà: = Eb(cđ) - Eb(sp)
=> = Eb(N2) + Eb(O2) – 2Eb(NO) = 945 + 498 – 2. 607 = 229 kJ/mol > 0
=> Phản ứng thu nhiệt
=> Để phản ứng xảy ra, cần cung cấp lượng nhiệt lớn 229 kJ/mol
=> Nitrogen chỉ phản ứng với oxygen khi ở nhiệt độ cao hoặc có tia lửa điện để tạo thành NO
Luyện tập trang 89 Hóa học 10: Xác định của phản ứng sau dựa vào giá trị Eb ở Bảng 14.1:
CH4(g) + Cl2(g) CH3Cl(g) + HCl(g)
Hãy cho biết phản ứng trên tỏa nhiệt hay thu nhiệt?
Phương pháp giải:
Bước 1: Xác định số lượng liên kết và loại liên kết của các chất trong phản ứng
Bước 2: Áp dụng công thức: = Eb(cđ) - Eb(sp)
=> Phản ứng thu nhiệt hay tỏa nhiệt
Lời giải:
CH4(g) + Cl2(g) CH3Cl(g) + HCl(g)
- Chất đầu:
+ CH4 có 4 liên kết C-H
+ Cl2 có 1 liên kết Cl-Cl
- Sản phẩm
+ CH3Cl có 3 liên kết C-H, 1 liên kết C-Cl
+ HCl có 1 liên kết H-Cl
Mà: = Eb(cđ) - Eb(sp)
=> = Eb(CH4) + Eb(Cl2) – Eb(CH3Cl)- Eb(HCl)
= 4 Eb(C-H) + Eb(Cl-Cl) – 3Eb(C-H) - Eb(C-Cl) - Eb(H-Cl)
= 4.413 + 243 – 3. 413 – 339 - 427 = -110 kJ/mol < 0
=> Phản ứng tỏa nhiệt
Xem thêm các bài giải Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác: