Với lời giải SBT Hóa học 11 trang 30 chi tiết trong Bài 7: Sulfuric acid và muối sulfate sách Chân trời sáng tạo giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 7: Sulfuric acid và muối sulfate
Bài 7.11 trang 30 SBT Hóa học 11: Cho các dung dịch không màu của mỗi chất sau đây chứa trong các lọ mất nhãn riêng biệt: Na2CO3, MgSO4, KNO3, NaOH, HCl. Hãy trình bày cách phân biệt các dung dịch đã cho bằng phương pháp hóa học. Viết phương trình hoá học của các phản ứng xảy ra.
Lời giải:
Đánh số thứ tự cho từng dung dịch, trích mẫu thử sang ống nghiệm đánh số tương ứng.
- Cho lần lượt từng mẫu thử tác dụng với dung dịch H2SO4:
+ Mẫu thử xuất hiện bọt khí là Na2CO3:
+ Mẫu thử không có hiện tượng là MgSO4, KNO3, NaOH, HCl.
- Cho lần lượt từng mẫu thử không hiện tượng ở trên tác dụng với dung dịch Ba(NO3)2:
+ Mẫu thử xuất hiện kết tủa trắng là MgSO4:
+ Mẫu thử không có hiện tượng là KNO3, NaOH, HCl.
- Nhúng quỳ tím vào nhóm mẫu thử không hiện tượng (KNO3, NaOH, HCl):
+ Mẫu thử không hiện tượng là KNO3.
+ Mẫu thử làm quỳ tím hóa xanh là NaOH.
+ Mẫu thử làm quỳ tím hóa đỏ là HCl.
Bài 7.12* trang 30 SBT Hóa học 11: Đặt hai cốc (A) và (B) có khối lượng bằng nhau lên hai đĩa cân thấy cân thăng bằng. Cho 15,9 gam Na2CO3 vào cốc (A) và 17,73 gam CaCO3 vào cốc (B), sau đó thêm 18 gam dung dịch H2SO4 98% vào cốc (A) và m gam dung dịch HCl 14,6% vào cốc (B) thì thấy cân thăng bằng. Tính khối lượng dung dịch HCl đã cho vào cốc (B).
Lời giải:
- Xét cốc (A):
Ta có:
=> H2SO4 dư, Na2CO3 hết. CO2 tính theo Na2CO3.
- Xét cốc (B):
Ta có:
+) Trường hợp (1): CaCO3 hết, HCl dư.
→ loại trường hợp CaCO3 hết, HCl dư.
+) Trường hợp (2): CaCO3 dư, HCl hết.
Đặt
Bài 7.13* trang 30 SBT Hóa học 11: Đặt hai cốc (A), (B) có cùng khối lượng lên hai đĩa cân thấy cân thăng bằng. Cho vào cốc (A) 102 gam AgNO3 dạng rắn; cốc (B) 124,2 gam K2CO3 dạng rắn.
a) Thêm 100 gam dung dịch HCl 29,2% vào cốc (A); 100 gam dung dịch H2SO4 24,5% vào cốc (B). Phải thêm bao nhiêu gam nước vào cốc (A) (hay cốc B) để cân trở lại thăng bằng?
b) Sau khi cân đã thăng bằng, lấy một nửa lượng dung dịch có trong cốc (A) cho vào cốc (B). Sau phản ứng, phải thêm bao nhiêu gam nước vào cốc (A) để cân trở lại thăng bằng?
Lời giải:
a)
Xét cốc (A):
Xét cốc (B):
Ta có:
=> H2SO4 hết, K2CO3 dư. CO2 tính theo H2SO4.
Ta thấy m(A) < m(B), để cân trở lại thăng bằng, ta cần thêm nước vào cốc (A).
b) – Xét cốc (A):
Ta có:
=> AgNO3 hết, HCl dư. AgCl tính theo AgNO3.
=> Khối lượng của cốc (A) sau khi lấy một nửa lượng dung dịch có trong cốc (A):
- Xét cốc (B):
Khi trộn một nửa dung dịch (A) phản ứng với dung dịch trong cốc (B), sẽ xảy ra phản ứng:
Ta thấy:
dư, H+ hết
tính theo H+
=> Khối lượng nước phải thêm vào cốc (A) để cân trở lại thăng bằng:
Bài 7.14* trang 30 SBT Hóa học 11: Bảng dưới đây cho biết độ tan của ba muối trong nước ở những nhiệt độ khác nhau:
a) Vẽ đồ thị biểu diễn độ tan của ba muối theo nhiệt độ.
|
Nhiệt độ của nước (oC)
|
Độ tan (gam/100 gam nước)
|
|
Na2CO3
|
NH4Cl
|
K2SO4
|
|
0
|
7,1
|
29,70
|
7,33
|
|
20
|
21,40
|
37,56
|
11,11
|
|
40
|
48,50
|
46,00
|
14,97
|
|
60
|
46,50
|
53,30
|
18,20
|
|
80
|
45,80
|
65,60
|
21,29
|
|
100
|
45,50
|
77,30
|
24,10
|
b) Độ tan của các chất rắn trong nước thường tăng theo nhiệt độ. Có nhận xét gì về độ tan của ba chất? Chất có độ tan lớn là ở nhiệt độ nào?
c) Chất nào có độ tan lớn nhất ở 30 °C và 90 °C?
Lời giải:
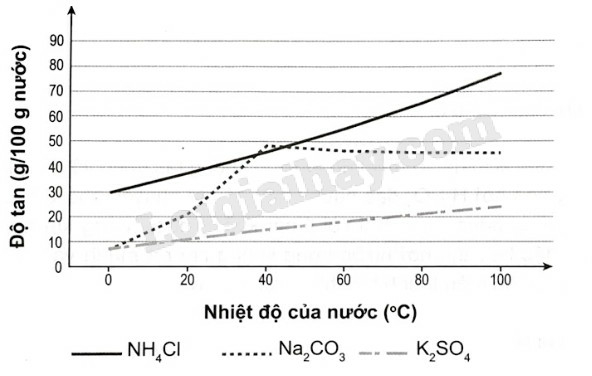
b) Độ tan của các muối tăng theo nhiệt độ. Trong đó, độ tan của NH4Cl tăng nhanh, độ tan của K2SO4 tăng chậm khi nhiệt độ tăng.
Độ tan của muối Na2CO3 tăng khi nhiệt độ tăng đến khoảng 40 °C. Sau đó độ tan của Na2CO3 lại bị giảm khi nhiệt độ tăng từ 40 °C đến 100 °C.
Chất có độ tan lớn nhất là NH4Cl, ở nhiệt độ 100 °C có độ tan là 77,30 g/100 g H2O.
c) Chất có độ tan lớn nhất: ở 30 °C là NH4Cl, ở 90 °C là NH4Cl.
Xem thêm lời giải Sách bài tập Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Bài 7.1 trang 28 SBT Hóa học 11: Kim loại nào sau đây không tác dụng với dung dịch H2SO4 loãng?...
Bài 7.2 trang 28 SBT Hóa học 11: Dãy kim loại nào trong các dãy sau đây gồm các kim loại không tác dụng với dung dịch H2SO4 đặc, nguội?...
Bài 7.3 trang 28 SBT Hóa học 11: Dung dịch sulfuric acid đặc khác dung dịch sulfuric acid loãng ở tính chất hoá học nào?...
Bài 7.4 trang 28 SBT Hóa học 11: Cách pha loãng dung dịch H2SO4 đặc nào sau đây đúng?...
Bài 7.5 trang 28 SBT Hóa học 11: Người ta thường dùng các bình bằng thép để đựng và chuyên chở dung dịch H2SO4 đặc vì...
Bài 7.6 trang 29 SBT Hóa học 11: Hỗn hợp (X) gồm Mg và Fe2O3 có khối lượng 20 gam tan hết trong dung dịch H2SO4 loãng thoát ra a L khí H2 (đkc) và tạo thành dung dịch (Y). Thêm dung dịch NaOH dư vào dung dịch (Y) và lọc kết tủa, tách ra nung đến khối lượng không đổi thu được 28 gam chất rắn. Phần trăm khối lượng Mg trong hỗn hợp (X) là...
Bài 7.7 trang 29 SBT Hóa học 11: Bình đựng dung dịch H2SO4 đặc để trong không khí ẩm lâu ngày thì khối lượng bình có thay đổi không? Vì sao?...
Bài 7.8 trang 29 SBT Hóa học 11: Trong lúc làm thí nghiệm, do bất cẩn nên một học sinh bị dung dịch H2SO4 đặc rơi lên tay. Hãy nêu biện pháp xử lí trong tình huống này trước khi đưa học sinh đến cơ sở y tế gần nhất...
Bài 7.9 trang 29 SBT Hóa học 11: Sulfuric acid là hoá chất hàng đầu trong nhiều ngành sản xuất, được mệnh danh là “máu” của các ngành công nghiệp. Trong công nghiệp, sulfuric acid được sản xuất bằng phương pháp tiếp xúc. Phương pháp này gồm 3 công đoạn chính: sản xuất SO2 → sản xuất SO3 → sản xuất H2SO4. Trong công đoạn sản xuất SO3 từ SO2 để thực hiện cần có điều kiện phản ứng thích hợp. Hãy cho biết điều kiện của phản ứng trên là gì? Biết rằng trong tự nhiên cũng có một lượng sulfuric acid sinh ra theo các công đoạn trên. Hãy giải thích quá trình hình thành...
Bài 7.10 trang 29 SBT Hóa học 11: Sơ đồ quy trình dưới đây mô tả các bước trong quá trình sản xuất phân bón (Z). Hãy xác định các chất (A), (Q), (X), (Y), (Z). Viết các phản ứng hoá học xảy ra...
Bài 7.11 trang 30 SBT Hóa học 11: Cho các dung dịch không màu của mỗi chất sau đây chứa trong các lọ mất nhãn riêng biệt: Na2CO3, MgSO4, KNO3, NaOH, HCl. Hãy trình bày cách phân biệt các dung dịch đã cho bằng phương pháp hóa học. Viết phương trình hoá học của các phản ứng xảy ra...
Bài 7.12* trang 30 SBT Hóa học 11: Đặt hai cốc (A) và (B) có khối lượng bằng nhau lên hai đĩa cân thấy cân thăng bằng. Cho 15,9 gam Na2CO3 vào cốc (A) và 17,73 gam CaCO3 vào cốc (B), sau đó thêm 18 gam dung dịch H2SO4 98% vào cốc (A) và m gam dung dịch HCl 14,6% vào cốc (B) thì thấy cân thăng bằng. Tính khối lượng dung dịch HCl đã cho vào cốc (B)...
Bài 7.13* trang 30 SBT Hóa học 11: Đặt hai cốc (A), (B) có cùng khối lượng lên hai đĩa cân thấy cân thăng bằng. Cho vào cốc (A) 102 gam AgNO3 dạng rắn; cốc (B) 124,2 gam K2CO3 dạng rắn...
Bài 7.14* trang 30 SBT Hóa học 11: Bảng dưới đây cho biết độ tan của ba muối trong nước ở những nhiệt độ khác nhau:...
Xem thêm các bài giải SBT Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Bài 6: Sulfur và sulfur dioxide
Bài 7: Sulfuric acid và muối sulfate
Ôn tập chương 2
