Với lời giải SBT Hóa học 11 trang 13 chi tiết trong Bài 2: Cân bằng trong dung dịch nước sách Chân trời sáng tạo giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 2: Cân bằng trong dung dịch nước
Bài 2.15 trang 13 SBT Hóa học 11: a) Tính pH của dung dịch có nồng độ ion H+ là 4,2×10-10 M
b) Tính nồng độ mol của ion H+ trong dung dịch có pH = 6,35.
c) Tính pH của dung dịch có nồng độ ion OH- là 4,0×10-11 M.
Lời giải:
a) [H+] = 4,2×10-10 (M)
=> pH = -lg(4,2×10-10) = 9,38
b)
c)
Bài 2.16 trang 13 SBT Hóa học 11: Cho 10 mL dung dịch HCl có pH = 3. Hãy đề nghị cách pha dung dịch có pH = 4 từ dung dịch trên.
Lời giải:
Gọi a (L) là thể tích nước cần pha.
Ta có:
Với
Mặt khác:
Cách pha: Đong 90 mL nước cất rồi cho vào bình đựng 10 mL dung dịch HCl có pH = 3, dùng đũa thủy tinh khuấy đều dung dịch. Ta thu được 100 mL dung dịch HCl có pH = 4.
Bài 2.17 trang 13 SBT Hóa học 11: Vì sao người ta không sử dụng dung dịch acid HNO3 trong phương pháp chuẩn độ acid – base?
Lời giải:
Người ta không sử dụng dung dịch acid HNO3 trong phương pháp chuẩn độ acid – base vì:
+ Acid HNO3 không bền, khi có ánh sáng dễ bị phân hủy, làm sai lệch nồng độ HNO3 ban đầu, dẫn tới sai lệch kết quả phân tích khi chuẩn độ.
+ Khi phản ứng với base, HNO3 có thể oxi hóa một số ion kim loại tạo thành các sản phẩm phức tạp khó xác định, gây ảnh hưởng đến độ chính xác của phép chuẩn độ.
Bài 2.18 trang 13 SBT Hóa học 11: Trộn 3 dung dịch H2SO4 0,1 M, HNO3 0,2 M và HCl 0,3 M với thể tích bằng nhau thu được dung dịch (A). Lấy 300 mL dung dịch (A) cho tác dụng với một dung dịch (B) gồm NaOH 0,20 M và KOH 0,29 M. Tính thể tích dung dịch (B) cần dùng để sau khi tác dụng với 300 mL dung dịch (A) thu được dung dịch có pH = 2.
Lời giải:
Bảo toàn nguyên tố H, ta có:
Gọi V là thể tích dung dịch B, ta có:
Dung dịch sau phản ứng có
=> H+ dư, OH- hết.
Phương trình:
0,49V ← 0,49V
Mặt khác:
Bài 2.19 trang 13 SBT Hóa học 11: Để chuẩn độ 40 mL dung dịch HCl chưa biết nồng độ đã dùng trung bình hết 34 mL dung dịch NaOH 0,12 M. Tính nồng độ mol của dung dịch HCl.
Lời giải:
VHCl = 40 (mL); CNaOH = 0,12 (M); VNaOH = 34 (mL)
Bài 2.20 trang 13 SBT Hóa học 11: Để chuẩn độ 50 mL dung dịch CH3COOH chưa biết nồng độ đã dùng trung bình hết 75 mL dung dịch NaOH 0,05 M. Tính nồng độ mol của dung dịch CH3COOH.
Lời giải:
Bài 2.21 trang 13 SBT Hóa học 11: Trong phương pháp chuẩn độ acid – base, xung quanh điểm tương đương có một sự thay đổi pH đột ngột gọi là bước nhảy chuẩn độ. Đường biểu diễn trên đồ thị chuẩn độ acid – base gọi là đường định phân. Từ các số liệu sau đây, hãy vẽ đồ thị biểu diễn sự biến thiên pH của dung dịch trong quá trình chuẩn độ dung dịch HCl bằng dung dịch chuẩn NaOH 0,100 M. Trục hoành ghi thể tích dung dịch NaOH, trục tung ghi pH của dung dịch. Xác định giá trị điểm tương đương và khoảng bước nhảy chuẩn độ của quá trình này.
|
VNaOH (mL)
|
Giá trị pH
|
VNaOH (mL)
|
Giá trị pH
|
|
0,0
|
1,00
|
25,1
|
10,30
|
|
5,0
|
1,18
|
25,5
|
11,00
|
|
10,0
|
1,37
|
26,0
|
11,29
|
|
15,0
|
1,60
|
28,0
|
11,75
|
|
20,0
|
1,95
|
30,0
|
11,96
|
|
22,0
|
2,20
|
35,0
|
12,22
|
|
24,0
|
2,69
|
40,0
|
12,36
|
|
24,5
|
3,00
|
45,0
|
12,46
|
|
24,9
|
3,70
|
50,0
|
12,52
|
|
25,0
|
7,00
|
|
|
Lời giải:
- Đồ thị biểu diễn sự biến thiên pH của dung dịch trong quá trình chuẩn độ dung dịch HCl bằng dung dịch chuẩn NaOH 0,100 M:
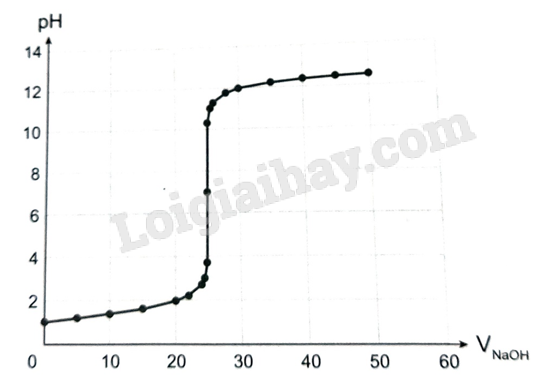
- Chuẩn độ HCl (acid mạnh) bằng NaOH (base mạnh):
+ Tại điểm tương đương, [H+] = [OH-]; pH = 7.
+ Bước nhảy chuẩn độ: ở khoảng pH từ 3,7 đến 10,3.
Xem thêm lời giải Sách bài tập Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Bài 2.1 trang 11 SBT Hóa học 11: Vì sao dung dịch của các muối, acid, base dẫn điện?...
Bài 2.2 trang 11 SBT Hóa học 11: Dung dịch sodium chloride (NaCl) dẫn được điện là do...
Bài 2.3 trang 11 SBT Hóa học 11: Saccharose là chất không điện li vì...
Bài 2.4 trang 11 SBT Hóa học 11: Phát biểu nào sau đây đúng khi nói về sự điện li?...
Bài 2.5 trang 11 SBT Hóa học 11: Các chất trong dãy nào sau đây là những chất điện li mạnh?...
Bài 2.6 trang 12 SBT Hóa học 11: Phương trình diện là nào sau đây biểu diễn không đúng?...
Bài 2.7 trang 12 SBT Hóa học 11: Phương trình điện li nào sau đây biểu diễn đúng?...
Bài 2.8 trang 12 SBT Hóa học 11: Khi chuẩn độ, người ta thêm từ từ dung dịch đựng trong (1) ... vào dung dịch đựng trong bình tam giác. Dụng cụ cần điền vào (1) là...
Bài 2.9 trang 12 SBT Hóa học 11: Cho các chất sau: glucose (C6H12O6), NaCl, KOH, Ba(OH)2, AlCl3, CuSO4, N2, O2, H2SO4, saccharose (C12H22O11). Chất nào là chất điện li trong các chất trên?...
Bài 2.10 trang 12 SBT Hóa học 11: Viết phương trình điện li của các chất sau trong nước: HBr, HNO3, KOH, Ca(OH)2, Al2(SO4)3, Cu(NO3)2, NaI, HCN, HF, HCOOH....
Bài 2.11 trang 12 SBT Hóa học 11: Tính nồng độ mol của các ion trong các dung dịch sau:...
Bài 2.12 trang 12 SBT Hóa học 11: Khả năng dẫn điện của nước vôi trong (dung dịch Ca(OH)2 trong nước) để trong không khí giảm dần theo thời gian. Hãy giải thích điều này....
Bài 2.13 trang 12 SBT Hóa học 11: Trong các phản ứng dưới đây, hãy cho biết ở phản ứng nào nước đóng vai trò là acid, ở phản ứng nào nước đóng vai trò là base theo thuyết Brønsted - Lowry:...
Bài 2.14 trang 12 SBT Hóa học 11: Cho các phân tử và ion sau:...
Bài 2.15 trang 13 SBT Hóa học 11: a) Tính pH của dung dịch có nồng độ ion H+ là 4,2×10-10 M...
Bài 2.16 trang 13 SBT Hóa học 11: Cho 10 mL dung dịch HCl có pH = 3. Hãy đề nghị cách pha dung dịch có pH = 4 từ dung dịch trên....
Bài 2.17 trang 13 SBT Hóa học 11: Vì sao người ta không sử dụng dung dịch acid HNO3 trong phương pháp chuẩn độ acid – base?...
Bài 2.18 trang 13 SBT Hóa học 11: Trộn 3 dung dịch H2SO4 0,1 M, HNO3 0,2 M và HCl 0,3 M với thể tích bằng nhau thu được dung dịch (A). Lấy 300 mL dung dịch (A) cho tác dụng với một dung dịch (B) gồm NaOH 0,20 M và KOH 0,29 M. Tính thể tích dung dịch (B) cần dùng để sau khi tác dụng với 300 mL dung dịch (A) thu được dung dịch có pH = 2...
Bài 2.19 trang 13 SBT Hóa học 11: Để chuẩn độ 40 mL dung dịch HCl chưa biết nồng độ đã dùng trung bình hết 34 mL dung dịch NaOH 0,12 M. Tính nồng độ mol của dung dịch HCl....
Bài 2.20 trang 13 SBT Hóa học 11: Để chuẩn độ 50 mL dung dịch CH3COOH chưa biết nồng độ đã dùng trung bình hết 75 mL dung dịch NaOH 0,05 M. Tính nồng độ mol của dung dịch CH3COOH....
Bài 2.21 trang 13 SBT Hóa học 11: Trong phương pháp chuẩn độ acid – base, xung quanh điểm tương đương có một sự thay đổi pH đột ngột gọi là bước nhảy chuẩn độ. Đường biểu diễn trên đồ thị chuẩn độ acid – base gọi là đường định phân. Từ các số liệu sau đây, hãy vẽ đồ thị biểu diễn sự biến thiên pH của dung dịch trong quá trình chuẩn độ dung dịch HCl bằng dung dịch chuẩn NaOH 0,100 M. Trục hoành ghi thể tích dung dịch NaOH, trục tung ghi pH của dung dịch. Xác định giá trị điểm tương đương và khoảng bước nhảy chuẩn độ của quá trình này...
Xem thêm các bài giải SBT Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Bài 1: Khái niệm về cân bằng hóa học
Bài 2: Cân bằng trong dung dịch nước
Ôn tập chương 1
Bài 3: Đơn chất nitrogen
Bài 4: Ammonia và một số hợp chất ammonium
