Với tóm tắt lý thuyết Hóa học lớp 11 Bài 1: Khái niệm về cân bằng hóa học sách Chân trời sáng tạo hay, chi tiết cùng với bài tập trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 11.
Lý thuyết Hóa học lớp 11 Bài 1: Khái niệm về cân bằng hóa học
A. Lý thuyết Khái niệm về cân bằng hóa học
1. Phản ứng một chiều, phản ứng thuận nghịch và cân bằng hóa học.
a. Tìm hiểu khái niệm phản ứng một chiều
- Phản ứng một chiều: Là phản ứng chỉ xảy ra theo chiều từ chất tham gia tạo thành sản phẩm mà sản phẩm không thể tác dụng với nhau lại chất ban đầu.
- Kí hiệu: (→) dùng để chỉ chiều phản ứng.
b. Tìm hiểu khái niệm phản ứng thuận nghịch
- Phản ứng thuận nghịch là phản ứng xảy ra theo hai chiều trái ngược nhau.
- Kí hiệu: (⇌). Chiều từ trái sang phải là chiều thuận, chiều từ phải sang trái chiều nghịch
c. Tìm hiểu khái niệm trạng thái cân bằng của phản ứng thuận nghịch
- Trạng thái cân bằng của phản ứng thuận nghịch là trạng thái mà tại đó tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
Ví dụ:
H2(g) + I2(g) ⇌ 2HI(g)
2SO2(g) + O2(g) ⇌ 2SO3(g)
2. Hằng số cân bằng của phản ứng thuận nghịch
Tìm hiểu hằng số cân bằng của phản ứng thuận nghịch
- Nếu phản ứng thuận nghịch ở dạng:
![]()
- Khi ở trạng thái cân bằng ta có:
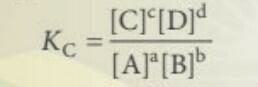
+ [A], [B], [C], [D] là nồng độ mol các chất ở trạng thái cân bằng
+ a, b, c, d hệ số tỉ lượng
+ Hằng số cân bằng Kc phụ thuộc vào nhiệt độ
3. Sự chuyển dịch cân bằng hóa học
Thí nghiệm nghiên cứu ảnh hưởng của nhiệt độ đến tới sự chuyển dịch cân bằng hóa học
- Nghiên cứu sự chuyển dịch cân bằng của phản ứng: 2NO2(g) ⇌ N2O2(g) hoặc thủy phân sodium acetate.
=> Sự chuyển dịch cân bằng hóa học là sự chuyển dịch từ trang thái cân bằng này sang trạng thái cân bằng khác.
4. Các yếu tố ảnh hưởng đến cân bằng hóa học
a. Tìm hiểu ảnh hưởng của nhiệt độ đến cân bằng hóa học
- Khi tăng nhiệt độ: Cân bằng chuyển dịch theo chiều phản ứng thu nhiệt (hay chiều làm giảm tác động)
- Khi nhiệt độ giảm: Cân bằng chuyển dịch theo chiều phản ứng tỏa nhiệt
b. Tìm hiểu ảnh hưởng của áp suất đến cân bằng hóa học
- Khi hệ đang ở trạng thái cân bằng thì tăng hoặc giảm áp suất chung của hệ, cân bằng bao giờ cũng chuyển dịch theo chiều làm giảm tác động của việc tăng hoặc giảm áp suất đó.
- Khi hệ số tỉ lượng của hai về bằng nhau không làm chuyển dịch cân bằng của hệ.
c. Tìm hiểu ảnh hưởng của nồng độ đến cân bằng hóa học
- Khi tăng hoặc giảm nồng độ một chất trong cân bằng thì cân bằng bao giờ cũng chuyển dịch theo chiều làm giảm tác động của việc tăng hoặc giảm nồng độ của chất đó.
Ví dụ:
C(r)+CO2 (k)⇌2CO(k)
Sơ đồ tư duy Khái niệm về cân bằng hóa học
B. Trắc nghiệm Khái niệm về cân bằng hóa học
Câu 1: Trộn 2 mol khí NO và một lượng chưa xác định khí O2 vào trong một bình kín có dung tích 1 lít ở 40oC Biết:
Khi phản ứng đạt đến trạng thái cân bằng, ta được hỗn hợp khí có 0,00156 mol O2 và 0,5 mol NO2. Hằng số cân bằng KC lúc này có giá trị là
A. 4,42.
B. 40,1.
C. 71,2.
D. 214.
Đáp án đúng là: C
Số mol NO ở trạng thái cân bằng là: nNO = nNO ban đầu – nNO phản ứng = 2 – 0,5 = 1,5 mol.
Vậy [NO] = 1,5M; [O2] = 0,00156M; [NO2] = 0,5M.
Câu 2: Cho cân bằng hoá học: ∆H > 0. Cân bằng không bị chuyển dịch khi:
A. tăng nhiệt độ của hệ.
B. giảm nồng độ HI.
C. giảm áp suất chung của hệ.
D. tăng nồng độ H2.
Đáp án đúng là: C
Do tổng số mol khí ở hai vế của phương trình hoá học bằng nhau nên thay đổi áp suất không làm cân bằng chuyển dịch.
Câu 3: Cho phản ứng: . Biết rằng phản ứng thuận là phản ứng toả nhiệt, cân bằng hoá học không bị chuyển dịch khi nào?
A. Thay đổi áp suất của hệ.
B. Thay đổi nhiệt độ của hệ.
C. Thay đổi nồng độ N2.
D. Thêm chất xúc tác Fe.
Đáp án đúng là: D
Chất xúc tác không làm thay đổi nồng độ các chất trong hệ cân bằng và cũng không làm thay đổi hằng số cân bằng nên không làm chuyển dịch cân bằng.
Câu 4: Cho phản ứng:
Nếu nhúng bình phản ứng vào nước đá thì:
A. Giữ nguyên màu như ban đầu.
B. Màu nâu đậm dần.
C. Màu nâu nhạt dần.
D. Chuyển sang màu xanh.
Đáp án đúng là: C
chiều thuận toả nhiệt.
Nếu nhúng bình phản ứng vào nước đá tức giảm nhiệt độ cân bằng sẽ chuyển dịch theo chiều phản ứng toả nhiệt, tức chiều thuận làm cho màu nâu nhạt dần.
Câu 5: Phản ứng tổng hợp ammonia là: .Yếu tố không giúp tăng hiệu suất tổng hợp ammonia là
A. tăng nhiệt độ.
B. lấy ammonia ra khỏi hỗn hợp phản ứng.
C. tăng áp suất.
D. bổ sung thêm khí nitrogen vào hỗn hợp phản ứng.
Đáp án đúng là: A
Tăng nhiệt độ cân bằng sẽ chuyển dịch theo chiều phản ứng thu nhiệt, tức chiều nghịch. Do đó không giúp tăng hiệu suất tổng hợp ammonia.
Câu 6: Cho phản ứng sau đây ở trạng thái cân bằng:
Nếu tách khí D ra khỏi môi trường phản ứng, thì:
A. Cân bằng hoá học chuyển dịch theo chiều thuận.
B. Cân bằng hoá học chuyển dịch theo chiều nghịch.
C. Tốc độ phản ứng thuận và tốc độ của phản ứng nghịch tăng như nhau.
D. Không gây ra sự chuyển dịch cân bằng hoá học.
Đáp án đúng là: A
Nếu tách khí D ra khỏi môi trường phản ứng, thì cân bằng hoá học sẽ chuyển dịch theo chiều làm tăng nồng độ chất D, tức chiều thuận.
Câu 7: Hằng số cân bằng KC của một phản ứng thuận nghịch phụ thuộc vào yếu tố nào sau đây?
A. Nồng độ
B. Nhiệt độ
C. Áp suất
D. Chất xúc tác
Đáp án đúng là: B
Trong phản ứng thuận nghịch, hằng số cân bằng KC của phản ứng xác định chỉ phụ thuộc vào nhiệt độ.
Câu 8: Phát biểu nào sau đây về một phản ứng thuận nghịch tại trạng thái cân bằng là không đúng?
A. Tốc độ của phản ứng thuận bằng tốc độ của phản ứng nghịch.
B. Nồng độ của tất cả các chất trong hỗn hợp phản ứng là không đổi.
C. Nồng độ mol của chất phản ứng luôn bằng nồng độ mol của chất sản phẩm phản ứng.
D. Phản ứng thuận và phản ứng nghịch vẫn diễn ra.
Đáp án đúng là: C
Tại trạng thái cân bằng, phản ứng thuận và phản ứng nghịch vẫn diễn ra, nhưng với tốc độ bằng nhau nên nồng độ của tất cả các chất trong hỗn hợp phản ứng là không đổi.
Câu 9: Cho phản ứng thuận nghịch: . Hằng số cân bằng của phản ứng trên là
A.
B.
C.
D.
Đáp án đúng là: A
Hằng số cân bằng của phản ứng trên là
Câu 10: Xét cân bằng: ở 25oC. Khi chuyển dịch sang một trạng thái cân bằng mới nếu nồng độ của N2O4 tăng lên 9 lần thì nồng độ của NO2:
A. tăng 9 lần.
B. tăng 3 lần.
C. tăng 4,5 lần.
D. giảm 3 lần.
Đáp án đúng là: B
Ta có:
Khi nồng độ của N2O4 tăng lên 9 lần, giả sử nồng độ NO2 tăng a lần:
Câu 11: Trong phản ứng tổng hợp ammonia:
Sẽ thu được nhiều khí NH3 nhất nếu:
A. Giảm nhiệt độ và áp suất.
B. Tăng nhiệt độ và áp suất.
C. Tăng nhiệt độ và giảm áp suất.
D. Giảm nhiệt độ và tăng áp suất.
Đáp án đúng là: D
∆rH < 0, chiều thuận toả nhiệt.
Để thu được nhiều NH3 nhất cần tác động để cân bằng chuyển dịch theo chiều thuận.
- Khi tăng áp suất, cân bằng chuyển dịch theo chiều làm giảm số mol khí, tức chiều thuận.
- Giảm nhiệt độ, cân bằng chuyển dịch theo chiều phản ứng toả nhiệt, tức chiều thuận.
Câu 12: Cho cân bằng:
Để cân bằng dịch chuyển theo chiều thuận, cách tốt nhất là
A. tăng nhiệt độ.
B. giảm nhiệt độ.
C. tăng áp suất.
D. tăng nhiệt độ, tăng áp suất.
Đáp án đúng là: B
∆rH < 0, chiều thuận toả nhiệt.
Giảm nhiệt độ, cân bằng sẽ chuyển dịch theo chiều phản ứng toả nhiệt, tức chiều thuận.
Câu 13: Ở nhiệt độ không đổi, hệ cân bằng nào sẽ dịch chuyển về bên phải nếu tăng áp suất?
A.
B.
C.
D.
Câu 14: Cho cân bằng hóa học: phản ứng thuận là phản ứng tỏa nhiệt. Phát biểu đúng là
A. Cân bằng chuyển dịch theo chiều thuận khi tăng nhiệt độ.
B. Cân bằng chuyển dịch theo chiều nghịch khi giảm nồng độ O2.
C. Cân bằng chuyển dịch theo chiều thuận khi giảm áp suất hệ phản ứng.
D. Cân bằng chuyển dịch theo chiều nghịch khi giảm nồng độ SO3.
Đáp án đúng là: B
Giảm nồng độ O2 cân bằng sẽ chuyển dịch theo chiều tăng nồng độ O2 tức chiều nghịch.
Câu 15: Cho phản ứng: Fe2O3 (s) + 3CO (g) 2Fe (s) + 3CO2 (g).
Khi tăng áp suất chung của hệ phản ứng thì
A. cân bằng chuyển dịch theo chiều thuận.
B. cân bằng không bị chuyển dịch.
C. cân bằng chuyển dịch theo chiều nghịch.
D. phản ứng dừng lại.
Đáp án đúng là: B
Do tổng hệ số tỉ lượng của các chất khí ở hai vế của phương trình hoá học bằng nhau nên việc thay đổi áp suất không làm cân bằng chuyển dịch.
Xem thêm các bài tóm tắt Lý thuyết Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác: