Với tóm tắt lý thuyết Hóa học lớp 11 Bài 4: Ammonia và một số hợp chất ammonium sách Chân trời sáng tạo hay, chi tiết cùng với bài tập trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học 11.
Lý thuyết Hóa học lớp 11 Bài 4: Ammonia và một số hợp chất ammonium
A. Lý thuyết Ammonia và một số hợp chất ammonium
1. Cấu tạo của phân tử Ammonia
- Amoniac là một hợp chất vô cơ được cấu tạo từ 3 nguyên tử nitơ và 1 nguyên tử hidro tạo thành liên kết kém bền.
- Cấu tạo của phân tử Ammonia:
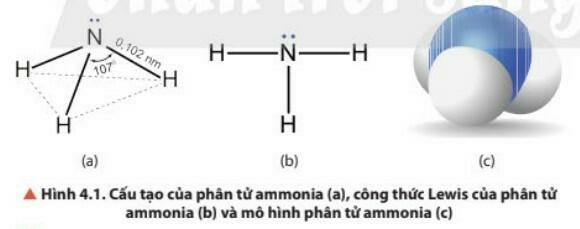
- NH3: có cấu trúc tóp tam giác, với nguyên tử nitrogen ở đỉnh, đáy là một tam giác mà đỉnh là 3 nguyên tử hydrogen
2. Tính chất của Ammonia
a. Tìm hiểu tính chất vật lí của Ammonia
- Ammonia là chất khí không màu, có mùi khai, xốc và nhẹ hơn không khí
- Tan nhiều trong nước → dung dịch Ammonia có nồng độ 25%
b. Tìm hiểu tính chất hóa học của Ammonia
* Ammonia có tính khử và tính base:
- Ammonia tan trong nước tạo thành ion ammonium NH4+ và giải phóng ion OH-
NH3 + H2O ⇌ NH4+ + OH-
- Ammonia tác dụng với Acid (HCl, H2SO4) → muối ammonium
- Ammonia cháy trong khí oxy → nitrogen và hơi nước
- Khi có xúc tác Pt, ở nhiệt độ cao tạo thành NO và H2O
3. Tổng hợp Ammonia
Vận dụng kiến thức hóa học cho phản ứng tổng hợp ammonia từ nitrogen và hydrogen trong quá trình Haber
- Các bước của quá trình Haber:
+ Trong điều kiện nhiệt độ, áp suất và chất xúc tác thích hợp, hỗn hợp nitrogen và hydrogen (tỉ lệ mol 1:3) được nén ở áp suất cao và đưa vào tháp tổng hợp ammonia
+ Hỗn hợp khí đi ra từ tháp tổng hợp gồm N2, H2 và NH3 được dẫn đến tháp làm lạnh:
+ NH3 được hóa lỏng
+ Hỗn hợp khí N, và H, chưa phản ứng được đưa trở lại tháp tổng hợp.
Ví dụ: N2(g) + 3H2(g) ⇌ 2NH3(g)
4. Muối Ammonium
a. Tìm hiểu tính chất vật lí của Ammonium
- Muối ammonium được cấu tạo bởi cation ammonium
- Kí hiệu: NH4
+ Muối ammonium là những chất tinh thể ion
+ Dễ tan trong nước
b. Tìm hiểu tính chất hóa học của Ammonium
- Muối ammonium tác dụng với dung dịch kiềm khi đun nóng cho khí ammonia có mùi xốc đặc trưng. Phản ứng này dùng để nhận biết ion ammonium trong dung dịch.
Ví dụ: NH4+ + OH- → NH3↑ + H2O
- Muối ammonium dễ bị phân huỷ khi đun nóng.
5. Ứng dụng
a. Tìm hiểu ứng dụng của ammonia
- Sử dụng để sản xuất nitric acid, các loại phân đạm
- Chất làm lạnh, làm dung môi và nhiều ứng dụng khác
b. Tìm hiểu ứng dụng của ammonium
- Ammonium nitrate dùng làm phân bón
- Ammonium khác dùng làm phân đạm, phân bón, phức hợp
Sơ đồ tư duy Ammonia và một số hợp chất ammonium
B. Trắc nghiệm Ammonia và một số hợp chất ammonium
Câu 1: Nhận định nào sau đây về phân tử ammonia không đúng?
A. Phân cực mạnh.
B. Có một cặp electron không liên kết.
C. Có độ bền nhiệt rất cao.
D. Có khả năng nhận proton.
Đáp án đúng là: C
Nhận định về phân tử ammonia không đúng là có độ bền nhiệt rất cao. Do có năng lượng liên kết nhỏ nên phân tử ammonia có độ bền nhiệt rất thấp.
Câu 2: Trong các phản ứng dưới đây, phản ứng nào NH3 thể hiện tính base?
A. 8NH3 + 3Cl2 6NH4Cl + N2.
B. 4NH3 + 5O2 4NO + 6H2O.
C. 2NH3 + 3CuO 3Cu + N2 + 3H2O.
D. NH3 + CO2 + H2O NH4HCO3.
Đáp án đúng là: D
Câu 3: Phản ứng nhiệt phân nào dưới đây không đúng?
A. NH4Cl NH3 + HCl.
B. NH4HCO3 NH3 + H2O + CO2.
C. NH4NO3 NH3 + HNO3.
D. NH4NO2 N2 + 2H2O.
Đáp án đúng là: C
NH4NO3 N2O + 2H2O.
Câu 4: Trong phân tử NH4NO3, nitrogen có số oxi hoá là
A. +1.
B. -1; +3.
C. +2.
D. -3; +5.
Đáp án đúng là: D
Câu 5: Nhận xét nào sau đây không đúng về muối ammonium?
A. Muối ammonium bền với nhiệt.
B. Các muối ammonium đều là chất điện li mạnh.
C. Tất cả các muối ammonium đều tan trong nước.
D. Các muối ammonium đều bị thủy phân trong nước.
Đáp án đúng là: A
Muối ammonium kém bền với nhiệt. Ví dụ:
NH4Cl NH3 + HCl.
NH4HCO3 NH3 + H2O + CO2.
Câu 6: Khi tác dụng với hydrochloric acid, ammonia đóng vai trò là
A. acid.
B. base.
C. chất oxi hoá.
D. chất khử.
Đáp án đúng là: B
Khi tác dụng với hydrochloric acid, ammonia đóng vai trò là base.
Câu 7: Ở trạng thái lỏng nguyên chất, phân tử chất nào sau đây tạo được liên kết hydrogen với nhau?
A. Nitrogen.
B. Ammonia.
C. Oxygen.
D. Hydrogen.
Đáp án đúng là: B
Các phân tử ammonia có thể tạo được liên kết hydrogen với nhau.
Câu 8: Trong phương pháp Ostwald, ammonia bị oxi hoá bởi oxygen không khí tạo thành sản phẩm chính là
A. NO.
B. N2.
C. N2O.
D. NO2.
Đáp án đúng là: A
Trong phương pháp Ostwald, ammonia bị oxi hoá bởi oxygen không khí tạo thành sản phẩm chính là NO.
Câu 9: Cho vài giọt dung dịch phenolphthalein vào dung dịch NH3, phenolphthalein chuyển sang màu nào sau đây?
A. Hồng.
B. Xanh.
C. Không màu.
D. Vàng.
Đáp án đúng là: A
Dung dịch NH3 có tính base, làm hồng dung dịch phenolphthalein.
Câu 10: Phân biệt được đung dịch NH4Cl và NaCl bằng thuốc thử là dung dịch
A. KCl
B. KNO3
C. KOH
D.K2SO4
Đáp án đúng là: C
Phân biệt được đung dịch NH4Cl và NaCl bằng thuốc thử là dung dịch KOH.
+ Nếu có khí mùi khai thoát ra → NH4Cl.
+ Nếu không có hiện tượng xuất hiện → NaCl.
Câu 11: Xét cân bằng hoá học:
Hằng số cân bằng (Kc) của phản ứng được biểu diễn bằng biểu thức nào sau đây?
A.
B.
C.
D.
Đáp án đúng là: B
Hằng số cân bằng của phản ứng:
Câu 12: X là muối khi tác dụng với dung dịch NaOH dư sinh khí mùi khai, tác dụng với dung dịch BaCl2 sinh kết tủa trắng không tan trong HNO3. X là muối nào trong số các muối sau?
A. (NH4)2CO3.
B. (NH4)2SO3.
C. NH4HSO3.
D. (NH4)2SO4.
Đáp án đúng là: D
(NH4)2SO4 + 2NaOH → Na2SO4 + 2NH3↑ + 2H2O
(NH4)2SO4 + BaCl2 → 2NH4Cl + BaSO4↓
Câu 13: Cho các phát biểu sau:
(1) Các muối ammonium tan trong nước tạo dung dịch chất điện li mạnh;
(2) Ion NH4+ tác dụng với dung dịch acid tạo kết tủa màu trắng;
(3) Muối ammonium tác dụng với dung dịch base thu được khí có mùi khai;
(4) Hầu hết muối ammonium đều bền nhiệt.
Phát biểu đúng là
A. (1) và (3).
B. (1) và (2).
C. (2) và (4).
D. (2) và (3).
Đáp án đúng là: A
Các phát biểu (1) và (3) đúng.
Câu 14: Cho phương trình hóa học tổng hợp NH3:
N2(g) + 3H2(g) 2NH3 (g);
Hiệu suất phản ứng tổng hợp NH3 tăng nếu:
A. Giảm áp suất, tăng nhiệt độ, có xúc tác.
B. Giảm áp suất, giảm nhiệt độ, có xúc tác.
C. Tăng áp suất, giảm nhiệt độ, có xúc tác.
D. Tăng áp suất, tăng nhiệt độ, có xúc tác.
Đáp án đúng là: C
Tăng áp suất, cân bằng chuyển dịch theo chiều giảm số mol khí, tức chiều thuận.
Giảm nhiệt độ, cân bằng chuyển dịch theo chiều phản ứng toả nhiệt, tức chiều thuận.
Câu 15: Các chất khí được thu vào bình theo đúng nguyên tắc bằng cách đẩy không khí (X, Y, Z) và đẩy nước (T) như sau:
Nhận xét nào sau đây không đúng?
A. X là chlorine.
B. Y là hydrogen.
C. Z là nitrogen dioxide.
D. T là ammonia.
Đáp án đúng là: D
Do ammonia tan tốt trong nước nên không được thu bằng phương pháp đẩy nước.
Xem thêm các bài tóm tắt Lý thuyết Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Lý thuyết Bài 3: Đơn chất nitrogen
Lý thuyết Bài 4: Ammonia và một số hợp chất ammonium
Lý thuyết Bài 5: Một số hợp chất với oxygen của nitrogen