Tailieumoi.vn xin giới thiệu đến các quý thầy cô, các em học sinh bộ câu hỏi trắc nghiệm Hóa học lớp 9 Bài 28: Co tác dụng với oxit kim loại chọn lọc, có đáp án. Tài liệu có 8 trang gồm 12 câu hỏi trắc nghiệm cực hay bám sát chương trình sgk Hóa học 9. Hi vọng với bộ câu hỏi trắc nghiệm Co tác dụng với oxit kim loại có đáp án này sẽ giúp bạn ôn luyện trắc nghiệm để đạt kết quả cao trong bài thi trắc nghiệm môn Hóa học 9.
Giới thiệu về tài liệu:
- Số trang: 8 trang
- Số câu hỏi trắc nghiệm: 12 câu
- Lời giải & đáp án: có
Mời quí bạn đọc tải xuống để xem đầy đủ tài liệu Trắc nghiệm Co tác dụng với oxit kim loại có đáp án – Hóa học lớp 9:

Co tác dụng với oxit kim loại
Bài 1: Cho luồng khí CO (dư) đi qua 9,1 gam hỗn hợp gồm CuO và Al2O3 nung nóng đến khi phản ứng hoàn toàn, thu được 8,3 gam chất rắn. Khối lượng CuO có trong hỗn hợp ban đầu là
A. 0,8 gam. B. 8,3 gam.
C. 2,0 gam. D. 4,0 gam.
Lời giải
Gọi số mol của CuO và Al2O3 lần lượt là a và b mol
=> mhỗnhợpđầu = 80a + 102b = 9,1 (1)
Khí CO chỉ phản ứng với CuO
CuO + CO 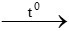 Cu + CO2
Cu + CO2
a mol → a mol
Hỗn hợp chất rắn sau phản ứng gồm Cu (a mol) và Al2O3 (b mol)
=> mhỗnhợp sau = 64a + 102b = 8,3 (2)
Lấy (1) trừ (2) ta có: 16a = 0,8 => a = 0,05 mol
=> mCuO = 0,05.80 = 4 gam
Đáp án: D
Bài 2: Cho V lít khí CO (ở đktc) phản ứng với một lượng dư hỗn hợp rắn gồm CuO và Fe2O3 nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng hỗn hợp rắn giảm 0,32 gam. Giá trị của V là
A. 0,224 B. 0,560
C. 0,112 D. 0,448
Lời giải
Giả sử khối lượng hỗn hợp rắn ban đầu là m gam => khối lượng rắn sau phản ứng là (m – 0,32) gam
CO + CuO 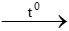 Cu + CO2
Cu + CO2
3CO + Fe2O3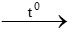 2Fe + 3CO2
2Fe + 3CO2
Từ 2 PTHH ta có: nCO = nCO2 = a mol
Bảo toàn khối lượng:
mCO + mCuO,Fe2O3 = mCO2 + mrắn sau phản ứng
=> 28a + m = 44a + m – 0,32
=> a = 0,02 mol
=> V = 0,02.22,4 = 0,448 lít
Đáp án: D
Bài 3: Dẫn từ từ V lít khí CO (ở đktc) đi qua một ống sứ đựng lượng dư hỗn hợp rắn gồm CuO, Fe2O3 (ở nhiệt độ cao). Sau khi các phản ứng xảy ra hoàn toàn, thu được khí X. Dẫn toàn bộ khí X ở trên vào lượng dư dung dịch Ca(OH)2 thì tạo thành 4 gam kết tủa. Giá trị của V là
A. 0,896 B. 1,120
C. 0,224 D. 0,448
Lời giải
CO + CuO 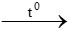 Cu + CO2
Cu + CO2
3CO + Fe2O3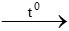 2Fe + 3CO2
2Fe + 3CO2
Từ 2 PTHH => nCO = nCO2
Cho khí X vào dung dịch Ca(OH)2
CO2 + Ca(OH)2 → CaCO3↓ + H2O
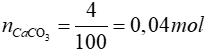
Theo PTHH: nCO2 = nCaCO3 = 0,04 mol
=> nCO = 0,04 mol
=> V = 0,04.22,4 = 0,896 lít
Đáp án: A
Bài 4: Hoà tan hoàn toàn 20 gam một oxit kim loại bằng dung dịch H2SO4 loãng thu được 50 gam muối. Khử hoàn toàn lượng oxit đó thành kim loại ở nhiệt độ cao cần V lít khí CO (đktc). Giá trị của V là
A. 2,80 B. 5,60
C. 6,72 D. 8,40
Lời giải
Gọi oxit kim loại cần tìm là R2On
R2On + nH2SO4 → R2(SO4)n + nH2O
Theo PTHH ta có:
![]()
Ta có bảng sau:
|
n |
1 |
2 |
3 |
4 |
|
R |
18,67 (loại) |
37,33 (loại) |
56 (Fe) |
74,67 (loại) |
=> oxit cần tìm là Fe2O3
![]()
Fe2O3 + 3CO 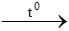 2Fe + 3CO2
2Fe + 3CO2
0,125 → 0,375
=> VCO = 0,375.22,4 = 8,4 lít
* Trường hợp oxit kim loại là Fe3O4
![]()
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
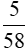 mol →
mol → 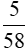 mol →
mol → 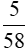 mol
mol
=> Khối lượng muối thu được là:
![]()
=> loại trường hợp này
Đáp án: D
Bài 5: Cho H2 dư qua 8,14 gam hỗn hợp A gồm CuO, Al2O3 và FexOy nung nóng. Sau khi phản ứng xong, thu được 1,44 gam H2O và a gam chất rắn. Giá trị của a là :
A. 6,70 B. 6,86
C. 6,78 D. 6,80
Lời giải
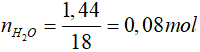
H2 + CuO 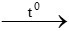 Cu + H2O
Cu + H2O
yH2 + FexOy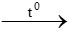 xFe + yH2O
xFe + yH2O
Từ PTHH ta có:
nH2 = nH2O =0,08 mol
Bảo toàn khối lượng:
mH2 = mhhA= mcran + mH2O
=> 0,08.2 + 8,14 = a + 1,44 => a = 6,86 gam
Đáp án: B
Bài 6: Khử 3,48 gam một oxit của kim loại M cần dùng 1,344 lít H2 (đktc). Toàn bộ lượng kim loại M sinh ra cho tác dụng với dung dịch HCl dư thu được 1,008 lít H2 (đktc). Công thức oxit là
A. Fe3O4. B. Fe2O3.
C. FeO. D. ZnO.
Lời giải
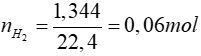
TH1: M không phải là Fe3O4
M2On + nH2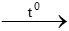 2M + nH2O
2M + nH2O
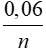 ← 0,06 →
← 0,06 → 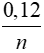
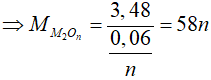
=> 2M + 16n = 58n => M = 21n
Ta có bảng sau:
|
n |
1 |
2 |
3 |
4 |
|
M |
21 (loại) |
42 (loại) |
63 (loại) |
84 (loại) |
=> loại trường hợp này
TH2: M là Fe3O4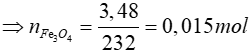
Fe3O4 + 4H2 3Fe + 4H2O
0,015 → 0,06 → 0,045 mol
Fe + 2HCl → FeCl2 + H2
0,045 mol → 0,045 mol
⇒VH2 = 0,045.22,4 = 1,008 lít (phù hợp đầu bài)
Vậy oxit cần tìm là Fe3O4
Đáp án: A
Bài 7: Cho luồng khí H2 dư qua hỗn hợp các oxit CuO, Fe2O3, ZnO, MgO nung nóng ở nhiệt độ cao. Sau phản ứng, hỗn hợp chất rắn còn lại là
A. Cu, Fe, ZnO, MgO.
B. Cu, Fe, Zn, Mg.
C. Cu, Fe, Zn, MgO.
D. Cu, FeO, ZnO, MgO.
Lời giải
Các chất khử C, CO, H2 không khử được các oxit MgO, Al2O3 và các oxit khác của kim loại kiềm và kiềm thổ
=> chỉ khử được CuO, Fe2O3, ZnO tạo thành Cu, Fe, Zn
=> hỗn hợp chất rắn thu được là Cu, Fe, Zn, MgO.
Đáp án: C
Bài 8: Cho khí CO (dư) đi vào ống sứ nung nóng đựng hỗn hợp X gồm Al2O3, MgO, Fe3O4, CuO thu được chất rắn Y. Cho Y vào dung dịch NaOH (dư), khuấy kĩ, thấy còn lại phần không tan Z. Giả sử các phản ứng xảy ra hoàn toàn. Phần không tan Z gồm:
A. MgO, Fe3O4, Cu.
B. MgO, Fe, Cu.
C. Mg, Fe, Cu.
D. Mg, Al, Fe, Cu.
Lời giải
Các chất khử C, CO, H2 không khử được các oxit MgO, Al2O3 và các oxit khác của kim loại kiềm và kiềm thổ.
=> trong hỗn hợp X, CO khử được Fe3O4 và CuO tạo ra Fe và Cu
=> chất rắn Y gồm: Al2O3, MgO, Fe, Cu
Cho Y vào dung dịch NaOH dư, chỉ có Al2O3 tan => chất rắn Z sau phản ứng gồm MgO, Fe, Cu
Đáp án: B
Bài 9: Khử hoàn toàn 32 gam CuO bằng khí CO dư, thu được m gam kim loại. Giá trị của m là
A. 12,8 B. 25,6
C. 32,0 D. 16,0
Lời giải
PTHH: CuO + CO 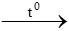 Cu + CO2
Cu + CO2
=> nCu = nCuO = 0,4 mol => mCu = 25,6 gam
Đáp án: B
Bài 10: Cho khí CO dư đi qua ống chứa 0,2 mol MgO và 0,2 mol CuO nung nóng đến phản ứng hoàn toàn, thu được x gam chất rắn. Giá trị của x là
A. 17,6 B. 4,8
C. 20,8 D. 24,0
Lời giải
MgO không phản ứng với CO
PTHH: CuO + CO 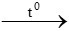 Cu + CO2
Cu + CO2
0,2 → 0,2
Chất rắn gồm MgO và Cu
=> x = mMgO + mCu = 0,2.40 + 0,2.64 = 20,8 gam
Đáp án: C
Bài 11: Cho khí CO qua ống chứa 15,2 gam hỗn hợp A gồm CuO và FeO nung nóng. Sau một thời gian thu được hỗn hợp khí B và 13,6 gam chất rắn C. Cho B tác dụng với dung dịch Ca(OH)2 dư thu được m gam kết tủa. Giá trị của m là :
A. 15 B. 10
C. 20 D. 25
Lời giải
CO + CuO 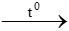 Cu + CO2
Cu + CO2
CO + FeO 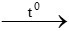 Fe + CO2
Fe + CO2
Từ PTHH ta có: nCO = nCo2 = a mol
Bảo toàn khối lượng: mCO + mhhA = mCo2 + mhhB
=> 28a + 15,2 = 44a + 13,6 => a = 0,1 mol
B tác dụng với dung dịch Ca(OH)2 dư:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,1 mol → 0,1 mol
=> mkếttủa = 0,1.100 = 10 gam
Đáp án: B
Bài 12: Dẫn một luồng khí CO dư qua ống sứ đựng m gam hỗn hợp Fe3O4 và CuO nung nóng đến khi phản ứng hoàn toàn thu được 2,32 gam hỗn hợp kim loại. Khí thoát ra khỏi bình được dẫn qua dung dịch nước vôi trong dư thu được 5 gam kết tủa. Giá trị của m là :
A. 6,24 B. 5,32
C. 3,12 D. 4,56
Lời giải
4CO + Fe3O4 → 3Fe + 4CO2
CO + CuO → Cu + CO2
Từ PTHH ta có: nCO = nCo2 = a mol
Khí thoát ra khỏi bình dẫn qua dung dịch Ca(OH)2 thu được 5 gam kết tủa CaCO3
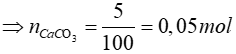
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,05 mol ← 0,05 mol
Bảo toàn khối lượng:
mCO + mhh Fe3O4, CuO = mCO2 + mhhkl
=> 0,05.28 + m = 0,05.44 + 2,32 => m = 3,12 gam
Đáp án: C