Với giải Câu hỏi 4 trang 12 Khoa học tự nhiên lớp 7 Cánh diều chi tiết trong Bài 1: Nguyên tử giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Khoa học tự nhiên 7. Mời các bạn đón xem:
Giải bài tập Khoa học tự nhiên lớp 7 Bài 1: Nguyên tử
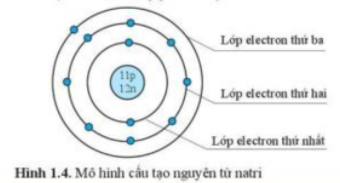
Câu hỏi 4 trang 12 KHTN lớp 7: Quan sát hình 1.4, hãy cho biết nguyên tử natri có bao nhiêu lớp electron. Mỗi lớp có bao nhiêu electron?
Phương pháp giải:
- Quan sát hình 1.4 và trả lời câu hỏi
+ Mỗi vòng tròn là 1 lớp electron
+ Mỗi chấm xanh là 1 electron
Trả lời:
- Trong hình 1.4 có
+ 3 vòng tròn => Natri có 3 lớp electron
+ 11 chấm xanh => Natri có 11 electron
Lý thuyết Sự chuyển động của electron trong nguyên tử
- Mô hình nguyên tử của Rơ-dơ-pho – Bo:
+ Electron chuyển động trên những quỹ đạo xác định xung quanh hạt nhân.
+ Electron phân bố trên các lớp electron theo chiều từ gần hạt nhân ra ngoài.
+ Số electron tối đa trên mỗi lớp được xác định, như lớp thứ nhất có tối đa 2 electron, lớp thứ hai có tối đa 8 electron,…
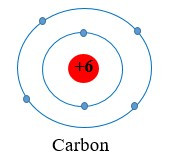
Ví dụ 1: Nguyên tử carbon có 6 electron, được phân bố thành hai lớp:
+ Lớp thứ nhất (lớp gần hạt nhân nhất) có 2 electron.
+ Lớp thứ hai có 4 electron.
Ta nói carbon có 4 electron ở lớp ngoài cùng.
Mở rộng: Trong số các nguyên tử đã biết hiện nay, nguyên tử có kích thước lớn nhất là francium, có chứa 7 lớp electron. Nguyên tử helium có kích thước nhỏ nhất với 1 lớp electron.
Xem thêm các bài giải Khoa học tự nhiên lớp 7 Cánh diều hay, chi tiết khác:
Câu hỏi 1 trang 10 KHTN lớp 7: Hãy cho biết nguyên tử là gì...
Câu hỏi 2 trang 10 KHTN lớp 7: Kể tên hai chất có chứa nguyên tử oxygen...
Câu hỏi 3 trang 11 KHTN lớp 7: Trong các hạt cấu tạo nên nguyên tử:...
Luyện tập 2 trang 11 KHTN lớp 7: Hoàn thành thông tin trong bảng sau:...
Tìm hiểu thêm trang 12 KHTN lớp 7: Điện tích của nguyên tử helium bằng bao nhiêu?...
Câu hỏi 6 trang 13 KHTN lớp 7: Khối lượng của nguyên tử được tính bằng đơn vị nào?...
Luyện tập 6 trang 13 KHTN lớp 7: Quan sát hình 1.5, hãy cho biết:...
Luyện tập 7 trang 14 KHTN lớp 7: Hoàn thành thông tin còn thiếu theo bảng sau:...
Xem thêm các bài giải SGK Khoa học tự nhiên lớp 7 Cánh diều hay, chi tiết khác:
Bài mở đầu : Phương pháp và kĩ năng trong học tập môn Khoa học tự nhiên
Bài 3: Sơ lược về bảng tuần hoàn các nguyên tố hóa học