Lời giải bài tập Khoa học tự nhiên lớp 7 Bài 3: Sơ lược về bảng tuần hoàn các nguyên tố hóa học sách Cánh diều hay, ngắn gọn sẽ giúp học sinh dễ dàng trả lời câu hỏi KHTN 7 Bài 3 từ đó học tốt môn Khoa học tự nhiên 7.
Giải bài tập KHTN lớp 7 Bài 3: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Video giải KHTN 7 Bài 3: Sơ lược về bảng tuần hoàn các nguyên tố hóa học - Cánh diều
Mở đầu trang 19 KHTN lớp 7: Trò chơi: Ai nhanh hơn?
Hãy sắp xếp những tấm thẻ vào các ô trong bảng dưới đây theo quy luật nhất định.
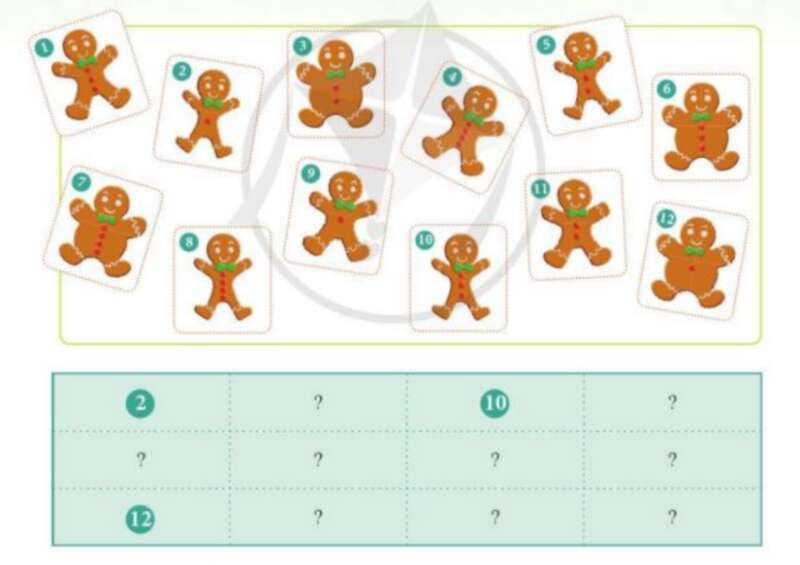
Hãy cho biết các tấm thẻ được sắp xếp theo quy luật nào theo hàng và theo cột. Tương tự như vậy, có thể sắp xếp các nguyên tố hóa học theo quy luật vào một bảng được không?
Phương pháp giải:
Coi các chấm đỏ là electron ở lớp ngoài cùng, kích thước con gấu là kích thước nguyên tử
Trả lời:
Coi các chấm đỏ là electron ở lớp ngoài cùng, kích thước con gấu là kích thước nguyên tử
+ Xét cột 1, (2) và (12) có cùng chấm đỏ, kích thước tăng dần
+ Xét hàng 1, (2) và (10) có cùng kích thước, số chấm đỏ tăng dần
=> Rút ra quy luật
+ Trong cùng 1 cột: Các nguyên tử có electron ở lớp ngoài cùng bằng nhau, kích thước nguyên tử tăng dần
+ Trong cùng 1 hàng: Các nguyên tử có kích thước bằng nhau, số electron ở lớp ngoài cùng tăng dần
| (2) | (5) | (10) | (8) |
| (9) | (11) | (1) | (4) |
| (12) | (3) | (6) | (7) |
Tương tự như vậy, ta có thể sắp xếp các nguyên tố hóa học theo quy luật vào 1 bảng
1. Nguyên tắc sắp xếp các nguyên tố hóa học trong bảng tuần hoàn
| C | ? | O |
| Si | ? | ? |
Phương pháp giải:
Sắp xếp các nguyên tố trên theo chiều điện tích hạt nhân tăng dần từ trái sang phải và từ trên xuống dưới
Trả lời:
| C | N | O |
| Si | P | S |
Phương pháp giải:
Học sinh tìm hiểu trên sách, báo, tivi, internet…
Trả lời:
- Năm 1860, Mendeleev (1834 - 1907) đã tiến hành nghiên cứu việc phân loại các nguyên tố. Cuối cùng Mendeleev đã phát hiện ra sự thay đổi tuần hoàn tính chất các nguyên tố theo khối lượng nguyên tử (thời đó người ta gọi là nguyên tử lượng) của chúng.
- Năm 1862, nhà địa chất Pháp đã sắp xếp các nguyên tố hóa học theo chiều tăng của khối lượng nguyên tử lên 1 băng giấy. Ông nhận thấy tính chất của các nguyên tô giống như tính chất của con số và tính chất đó lặp lại sau mỗi 7 nguyên tố
- Năm 1864, John Newlands tìm ra quy luật: Mỗi nguyên tố hóa học đều thể hiện tính chất tương tự như nguyên tố thứ 8 khi xếp các nguyên tố theo khối lượng nguyên tử tăng dần
2. Cấu tạo bảng tuần hoàn
Câu hỏi 2 trang 20 KHTN lớp 7: Hình 3.1 cho biết các thông tin gì về nguyên tố carbon?
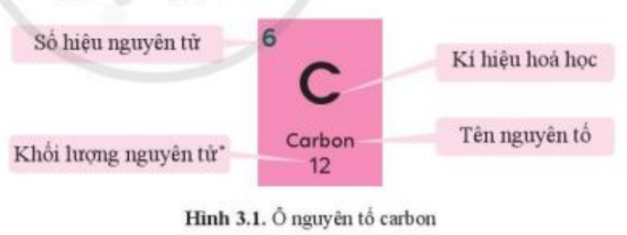
Phương pháp giải:
Quan sát hình 3.1 và nêu các thông tin đã biết từ ô nguyên tố carbon
Trả lời:
- Từ hình 3.1, ta biết được các thông tin sau:
+ Số hiệu nguyên tử của carbon là 6
+ Kí hiệu hóa học: C
+ Tên nguyên tố: Carbon
+ Khối lượng nguyên tử carbon: 12
Phương pháp giải:
- Quan sát bảng tuần hoàn trang 25
- Số thứ tự = số hiệu nguyên tử = số đơn vị điện tích hạt nhân
- Đọc thông tin ô 16 và 20 tương tự như nguyên tố carbon ở hình 3.1
Trả lời:
- Nguyên tố có số thứ tự 16:
+ Tên nguyên tố: sulfur
+ Số hiệu nguyên tử = số thứ tự: 16
+ Kí hiệu hóa học: S
+ Khối lượng nguyên tử: 32
- Nguyên tố có số thứ tự 20:
+ Tên nguyên tố: calcium
+ Số hiệu nguyên tử = số thứ tự: 20
+ Kí hiệu hóa học: Ca
+ Khối lượng nguyên tử: 40
Phương pháp giải:
Số thứ tự chu kì bằng số lớp electron trong nguyên tử của các nguyên tố trong chu kì đó
Trả lời:
- Nguyên tố carbon:
+ Có số hiệu nguyên tử: 6
+ Nằm ở chu kì 2 => Có 2 lớp electron
- Nguyên tố nhôm:
+ Có số hiệu nguyên tử: 13
+ Nằm ở chu kì 3 => Có 3 lớp electron
Phương pháp giải:
Số thứ tự chu kì bằng số lớp electron trong nguyên tử của các nguyên tố trong chu kì đó
Trả lời:
Nguyên tố có số thứ tự 15 là nguyên tố phosphorus, nằm ở hàng số 3
=> Nguyên tố đó nằm ở chu kì 3 và có 3 lớp electron
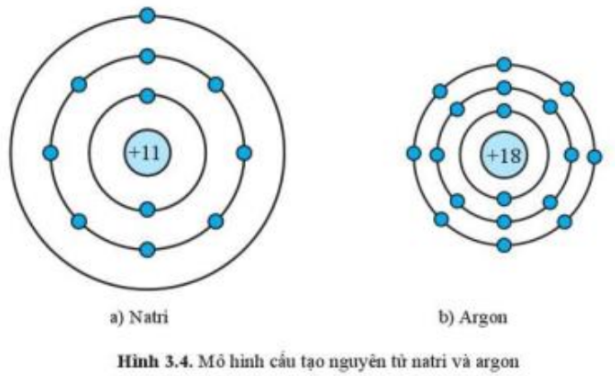
Phương pháp giải:
- Số hiệu nguyên tử = số đơn vị điện tích hạt nhân
- Số lớp electron = số chu kì = số vòng tròn quanh hạt nhân
- Số electron ở lớp ngoài cùng = số hình tròn xanh ở vòng tròn ngoài cùng
Trả lời:
- Xét mô hình nguyên tử natri:
+ Số hiệu nguyên tử: 11
+ Điện tích hạt nhân: +11
+ Có 3 vòng tròn quanh hạt nhân => Số lớp electron = chu kì = 3
+ Có 1 hình tròn xanh ở vòng tròn ngoài cùng => Có 1 electron ở lớp ngoài cùng
- Xét mô hình nguyên tử argon:
+ Số hiệu nguyên tử: 18
+ Điện tích hạt nhân: +18
+ Có 3 vòng tròn quanh hạt nhân => Số lớp electron = chu kì = 3
+ Có 8 hình tròn xanh ở vòng tròn ngoài cùng => Có 8 electron ở lớp ngoài cùng
Phương pháp giải:
Chất khí duy trì sự hô hấp của con người là khí oxygen
Trả lời:
- Chất khí duy trì sự hô hấp của con người và có nhiều trong không khí
=> Khí oxygen
- Tên nguyên tố: Oxygen
- Oxygen nằm ở ô số 8, hàng số 2 => Oxygen thuộc chu kì 2 trong bảng tuần hoàn
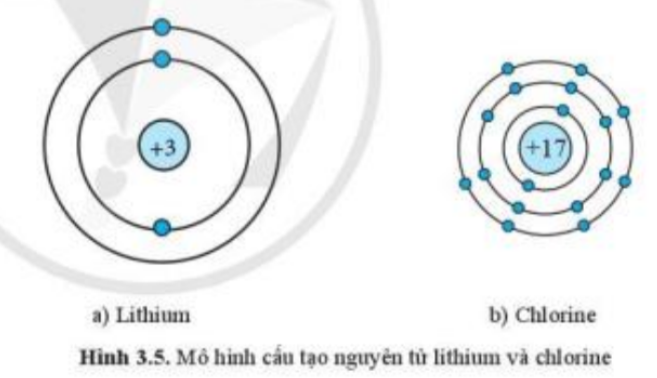
Phương pháp giải:
Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng trong nguyên tử của nguyên tố thuộc nhóm đó.
Trả lời:
- Xét mô hình cấu tạo của nguyên tử lithium: có 1 hình tròn xanh ở vòng tròn ngoài cùng => Có 1 electron ở lớp vỏ ngoài cùng => Thuộc nhóm IA
- Xét mô hình cấu tạo của nguyên tử chlorine: có 7 hình tròn xanh ở vòng tròn ngoài cùng => Có 7 electron ở lớp vỏ ngoài cùng => Thuộc nhóm VIIA
Phương pháp giải:
- Quan sát bảng tuần hoàn
- Số electron lớp ngoài cùng = số thứ tự nhóm A của nguyên tố
- Nhóm IA: kim loại hoạt động mạnh
- Nhóm VIIA: phi kim hoạt động mạnh
- Nhóm VIIIA: khí hiếm
Trả lời:
- Xét nguyên tố có số thứ tự 9:
+ Nằm ở nhóm VIIA => Có 7 electron ở lớp vỏ ngoài cùng và thuộc phi kim hoạt động mạnh
- Xét nguyên tố có số thứ tự 18:
+ Nằm ở nhóm VIIIA => Có 8 electron ở lớp vỏ ngoài cùng và là khí hiếm
- Xét nguyên tố có số thứ tự 19:
+ Nằm ở nhóm IA => Có 1 electron ở lớp vỏ ngoài cùng thuộc kim loại hoạt động mạnh
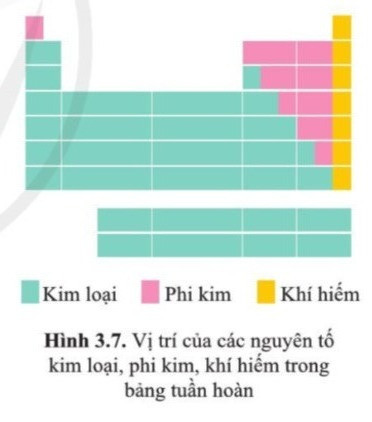
3. Vị trí của các nguyên tố kim loại, phi kim và khí hiếm trong bảng tuần hoàn
Phương pháp giải:
- Dựa vào chú thích của bảng tuần hoàn:
+ Màu xanh: kim loại
+ Màu hồng: phi kim
+ Màu vàng: khí hiếm
Trả lời:
- Vị trí kim loại: nằm ở phía bên trái và góc dưới bên phải của bảng tuần hoàn
- Vị trí phi kim: nằm ở phía trên, bên phải của bảng tuần hoàn
- Vị trí khí hiếm: tất cả các nguyên tố nằm trong nhóm VIIIA
4. Ý nghĩa của bảng tuần hoàn
Phương pháp giải:
- Nguyên tố X nằm ở chu kì 2, nhóm VA => Hàng số 2, cột VA => Nguyên tố phosphorus
Trả lời:
- Nguyên tố X nằm ở chu kì 2, nhóm VA => Hàng số 2, cột VA
=> Nguyên tố phosphorus
+ Tên nguyên tố: Phosphorus
+ Kí hiệu hóa học: P
+ Khối lượng nguyên tử: 31
+ Ví trí ô của nguyên tố trong bảng tuần hoàn = số hiệu nguyên tử = 15
+ Ô nguyên tố có màu hồng => Phi kim
Phương pháp giải:
Tham khảo bảng tuần hoàn trang 25
Trả lời:
Lý thuyết KHTN 7 Bài 3: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
I. Nguyên tắc sắp xếp bảng tuần hoàn các nguyên tố hóa học
- Các nguyên tố hóa học được xếp theo quy luật trong một bảng, gọi là bảng tuần hoàn các nguyên tố hóa học (gọi tắt là bảng tuần hoàn).
- Bảng tuần hoàn hiện nay có 118 nguyên tố hóa học và được xếp theo nguyên tắc sau:
+ Các nguyên tố hóa học được xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử.
+ Các nguyên tố được xếp trong cùng một hàng có cùng số lớp electron trong nguyên tử.
+ Các nguyên tố trong cùng một cột có tính chất hóa học tương tự nhau.
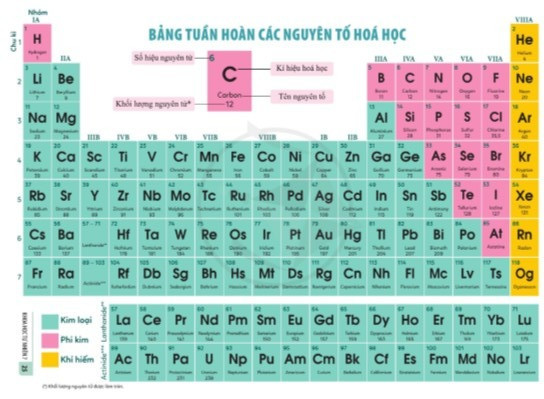
II. Cấu tạo bảng tuần hoàn
Bảng tuần hoàn gồm các ô được sắp xếp thành các hàng và các cột.
1. Ô nguyên tố
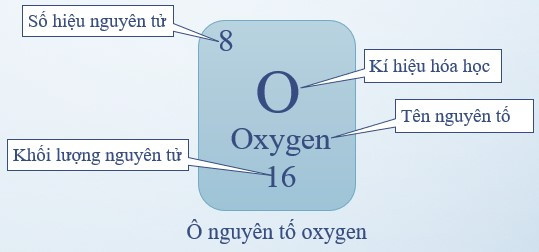
- Ô nguyên tố: là một ô trong bảng tuần hoàn tương ứng với một nguyên tố hóa học.
- Ô nguyên tố cho biết:
+ Số hiệu nguyên tử (kí hiệu là Z): bằng số đơn vị điện tích hạt nhân (bằng số proton và bằng số electron) và là số thứ tự của nguyên tố
+ Kí hiệu hóa học
+ Tên nguyên tố
+ Khối lượng nguyên tử
Ví dụ: Ô nguyên tố oxygen
2. Chu kì
- Chu kì gồm các nguyên tố thuộc cùng nguyên tử có cùng số lớp electron và được sắp xếp thành hàng theo chiều tăng dần của điện tích hạt nhân.
- Số thứ tự của chu kì = số lớp electron của nguyên tố
- Bảng tuần hoàn hiện nay gồm 7 chu kì, được đánh số từ chu kì 1 đến chu kì 7.
- Trong một chu kì, khi đi từ trái qua phải theo chiều tăng dần của điện tích hạt nhân:
+ Mở đầu chu kì là một kim loại điển hình (trừ chu kì 1).
+ Cuối chu kì là một phi kim điển hình (trừ chu kì 7).
+ Kết thúc chu kì là một khí hiếm.
- Ví dụ: Trong chu kì 4:
+ Mở đầu chu kì là nguyên tố potassium (K) – là một kim loại điển hình
+ Cuối chu kì là nguyên tố bromine (Br) – là một phi kim điển hình
+ Kết thúc chu kì là nguyên tố krypton (Kr) – là một khí hiếm
3. Nhóm
- Nhóm gồm các nguyên tố có tính chất hóa học tương tự nhau, được xếp thành cột theo chiều tăng dần của điện tích hạt nhân.
- Bảng tuần hoàn gồm 18 cột gồm:
+ 8 cột là nhóm A.
+ 10 cột là nhóm B: gọi kà nhóm các nguyên tố kim loại chuyển tiếp (trong phạm vi chương trình chỉ nghiên cứu 8 nhóm A).
- Nhóm A được đánh số bằng số La Mã lần lượt từ nhóm IA đến VIIIA.
- Số thứ tự của nhóm A = số electron lớp ngoài cùng.
Ví dụ:
+ Nhóm IA: gồm các nguyên tố kim loại hoạt động mạnh (kim loại điển hình), trừ hydrogen (H); đều có 1 electron ở lớp ngoài cùng.
+ Nhóm VIIA: gồm các nguyên tố phi kim hoạt động mạnh (phi kim điển hình), trừ tennessine (Ts); đều có 7 electron ở lớp ngoài cùng.
III. Vị trí của các nguyên tố kim loại, phi kim và khí hiếm trong bảng tuần hoàn
- Các nguyên tố kim loại: (chiếm hơn 80% trong bảng tuần hoàn), nằm bên góc trái và góc dưới bên phải của bảng tuần hoàn.
- Các nguyên tố phi kim: nằm phía trên, bên phải của bảng tuần hoàn. Trong đó, các phi kim hoạt động mạnh nằm ở phía trên.
- Các nguyên tố khí hiếm: Là nguyên tố nằm trong nhóm VIIIA.
IV. Ý nghĩa của bảng tuần hoàn
Bảng tuần hoàn cho biết:
- Các thông tin của một nguyên tố hóa học: tên nguyên tố, số hiệu nguyên tử, kí hiệu hóa học, khối lượng nguyên tử.
- Vị trí của nguyên tố hóa học (ô, chu kì, nhóm). Từ đó nhận ra được các nguyên tố kim loại, phi kim hay khí hiếm:
+ Các nguyên tố ở nhóm IA, IIA, IIIA là kim loại (trừ hydrogen và boron).
+ Hầu hết các nguyên tố ở nhóm VA, VIA, VIIA là phi kim.
+ Các nguyên tố nhóm VIIIA là khí hiếm.
Ví dụ: Bảng tuần hoàn cho biết nguyên tố bromine (Br) ở ô số 35, chu kì 4, nhóm VIIA, là nguyên tố phi kim.
Xem thêm các bài giải SGK Khoa học tự nhiên lớp 7 Cánh diều hay, chi tiết khác:
Bài 4: Phân tử, đơn chất, hợp chất
Bài 5: Giới thiệu về liên kết hóa học