Với Giải hóa học lớp 10 trang 75 Kết nối tri thức chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải hóa học 10 trang 75 Kết nối tri thức
Câu 3 trang 75 Hóa học 10: Xét các phản ứng hóa học xảy ra trong công nghiệp:
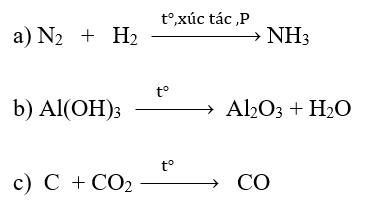
Phản ứng nào là phản ứng oxi hóa – khử? Lập phương trình hóa học của phản ứng oxi hóa khử theo phương pháp thăng bằng electron.
Phương pháp giải:
Dấu hiệu để nhận biết phản ứng oxi hóa – khử là có sự thay đổi số oxi hóa của các nguyên tử.
Lời giải:
a)
Nguyên tử N trong phản ứng có sự thay đổi số oxi hóa từ 0 xuống -3
=> Phản ứng oxi hóa – khử.
Bước 1: Xác định số oxi hóa của nguyên tử bị thay đổi:
![]()
Bước 2: Biểu diễn quá trình oxi hóa – khử:
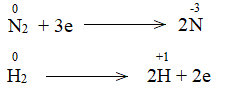
Bước 3: Tìm hệ số thích hợp cho chất khử và chất oxi hóa theo nguyên tắc: tổng số electron chất khử nhường bằng tổng số electron chất oxi hóa nhận.
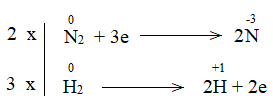
Bước 4: Đặt hệ số
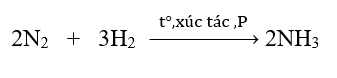
b)
Trước phản ứng, các nguyên tử Al, O và H có số oxi hóa lần lượt là +3, -2, +1
Sau phản ứng, các nguyên tử Al, O và H có số oxi hóa lần lượt là +3, -2, +1.
=> Trong phản ứng, các nguyên tử không có sự thay đổi số oxi hóa => Không là phản ứng oxi hóa – khử.
c)
Trong phản ứng, C trước phản ứng có số oxi hóa 0. Kết thúc phản ứng, C có số oxi hóa +2
=> Phản ứng oxi hóa khử
Bước 1: Xác định số oxi hóa của nguyên tử bị thay đổi:
![]()
Bước 2: Biểu diễn quá trình oxi hóa – khử:
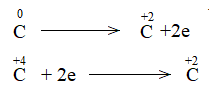
Bước 3: Tìm hệ số thích hợp cho chất khử và chất oxi hóa theo nguyên tắc: tổng số electron chất khử nhường bằng tổng số electron chất oxi hóa nhận.
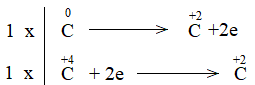
Bước 4: Đặt hệ số
C + CO2 2CO
Xem thêm các bài giải Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác: