Với lời giải SBT Hóa học 11 trang 37 chi tiết trong Bài 9: Ôn tập chương 2 sách Kết nối tri thức giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 9: Ôn tập chương 2
Bài 9.19 trang 37 Sách bài tập Hóa học 11: Một nhà máy luyện kim, ở giai đoạn đầu của quá trình sản xuất Zn từ quặng blend thu được sản phẩm phụ là SO2 theo so đồ phản ứng:
Đốt cháy 1 tấn quặng blend (chứa 77,6% khối lượng ZnS) bằng không khí, thu được tối đa V m3 khí SO2 (đkc). Giá trị của V là
A. 99,2.
B. 198,3.
C. 297,5.
D. 396,6.
Lời giải:
Đáp án đúng là: B
Bài 9.20 trang 37 Sách bài tập Hóa học 11: Cho cân bằng hoá học sau:
a) Hãy tính của phản ứng, cho nhiệt tạo thành của NO2(g) và N2O4(g) lần lượt là 33,2 kJ/mol và 11,1 kJ/mol.
b) Cân bằng sẽ chuyển dịch theo chiều nào khi giảm nhiệt độ của hệ?
Lời giải:
a)
b) , phản ứng tỏa nhiệt cân bằng chuyển dịch theo chiều thuận khi giảm nhiệt độ của hệ.
Bài 9.21 trang 37 Sách bài tập Hóa học 11: Hoà tan 3,92 g một muối X ngậm nước vào cốc nước, thu được 100 mL dung dịch X gồm các ion: Fe2+, NH4+ và SO42-. Cho dung dịch NaOH dư vào 20 mL dung dịch X, đun nóng, thu được 49,58 mL khí (đkc). Cho dung dịch BaCl2 dư vào 20 mL dung dịch X, thu được 0,466 g kết tủa. Xác định công thức của X.
Lời giải:
Thí nghiệm 1:
Thí nghiệm 2:
Áp dụng định luật bảo toàn điện tích: Số mol Fe2+ = 0,001 mol.
Công thức của X có dạng: (NH4)2Fe(SO4)2.nH2O = 0,001 mol.
M = 392 n = 6.
Bài 9.22 trang 37 Sách bài tập Hóa học 11: Cho phản ứng sau:
Hãy xác định :
a) Biến thiên enthalpy . của phản ứng, cho nhiệt tạo thành chuẩn của S8(g) và H2S(g) lần lượt là 101,3 kJ/mol và -20,6 kJ/mol.
b) Năng lượng liên kết S-S trong phân tử S8(g), biết Eb(H-H) = 436 kJ/mol và Eb(S-H) = 363 kJ/mol.
Lời giải:
a)
b) 436.1 + Eb(S-S).1 – 363.2 = -33,3 Eb(S-S) = 257 kJ/mol.
Bài 9.23 trang 37 Sách bài tập Hóa học 11: Hydrogen sulfide phân huỷ theo phản ứng sau đây:
Hằng số cân bằng KC = 9,3.10-8 ở 427oC.
a) Viết biểu thức hằng số cân bằng KC của phản ứng.
b) Xác định biến thiên enthalpy chuẩn của phản ứng, biết nhiệt tạo thành chuẩn của và lần lượt là -20,6 kJ/mol và 128,6 kJ/mol. Cho biết phản ứng thuận là toả nhiệt hay thu nhiệt.
c) Ở 427oC, tính hằng số cân bằng K’C của phản ứng:
Lời giải:
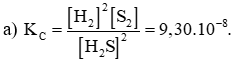
b)
Phản ứng thuận là phản ứng thu nhiệt.
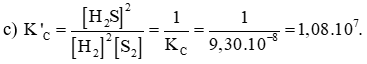
Xem thêm lời giải Sách bài tập Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 9.1 trang 34 Sách bài tập Hóa học 11: Trong khí quyển Trái Đất, phần trăm thể tích khí nitrogen chiếm là...
Bài 9.2 trang 34 Sách bài tập Hóa học 11: Chất nào sau đây được sử dụng là chất làm lạnh trong các hệ thống làm lạnh công nghiệp?....
Bài 9.3 trang 35 Sách bài tập Hóa học 11: Mưa acid là một thảm hoạ thiên nhiên toàn cầu, ảnh hưởng đến sự sống của các sinh vật. Mưa acid là hiện tượng nước mưa có....
Bài 9.4 trang 35 Sách bài tập Hóa học 11: Quá trình đốt cháy hồn hợp hơi nhiên liệu và không khí trong động cơ khi đánh tia lửa điện sinh ra khí NO, một tác nhân gây ô nhiễm không khí. Tên gọi của NO là...
Bài 9.5 trang 35 Sách bài tập Hóa học 11: Oxide X là chất khí, mùi hắc, độc (gây ho, viêm đường hô hấp). Trong công nghiệp, X được dùng làm chất tẩy trắng bột gỗ, sản xuất sulfuric acid. Công thức của X là...
Bài 9.6 trang 35 Sách bài tập Hóa học 11: Nhỏ 1 giọt dung dịch acid đặc nào sau đây lên tờ giấy trắng thì tờ giấy bị hoá đen ở chỗ tiếp xúc với acid?.....
Bài 9.7 trang 35 Sách bài tập Hóa học 11: Dung dịch loãng của acid nào sau đây hoà tan được lá bạc, tạo thành muối tương ứng?....
Bài 9.8 trang 35 Sách bài tập Hóa học 11: Trong công nghiệp, quặng pyrite sắt (FeS2) được dùng làm nguyên liệu để....
Bài 9.9 trang 35 Sách bài tập Hóa học 11: Khí nào sau đây tan trong nước thu được dung dịch có khả năng làm phenolphthalein chuyển màu hồng?....
Bài 9.10 trang 35 Sách bài tập Hóa học 11: Trong công nghiệp thực phẩm, nitrogen lỏng (D = 0,808 g/mL) được phun vào vỏ bao bì trước khi đóng nắp để làm căng vỏ bao bì. Thể tích khí nitrogen thu được (đkc) khi hoá hơi 1 mL nitrogen lỏng là...
Bài 9.11 trang 36 Sách bài tập Hóa học 11: Cho cân bằng hoá học sau: ...
Bài 9.12 trang 36 Sách bài tập Hóa học 11: Cho một ít tinh thể muối X vào ống nghiệm và đun nóng trên ngọn lửa đèn cồn, sau một thời gian thấy không còn chất rắn nào ở đáy ống nghiệm. Muối X có thể là muối nào sau đây?...
Bài 9.13 trang 36 Sách bài tập Hóa học 11: Cho các chất sau: H2SO4, SO2, N2, NH3......
Bài 9.14 trang 36 Sách bài tập Hóa học 11: Trong phản ứng giữa khí ammonia và khí hydrogen chloride tạo thành ammonium chloride ở dạng khói trắng, ammonia đóng vai trò là....
Bài 9.15 trang 36 Sách bài tập Hóa học 11: Cho các acid ở dạng đậm đặc sau: HCl, HNO3, H3PO4, H2SO4.....
Bài 9.16 trang 36 Sách bài tập Hóa học 11: Tiến hành các thí nghiệm cho dung dịch H2SO4 loãng lần lượt tác dụng với: Mg, NaHCO3, BaCl2, CaCO3. Số thí nghiệm xảy ra phản ứng oxi hoá – khử là...
Bài 9.17 trang 36 Sách bài tập Hóa học 11:Cho các chất khí sau: H2S, NO, NO2, SO2....
Bài 9.18 trang 36 Sách bài tập Hóa học 11: Cho cân bằng hoá học sau:.....
Bài 9.19 trang 37 Sách bài tập Hóa học 11: Một nhà máy luyện kim, ở giai đoạn đầu của quá trình sản xuất Zn từ quặng blend thu được sản phẩm phụ là SO2 theo so đồ phản ứng:....
Bài 9.20 trang 37 Sách bài tập Hóa học 11: Cho cân bằng hoá học sau: ......
Bài 9.21 trang 37 Sách bài tập Hóa học 11: Hoà tan 3,92 g một muối X ngậm nước vào cốc nước, thu được 100 mL dung dịch X gồm các ion: Fe2+, NH4+ và SO42-. Cho dung dịch NaOH dư vào 20 mL dung dịch X, đun nóng, thu được 49,58 mL khí (đkc). Cho dung dịch BaCl2 dư vào 20 mL dung dịch X, thu được 0,466 g kết tủa. Xác định công thức của X.....
Bài 9.22 trang 37 Sách bài tập Hóa học 11: Cho phản ứng sau:...
Bài 9.23 trang 37 Sách bài tập Hóa học 11: Hydrogen sulfide phân huỷ theo phản ứng sau đây:.....
Bài 9.24 trang 38 Sách bài tập Hóa học 11: Hiện nay, mưa acid, hiệu ứng nhà kính và thủng tầng ozone là ba thảm hoạ môi trường toàn cầu. Mưa acid tàn phá nhiều rừng cây, các công trình kiến trúc bằng đá và kim loại. Tác nhân chủ yếu gây ra mưa acid là sulfur dioxide......
Xem thêm các bài giải SBT Hóa học lớp 11 Kết nối tri thức hay, chi tiết khác:
Bài 8: Sulfuric acid và muối sulfate
Bài 9: Ôn tập chương 2
Bài 10: Hợp chất hữu cơ và hoá học hữu cơ
Bài 11: Phương pháp tách biệt và tinh chế hợp chất hữu cơ
Bài 12: Công thức phân tử hợp chất hữu cơ
Bài 13: Cấu tạo hoá học hợp chất hữu cơ