Với giải sách bài tập Khoa học tự nhiên 7 Bài 6: Giới thiệu về liên kết hóa học sách Chân trời sáng tạo hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Khoa học tự nhiên 7. Mời các bạn đón xem:
Giải SBT Khoa học tự nhiên lớp 7 Bài 6: Giới thiệu về liên kết hóa học
Bài 6.1 trang 18 SBT Khoa học tự nhiên 7: Phát biểu nào sau đây đúng?
A. Tất các các nguyên tố khí hiếm đều có 8 electron ở lớp ngoài cùng.
B. Vỏ nguyên tử của các nguyên tố khí hiếm đều có cùng số lớp electron.
C. Các nguyên tố khí hiếm đều rất khó hoặc không kết hợp với nguyên tố khác thành hợp chất.
D. Hợp chất tạo bởi các nguyên tố khí hiếm đều ở thể khí.
Lời giải:
Đáp án đúng là: C
A sai vì He là khí hiếm chỉ có 2 electron ở lớp ngoài cùng.
B sai vì số lớp electron của các khí hiếm là khác nhau.
D sai vì khí hiếm gần như không kết hợp với các nguyên tố khác tạo hợp chất.
A. nhường các electron ở lớp ngoài cùng.
B. nhận thêm electron vào lớp electron ngoài cùng.
C. nhường electron hoặc nhận electron để lớp electron ngoài cùng đạt trạng thái bền (có 8 electron).
D. nhường electron hoặc nhận electron hoặc góp chung electron.
Lời giải:
Đáp án đúng là: D
Để có số electron ở lớp ngoài cùng giống nguyên tử của nguyên tố khí hiếm, các nguyên tử của nguyên tố có khuynh hướng nhường electron hoặc nhận electron hoặc góp chung electron.
Bài 6.3 trang 18 SBT Khoa học tự nhiên 7: Phát biểu nào sau đây đúng?
A. Để tạo ion dương thì nguyên tử của nguyên tố phi kim sẽ nhường các electron ở lớp ngoài cùng.
B. Để tạo ion dương thì nguyên tử của nguyên tố phi kim sẽ nhận thêm electron để có đủ 8 electron ở lớp electron ngoài cùng.
C. Để tạo ion dương thì nguyên tử của nguyên tố kim loại sẽ nhận thêm electron để có đủ 8 electron ở lớp electron ngoài cùng.
D. Để tạo ion dương thì nguyên tử của nguyên tố hóa học sẽ nhường các electron ở lớp ngoài cùng.
Lời giải:
Đáp án đúng là: D
Để tạo ion dương thì nguyên tử của nguyên tố hóa học sẽ nhường các electron ở lớp ngoài cùng.
A, B sai vì nguyên tử của nguyên tố phi kim không tạo ion dương.
C sai vì nguyên tử của nguyên tố kim loại chỉ nhường electron.
Bài 6.4 trang 18 SBT Khoa học tự nhiên 7: Phát biểu nào sau đây đúng?
A. Nguyên tố tạo ion âm đều là nguyên tố phi kim.
B. Nguyên tố tạo ion dương có thể là nguyên tố kim loại hoặc nguyên tố phi kim.
C. Để tạo ion dương thì nguyên tố phi kim sẽ nhường electron.
D. Để tạo ion âm thì nguyên tố kim loại sẽ nhận electron.
Lời giải:
Đáp án đúng là: A
B sai vì nguyên tố kim loại không tạo ion âm.
C sai vì nguyên tố phi kim không nhường electron.
D sai vì nguyên tố kim loại không nhận electron.
Bài 6.5 trang 18 SBT Khoa học tự nhiên 7: Phát biểu nào sau đây đúng?
A. Để tạo ion âm thì nguyên tử của nguyên tố phi kim sẽ nhường electron ở lớp ngoài cùng.
B. Để tạo ion âm thì nguyên tử của nguyên tố phi kim sẽ nhận thêm electron để có đủ 8 electron ở lớp electron ngoài cùng.
C. Để tạo ion âm thì nguyên tử của nguyên tố kim loại sẽ nhận thêm electron để có đủ 8 electron ở lớp electron ngoài cùng.
D. Để tạo ion âm thì nguyên tử của nguyên tố hóa học sẽ nhường các electron ở lớp ngoài cùng.
Lời giải:
Đáp án đúng là: B
A sai vì nguyên tố phi kim nhận electron.
C sai vì nguyên tố kim loại không nhận thêm electron.
D sai vì nguyên tử của nguyên tố hóa học nhường electron sẽ tạo thành ion dương.
Bài 6.6 trang 19 SBT Khoa học tự nhiên 7: Phát biểu nào sau đây không đúng?
A. Liên kết trong các phân tử đơn chất thường là liên kết cộng hóa trị.
B. Sau khi các nguyên tử liên kết với nhau, số electron ở lớp ngoài cùng sẽ giống nguyên tố khí hiếm.
C. Liên kết giữa các nguyên tố phi kim thường là liên kết cộng hóa trị.
D. Liên kết giữa các nguyên tố kim loại với nguyên tố phi kim đều là liên kết ion.
Lời giải:
Đáp án đúng là: D
D sai vì có một số trường hợp đặc biệt liên kết giữa nguyên tố kim loại với nguyên tố phi kim là liên kết cộng hóa trị vú dụ AlCl3.
Bài 6.7 trang 19 SBT Khoa học tự nhiên 7: Ở điều kiện thường, phát biểu nào sau đây là đúng?
A. Tất cả các hợp chất ở thể rắn đều là chất ion.
B. Chất cộng hóa trị luôn ở thể rắn.
C. Chất chỉ có liên kết cộng hóa trị là chất cộng hóa trị và luôn ở thể khí.
D. Hợp chất có chứa kim loại thường là chất ion.
Lời giải:
Đáp án đúng là: D
A sai vì hợp chất cộng hóa trị cũng ở thể rắn, ví dụ đường, iodine…
B, C sai vì hợp chất cộng hóa trị có thể ở thể rắn, thể lỏng hoặc thể khí.
Bài 6.8 trang 19 SBT Khoa học tự nhiên 7: Phát biểu nào sau đây không đúng?
A. Hợp chất chỉ có liên kết cộng hóa trị là chất cộng hóa trị.
B. Hợp chất chỉ có liên kết ion là chất ion.
C. Một số hợp chất có cả liên kết ion và liên kết cộng hóa trị.
D. Ở điều kiện thường, hợp chất ở thể rắn là chất ion.
Lời giải:
Đáp án đúng là: D
Đáp án D không đúng, vì hợp chất ở thể rắn có thể là chất cộng hóa trị (đường, paraffin, …)
Bài 6.9 trang 19 SBT Khoa học tự nhiên 7: Phát biểu nào sau đây đúng?
A. Hợp chất ion và chất cộng hóa trị đều bền với nhiệt.
B. Hợp chất ion và chất cộng hóa trị đều tan tốt trong nước.
C. Khi các chất ion và chất cộng hóa trị tan trong nước đều tạo dung dịch có khả năng dẫn điện được.
D. Các chất ion luôn ở thể rắn.
Lời giải:
Đáp án đúng là: D
A sai vì một số hợp chất cộng hóa trị kém bền với nhiệt.
B sai vì nhiều hợp chất khó tan hoặc không tan trong nước.
C sai vì có hợp chất tan trong nước tạo dung dịch không có khả năng dẫn điện.
Bài 6.10 trang 19 SBT Khoa học tự nhiên 7: Có các phát biểu sau:
(a) Tất cả các chất ion đều ở thể rắn.
(b) Tất cả các chất ion đều tan trong nước và tạo thành dung dịch có khả năng dẫn điện.
(c) Khi đun sodium chloride rắn ở nhiệt độ cao sẽ được sodium chloride lỏng, dẫn điện.
(d) Đường tinh luyện và muối ăn đều là chất rắn tan được trong nước tạo dung dịch dẫn điện.
Số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án đúng là: C
(d) sai vì dung dịch nước đường không dẫn điện.
Bài 6.11 trang 20 SBT Khoa học tự nhiên 7: Có các phát biểu sau:
a) Ở điều kiện thường, các chất ion đều ở thể rắn.
b) Ở điều kiện thường, các hợp chất ở thể lỏng đều là chất cộng hóa trị.
c) Hợp chất của kim loại khó bay hơi, khó nóng chảy, dễ tan trong nước tạo thành dung dịch dẫn được điện.
d) Hợp chất chỉ gồm các nguyên tố phi kim thường dễ bay hơi, kém bền với nhiệt.
e) Hợp chất tan được trong nước thành dung dịch không dẫn điện thường là chất cộng hóa trị.
Số phát biểu đúng là
A. 5.
B. 4.
C. 3.
D. 2.
Lời giải:
Cả 5 phát biểu đều đúng.
Bài 6.12 trang 20 SBT Khoa học tự nhiên 7: Có các phát biểu sau:
a) Trong hợp chất, kim loại luôn nhường electron, phi kim luôn nhận electron.
b) Để có 8 electron ở lớp vỏ ngoài cùng thì nguyên tử aluminium hoặc nhường 3 electron hoặc nhận 5 electron.
c) Liên kết trong hợp chất tạo bởi magnesium và chlorine là liên kết ion.
d) Trong phân tử, hợp chất gồm các nguyên tố C, H, O chỉ có liên kết cộng hóa trị.
e) Khi tạo liên kết hóa học, nguyên tử chlorine chỉ tạo ion âm bằng cách nhận thêm 1 electron.
Số phát biểu đúng là
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án đúng là: B
Các phát biểu đúng là (c); (d).
a) Để tạo ion dương thì (1) …. sẽ (2) ….. Số electron (3) …. bằng (4) ….
b) Để tạo ion âm thì (5) … sẽ (6) …. Số electron (7) … bằng (8) ….
Lời giải:
a) Để tạo ion dương thì (1) kim loại sẽ (2) nhường electron. Số electron (3) nhường bằng (4) số electron lớp ngoài cùng.
b) Để tạo ion âm thì (5) phi kim sẽ (6) nhận electron. Số electron (7) nhận bằng (8) 8 – số electron lớp ngoài cũng.
a) Chất ion luôn chứa nguyên tố (1)…., ở điều kiện thường luôn ở (2)…
b) Ở điều kiện thường, chất ở thể khí luôn là (3)… Chất này có thể (4)…., tạo dung dịch có khả năng (5)…
Lời giải:
a) Chất ion luôn chứa nguyên tố (1) kim loại, ở điều kiện thường luôn ở (2) thể rắn.
b) Ở điều kiện thường, chất ở thể khí luôn là (3) chất cộng hóa trị. Chất này có thể (4) tan được trong nước, tạo dung dịch có khả năng (5) dẫn điện hoặc không dẫn điện.

Lời giải:
- Các ứng dụng khác của magnesium oxide: Xử lí đất, nước ngầm, xử lí nước thải, xử lí nước uống bằng cách ổn định độ pH. Magnesium oxide còn được sử dụng làm thuốc dịu cơn đau, ợ nóng và chua của chứng đau dạ dày, khó tiêu, ổn định tính acid của dạ dày,…
- Sơ đồ hình thành liên kết tạo ra phân tử magnesium oxide:
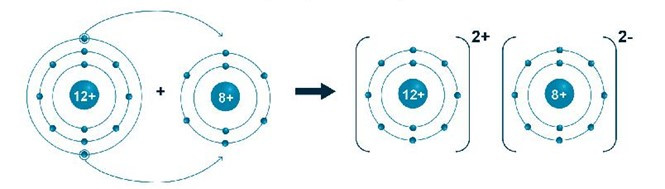
- Khối lượng phân tử magnesium oxide = 24 + 16 = 40 (amu).
Lời giải:
Chất khó bay hơi, khó nóng chảy, dễ tan trong nước tạo dung dịch dẫn được điện là chất ion.
Ví dụ hai chất có tính chất trên là:
+ Muối ăn (sodium chloride, NaCl) gồm 1 nguyên tử Na và 1 nguyên tử Cl.
+ Calcium chloride (CaCl2) gồm 1 nguyên tử Ca và 2 nguyên tử Cl.

Lời giải:
Phân tử acetic acid là chất cộng hóa trị do phân tử gồm các nguyên tố phi kim, điều kiện thường ở thể lỏng.
Khối lượng phân tử acetic acid là: 12 . 2 + 1 . 4 + 16 . 2 = 60 (amu).
Lời giải:
Chất (A) có khối lượng phân tử > 30 amu, thể khí, là nguyên nhân gây ra hiệu ứng nhà kính vậy (A) là carbon dioxide.
Carbon dioxide thể khí, được tạo thành từ các nguyên tử phi kim liên kết trong phân tử carbon dioxide là liên kết cộng hóa trị.
Sơ đồ hình thành liên kết trong phân tử carbon dioxide:
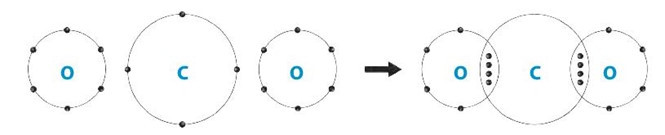
Lời giải:
Nguyên tố T là oxygen.
+ Phân tử đơn chất là khí oxygen (gồm 2 nguyên tử oxygen), khối lượng phân tử là:
16 . 2 = 32 (amu).
+ Phân tử hợp chất có liên kết ion là magnesium oxide (gồm 1 nguyên tử Mg và 1 nguyên tử O), khối lượng phân tử là: 24 + 16 = 40 (amu).
+ Phân tử hợp chất có liên kết cộng hóa trị là carbon dioxide (gồm 1 nguyên tử C và 2 nguyên tử O), khối lượng phân tử là: 12 + 16 . 2 = 44 (amu).

Lời giải:
Các nguyên tố trong phân tử glucose chỉ gồm các nguyên tố phi kim nên trong phân tử glucose chỉ có liên kết cộng hóa trị.
Khối lượng phân tử: 12 . 6 + 1 . 12 + 16 . 6 = 180 (amu).
Lời giải:
(B) là potassium iodide. Trong phân tử (B) có liên kết ion nên (B) là hợp chất ion.
Phân tử (B) gồm 1 nguyên tử K (potassium) và 1 nguyên tử I (iodine).
Khối lượng phân tử (B) là: 39 + 127 = 166 (amu).

Lời giải:
Khối lượng phân tử (D) = khối lượng nguyên tử (M) + x. khối lượng nguyên tử (Cl)
Với x là số nguyên tử Cl.
Thay số vào ta được: 135 = khối lượng nguyên tử (M) + x . 35,5
+ Với x = 1, khối lượng nguyên tử (M) = 99,5 amu (loại)
+ Với x = 2, khối lượng nguyên tử (M) = 64 amu (thỏa mãn).
Vậy M là Cu.
Vì phân tử (D) chứa Cu và Cl nên trong phân tử (D) có liên kết ion.
Xem thêm các bài giải SBT Khoa học tự nhiên lớp 7 Chân trời sáng tạo hay, chi tiết khác:
Bài 5: Phân tử - đơn chất - hợp chất
Bài 6: Giới thiệu về liên kết hóa học
Bài 7: Hóa trị và công thức hóa học
Bài 9: Đồ thị quãng đường - thời gian
Lý thuyết KHTN 7 Bài 6: Giới thiệu về liên kết hóa học
I. Vỏ nguyên tử khí hiếm
- Nhóm khí hiếm là nhóm các nguyên tố hoạt động hóa học kém.
Nhóm khí hiếm gồm: helium (He); neon (Ne); argon (Ar); krypton (Kr); xenon (Xe), …
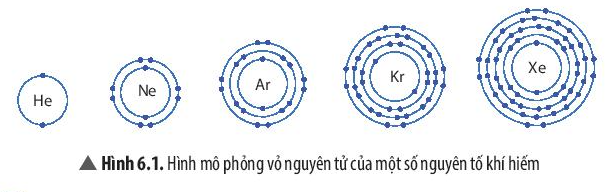
- Vỏ nguyên tử của các nguyên tố khí hiếm đều có 8 electron ở lớp ngoài cùng, riêng helium ở lớp ngoài cùng có 2 electron.
Chú ý:
Để có số electron ở lớp ngoài cùng giống nguyên tử của nguyên tố khí hiếm, các nguyên tử của các nguyên tố có khuynh hướng nhường hoặc nhận hoặc góp chung electron.
+ Nguyên tử của các nguyên tố kim loại thường có khuynh hướng nhường electron ở lớp ngoài cùng.
+ Nguyên tử của các nguyên tố phi kim thường có khuynh hướng nhận thêm hoặc góp chung electron để có lớp electron ngoài cùng bền vững.
II. Liên kết ion
1. Sự tạo thành ion dương
- Các nguyên tử của nguyên tố kim loại thường có xu hướng nhường electron ở lớp ngoài cùng để có lớp electron ngoài cùng giống nguyên tử của nguyên tố khí hiếm gần nhất trong bảng tuần hoàn.
- Nguyên tử kim loại khi nhường electron sẽ tạo thành ion dương tương ứng.
Ví dụ: Nguyên tử magnesium nhường 2 electron lớp ngoài cùng tạo thành ion magnesium. Ion magnesium là ion dương, có 8 electron lớp ngoài cùng, cấu hình electron giống với khí hiếm Ne.
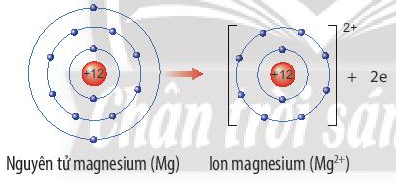
Hay viết gọn: Mg → Mg2+ + 2e
2. Sự tạo thành ion âm
- Các nguyên tử của nguyên tố phi kim (Cl, O, N …) có số electron lớp ngoài cùng là 7, 6, 5, … nên khi kết hợp với các nguyên tử kim loại, nguyên tử phi kim có xu hướng nhận electron từ nguyên tử kim loại để có lớp ngoài cùng giống nguyên tử của nguyên tố khí hiếm gần nhất trong bảng tuần hoàn.
- Nguyên tử phi kim khi nhận electron sẽ tạo thành ion âm tương ứng.
Ví dụ: Nguyên tử oxygen nhận thêm 2 electron vào lớp ngoài cùng tạo thành ion oxygen. Ion oxygen có 8 electron lớp ngoài cùng, cấu hình electron giống với nguyên tử khí hiếm Ne.

Hay viết gọn: O + 2e → O2-
3. Sự tạo thành liên kết ion
- Khi nguyên tử kim loại kết hợp với nguyên tử phi kim, nguyên tử kim loại nhường electron tạo thành ion dương, đồng thời nguyên tử phi kim nhận electron tạo thành ion âm.
- Ion âm và ion dương mang điện tích trái dấu, hút nhau, tạo thành liên kết ion.
Ví dụ 1: Sơ đồ tạo thành liên kết ion trong phân tử NaCl (sodium chloride).
Nguyên tử sodium nhường 1 electron tạo thành ion sodium (điện tích dương), nguyên tử chlorine nhận 1 electron tạo thành ion chlorine (điện tích âm), hai ion trên trái dấu nên hút nhau tạo thành phân tử sodium chlorine.
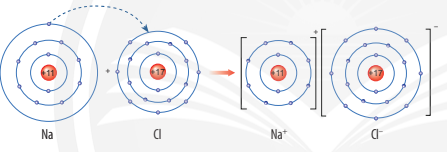
Ví dụ 2: Sơ đồ tạo thành liên kết ion trong phân tử MgO (magnesium oxide).
Nguyên tử magnesium nhường 2 electron tạo thành ion magnesium (điện tích dương), nguyên tử oxygen nhận 2 electron tạo thành ion oxygen (điện tích âm), hai ion trên trái dấu nên hút nhau tạo thành phân tử magnesium oxide
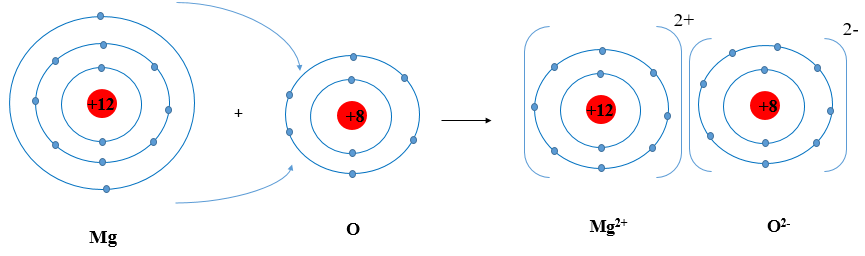
Kết luận:
- Liên kết ion là liên kết giữa ion dương và ion âm.
- Các ion dương và ion âm đơn nguyên tử có lớp electron ngoài cùng giống với nguyên tử của nguyên tố khí hiếm.
III. Liên kết cộng hóa trị
- Liên kết cộng hóa trị là liên kết được hình thành bởi sự dùng chung electron giữa hai nguyên tử.
- Liên kết cộng hóa trị thường là liên kết giữa hai nguyên tử của nguyên tố phi kim với phi kim.
Ví dụ 1: Quá trình tạo thành liên kết cộng hóa trị trong phân tử chlorine:
+ Nguyên tử Cl có 7 electron lớp ngoài cùng và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử Cl liên kết với nhau, mỗi nguyên tử góp 1 electron để tạo ra đôi electron dùng chung.
+ Hạt nhân của hai nguyên tử Cl cùng hút đôi electron dùng chung và liên kết với nhau tạo thành phân tử chlorine.
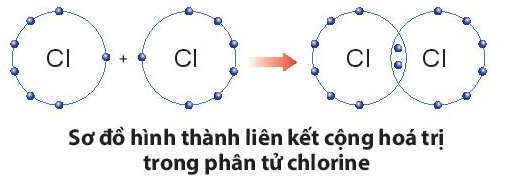
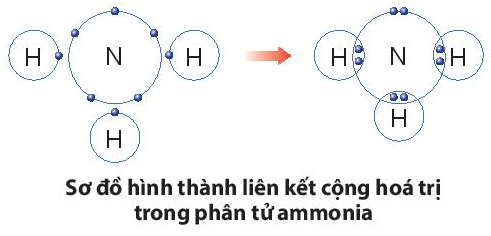
Ví dụ 2: Quá trình tạo thành liên kết cộng hóa trị trong phân tử ammonia:
+ Nitrogen thuộc nhóm VA, có 5 electron lớp ngoài cùng, nguyên tử nitrogen sẽ góp chung 3 electron.
+ Hydrogen thuộc nhóm IA, có 1 electron lớp ngoài cùng, mỗi nguyên tử hydrogen sẽ góp chung 1 electron, theo sơ đồ sau:
IV. Chất ion, chất cộng hóa trị
- Chất được tạo bởi các ion dương và ion âm được gọi là chất ion.
Ví dụ một số hợp chất ion:

- Chất được tạo thành nhờ liên kết cộng hóa trị được gọi là chất cộng hóa trị.
Ví dụ một số hợp chất cộng hóa trị:

- Ở điều kiện thường, chất ion thường ở thể rắn, chất cộng hóa trị ở thể rắn, thể lỏng hoặc thể khí.
V. Một số tính chất của chất ion và chất cộng hóa trị
- Chất ion khó bay hơi, khó nóng chảy, khi tan trong nước tạo dung dịch dẫn được điện.
- Chất cộng hóa trị thường dễ bay hơi, kém bền với nhiệt; một số chất tan được trong nước thành dung dịch. Tùy thuộc vào chất cộng hóa trị khi tan trong nước mà dung dịch thu được có thể dẫn điện hoặc không dẫn điện.
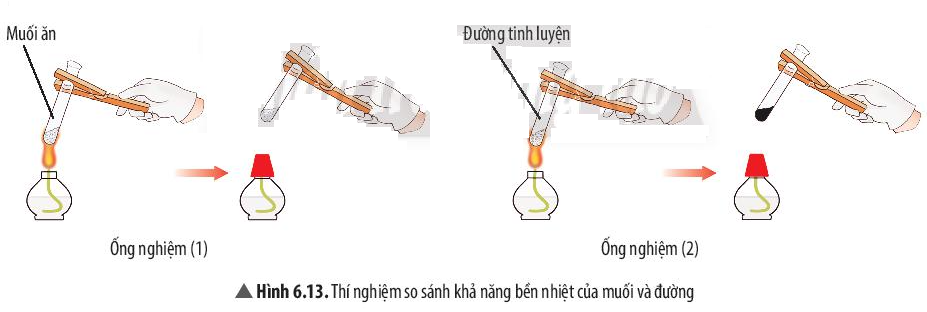
- Ví dụ 1: Dung dịch nước muối dẫn điện còn dung dịch nước đường thì không dẫn điện.
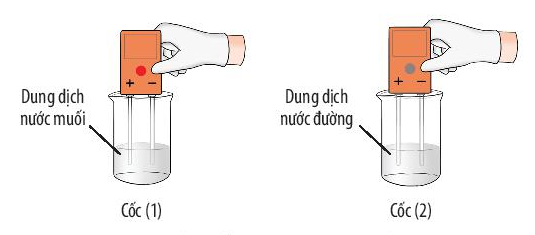
Ví dụ 2: Đường nóng chảy và biến đổi thành chất khác có màu đen. Muối ăn không bị nóng chảy.