Với giải Bài 12.18 trang 54 SBT Hóa Học lớp 11 Chân trời sáng tạo chi tiết trong Bài 12: Alkane giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa Học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 12: Alkane
Bài 12.18 trang 54 SBT Hóa học 11: Phân tích thành phần nguyên tố của hợp chất hữu cơ (X) thu được kết quả %C và %H (theo khối lượng) lần lượt là 84,21% và 15,79%. Phân tử khối của hợp chất (X) này được xác định thông qua kết quả phổ khối lượng) như hình bên dưới với peak ion phân tử có giá trị m/z lớn nhất.
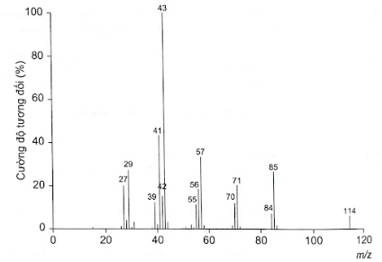
a) Xác định công thức phân tử của (X).
b) Nếu không có kết quả phân tích phổ khối lượng của (X), trình bày cách xác định công thức phân tử của (X) dựa trên những dữ kiện em đã biết.
Lời giải:
a) Vì
nên phân tử (X) chỉ chứa nguyên tố hydrogen và carbon.
Gọi công thức phân tử của (X) là CxHy.
Khối lượng mol phân tử của (X) được xác định trên phổ khối lượng tương ứng với peak có giá trị m/z lớn nhất. Do đó, từ phổ khối lượng của (X), ta có:
Vậy công thức phân tử của (X) là C8H18.
b) Vì nên phân tử (X) chỉ chứa nguyên tố hydrogen và carbon.
Gọi công thức đơn giản nhất của (X) là CxHy.
=> Công thức đơn giản nhất của (X) là (C4H9)n hay C4nH9n.
Vì trong hợp chất CxHyOz bất kì, ta có:
+) Với n = 1, công thức phân tử của (X) là C4H9
=> Loại trường hợp này vì số H trong hợp chất hydrocarbon luôn luôn là số chẵn.
+) Với n = 2, công thức phân tử của (X) là C8H18 (nhận).
Vậy công thức phân tử của (X) là C8H18.
Xem thêm lời giải Sách bài tập Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Bài 12.1 trang 51 SBT Hóa học 11: Theo ước tính, trung bình mỗi ngày một con bò “ợ” vào bầu khí quyển khoảng 250 L – 300 L một chất khí có khả năng gây hiệu ứng nhà kính. Khi đó là.....
Bài 12.2 trang 51 SBT Hóa học 11: Biogas là một loại khí sinh học, được sản xuất bằng cách ủ kín các chất thải hữu cơ trong chăn nuôi, sinh hoạt. Biogas được dùng để đun nấu, chạy máy phát điện sinh hoạt gia đình. Thành phần chính của biogas là....
Bài 12.3 trang 51 SBT Hóa học 11: Đồ thị dưới đây thể hiện mối tương quan giữa nhiệt độ sôi và số nguyên tử carbon trong phân tử alkane không phân nhánh được biểu diễn như sau:....
Bài 12.4 trang 52 SBT Hóa học 11: Alkane (A) có công thức phân tử C5H12. (A) tác dụng với chlorine khi đun nóng chỉ tạo một dẫn xuất monochloro duy nhất. Tên gọi của (A) là....
Bài 12.5 trang 52 SBT Hóa học 11: Có bao nhiêu alkane (có số nguyên tử C ≤ 5) khi tác dụng với chlorine (có ánh sáng hoặc đun nóng) tạo duy nhất một sản phẩm thế monochloro?...
Bài 12.6 trang 52 SBT Hóa học 11: Khi cho 2,2-dimethylbutane tác dụng với chlorine thu được tối đa bao nhiêu dẫn xuất monochloro?....
Bài 12.7 trang 52 SBT Hóa học 11: Cho alkane sau:....
Bài 12.8 trang 52 SBT Hóa học 11: Để hoàn thành bài tập gọi tên các đồng phân của alkane có công thức phân tử là C4H10, một bạn học sinh đã vẽ các dạng mạch carbon của alkane này, biết rằng dạng mạch carbon này chỉ chứa các liên kết đơn có thể có, sau đó bạn tiếp tục bổ sung các nguyên tử hydrogen vào dạng mạch carbon để hoàn tất bài tập. Theo em, học sinh đó đã sai ở điểm nào......
Bài 12.9 trang 53 SBT Hóa học 11: So sánh và giải thích nhiệt độ sôi của alkane mạch không phân nhánh với alkane mạch phân nhánh khi chúng có cùng số nguyên tử carbon trong phân tử....
Bài 12.10 trang 53 SBT Hóa học 11: Mặc dù có 5 nguyên tử carbon trong phân tử nhưng neopentane (2,2-dimethylpropane) ở thể khí trong điều kiện thường. Giải thích....
Bài 12.11 trang 53 SBT Hóa học 11: Em hãy cho biết xăng có tan được trong nước hay không và chất béo có tan được trong xăng hay không. Theo em, bác thợ sửa xe thường rửa tay bằng gì để sạch các vết dầu mỡ?....
Bài 12.12 trang 53 SBT Hóa học 11: Vì sao khi tiếp xúc lâu dài với xăng sẽ làm cho da bị phồng rộp và gây đau nhức?.....
Bài 12.13 trang 53 SBT Hóa học 11: Butane là chất lỏng có thể nhìn thấy bên trong một chiếc bật lửa trong suốt, có nhiệt độ sôi thấp hơn một ít so với nhiệt độ của nước đóng băng (–0,5 °C). Tuy nhiên vì sao butane trong bật lửa lại không sôi...
Bài 12.14 trang 53 SBT Hóa học 11: Cho 2-methylpropane tác dụng với chlorine (tỉ lệ mol 1 : 1, có ánh sáng) thu được tối đa bao nhiêu sản phẩm thế monochloro?....
Bài 12.15 trang 53 SBT Hóa học 11: Khi cho 2-methylpropane tác dụng với bromine ở 127 °C thu được hỗn hợp 2 sản phẩm thế monobromo là 1-bromo-2-methylpropane (0,56%) và 2-bromo-2-methylpropane (99,44%). Xác định tỉ lệ khả năng phản ứng tương đối của nguyên tử hydrogen gắn ở nguyên tử carbon bậc I và nguyên tử carbon bậc III trong phản ứng.....
Bài 12.16 trang 53 SBT Hóa học 11: Trong phản ứng thế của propane với chlorine ở nhiệt độ phòng khi có ánh sáng, tỉ lệ khả năng phản ứng tương đối của nguyên tử hydrogen gắn ở nguyên tử carbon bậc I và nguyên tử carbon bậc II tương ứng là 1 : 4.....
Bài 12.17 trang 54 SBT Hóa học 11: Giải thích tại sao các bể chứa xăng thường được quét một lớp nhũ màu trắng bạc?...
Bài 12.18 trang 54 SBT Hóa học 11: Phân tích thành phần nguyên tố của hợp chất hữu cơ (X) thu được kết quả %C và %H (theo khối lượng) lần lượt là 84,21% và 15,79%. Phân tử khối của hợp chất (X) này được xác định thông qua kết quả phổ khối lượng) như hình bên dưới với peak ion phân tử có giá trị m/z lớn nhất....
Bài 12.19* trang 54 SBT Hóa học 11: Gọi tên alkane sau theo danh pháp thay thế:...
Bài 12.20* trang 55 SBT Hóa học 11: Chỉ số octane (octane number) là đại lượng đặc trưng cho yếu tố đo lường khả năng chống kích nổ của một nhiên liệu khi nhiên liệu này bốc cháy với không khí bên trong xi lanh của động cơ đốt trong. Nếu chỉ số octane của một mẫu xăng thấp, xăng sẽ tự cháy mà không do bu-gi bật tia lửa điện đốt. Điều này làm cho hiệu suất động cơ giảm và sẽ hư hao các chi tiết máy.....
Bài 12.21* trang 55 SBT Hóa học 11: Ethanol có thể làm tăng chỉ số octane của xăng không?...
Bài 12.22* trang 55 SBT Hóa học 11: Thế nào là xăng RON 92? RON 95? Xăng nào có chỉ số octane cao hơn?....
Bài 12.23* trang 55 SBT Hóa học 11: Tính chỉ số octane của xăng E5 và xăng E10...
Xem thêm các bài giải SBT Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
