Với giải sách bài tập Hóa học 11 Bài 12: Alkane sách Chân trời sáng tạo hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Bài 12: Alkane
A. O2.
B. CO2.
C. CH4.
D. NH3.
Lời giải:
CO2 và CH4 có khả năng gây hiệu ứng nhà kính. Tuy nhiên, CH4 là khí do bò “ợ” ra.
→ Chọn C.
A. N2.
B. CO2.
C. CH4.
D. NH3.
Lời giải:
Thành phần chính của biogas là methane (CH4).
→ Chọn C.
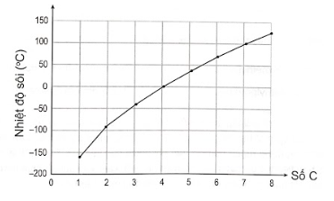
Đồ thị biểu diễn mối tương quan giữa nhiệt độ sôi và số nguyên tử carbon trong phân tử alkane không phân nhánh
Dựa vào đồ thị đã cho, số phân tử alkane không phân nhánh ở thể khí trong điều kiện thường là
A. 4.
B. 2.
C. 3.
D. 1.
Lời giải:
Trên đồ thị, ta thấy có 4 alkane có nhiệt độ sôi nhỏ hơn nhiệt độ phòng. Do đó, 4 alkane này ở thể khí trong điều kiện thường.
→ Chọn A.
A. pentane.
B. 2-methylbutane.
C. 2,2-dimethylpropane.
D. 3-methylbutane.
Lời giải:
Alkane có công thức phân tử C5H12, tạo ra một dẫn xuất monochloro duy nhất là 2,2 – dimethylpropane.
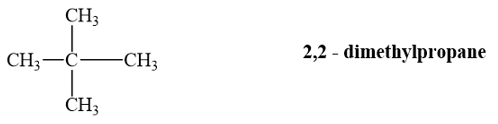
→ Chọn C.
A. 3.
B. 2.
C. 1.
D. 4.
Lời giải:
Các alkane (có số nguyên tử C ≤ 5) khi tác dụng với chlorine (có ánh sáng hoặc đun nóng) tạo duy nhất một sản phẩm thế monochloro:

→ Chọn A.
A. 3.
B. 2.
C. 5.
D. 4.
Lời giải:
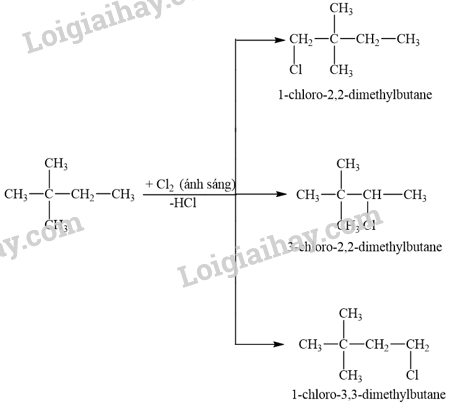
Khi cho 2,2-dimethylbutane tác dụng với chlorine thu được 3 dẫn xuất monochloro.
→ Chọn A.
Bài 12.7 trang 52 SBT Hóa học 11: Cho alkane sau:
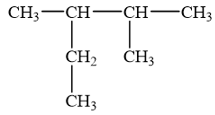
Danh pháp thay thế của alkane trên là
A. 2-ethyl-3-methylbutane.
B. 2-methyl-3-ethylbutane.
C. 3,4-dimethylpentane.
D. 2,3-dimethylpentane.
Lời giải:
Cần chọn mạch chính dài nhất (5 nguyên tử C), nhiều nhánh nhất (hai nhánh). Đánh số thứ tự theo chiều sao cho tổng chỉ số của các nhánh là nhỏ nhất (vị trí số 1 ở đầu mạch carbon và gần nhánh nhất).
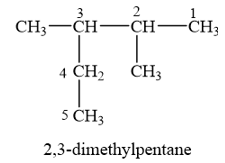
→ Chọn D.
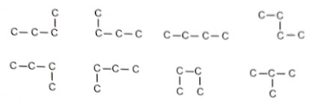
Lời giải:
4 nguyên tử carbon chỉ chứa liên kết đơn có thể được “bẻ” theo nhiều cách khác nhau vì các liên kết C−C có thể quay tự do. Trong hình trên, có 7 cách quay các liên kết C—C trong hình mà vẫn không làm đổi bản chất giữa chúng. Do đó bạn học sinh này chỉ đưa ra được 2 đồng phân của C4H10.
Lời giải:
Các phân tử alkane phân nhánh có nhiệt độ sôi thấp hơn các phân tử alkane không phân nhánh dù cho chúng có cùng số nguyên tử carbon. Điều này được giải thích vì các phân tử alkane không phân nhánh có diện tích bề mặt lớn hơn so với phân tử alkane phân nhánh nên tồn tại tương tác van der Waals giữa các phân tử lớn hơn, dẫn đến nhiệt độ sôi cao hơn.
Lời giải:
Trong số 3 đồng phân của C5H12, neopentane có cấu trúc đối xứng cao, phân tử xem như có dạng hình cầu nên tương tác van der Waals giữa các phân tử neopentane rất yếu, dẫn đến nhiệt độ sôi của neopentane là 9,5 °C. Điều này làm cho phân tử neopentane ở thể khí trong điều kiện thường (hai đồng phân còn lại là pentane có nhiệt độ sôi ở 36 °C và isopentane có nhiệt độ sôi ở 27,8 °C nên trong điều kiện thường, chúng ở thể lỏng).
Lời giải:
Xăng có thành phần chính là các phân tử alkane có số nguyên tử carbon từ 7 – 11 nguyên tử.
Vì xăng là các phân tử không phân cực trong khi nước là phân tử phân cực, nên xăng không tan được trong nước.
Đồng thời, chất béo là hợp chất không phân cực nên chất béo cũng tan được trong xăng. Dầu mỡ sửa chữa xe cũng là các phân tử alkane nên không thể tan được trong nước, điều đó được hiểu là dầu mỡ trên tay bác thợ sửa chữa xe không thể làm sạch chỉ bởi nước. Bác thợ sửa xe thường dùng dầu hoả (là các phân tử alkane có số nguyên tử carbon từ 12 – 15 nguyên tử) để hoà tan các vết dầu mỡ, sau đó rửa lại bằng xà phòng.
Lời giải:
Vì xăng hay dầu hỏa có thể hòa tan được lớp dầu trên da. Khi tiếp xúc lâu dài với xăng, dầu hoả, ... sẽ làm cho lớp dầu bảo vệ da bị trôi đi, da không còn lớp dầu bảo vệ nên sẽ bị phồng rộp và gây đau nhức.
Khi tiếp xúc với xăng, dầu hoả, dung môi pha sơn, ... cần đeo găng tay cẩn thận.
Lời giải:
Butane trong bật lửa không sôi, mặc dù butane có nhiệt độ sôi thấp hơn một ít so với nhiệt độ của nước đóng băng (–0,5 °C), vì các lý do sau:
+ Khi được đưa vào trong bật lửa, butane chịu áp suất rất cao so với áp suất khí quyển. Điều này làm tăng nhiệt độ sôi của butane lên cao hơn nhiệt độ phòng. Do đó butane không thể sôi ở áp suất cao này.
+ Khi được giải nén, butane lỏng lập tức bốc hơi và tạo khí butane, bốc cháy khi gặp tia lửa do ma sát giữa bánh răng kim loại với đá lửa.
Lời giải:
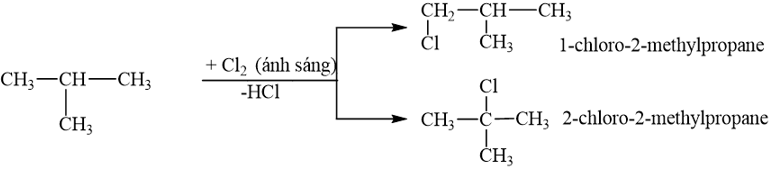
Cho 2-methylpropane tác dụng với chlorine (tỉ lệ mol 1 : 1, có ánh sáng) thu được 2 sản phẩm thế monochloro.
Lời giải:
2-methylpropane có công thức cấu tạo:
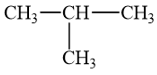
Như vậy 2-methylpropane có 9 nguyên tử hydrogen gắn ở nguyên tử carbon bậc I và 1 nguyên tử hydrogen gắn ở nguyên tử carbon bậc III. Gọi a và k là khả năng phản ứng tương đối của nguyên tử hydrogen gắn ở nguyên tử carbon bậc I và nguyên tử carbon bậc III trong phản ứng thế bromine đã cho.
Vì sản phẩm thế hydrogen vào carbon bậc I chiếm 0,56% nên ta có phương trình:
Chọn a = 1
Vậy với 2-methylpropane, tỉ lệ khả năng phản ứng tương đối của nguyên tử hydrogen gắn ở nguyên tử carbon bậc I và nguyên tử carbon bậc III trong phản ứng là 1 : 1 598.
a) Xác định tỉ lệ phần trăm các sản phẩm thế monochloro thu được trong phản ứng thế trên.
b) Dự đoán khả năng phản ứng và tỉ lệ phần trăm các sản phẩm thế thu được khi thay chlorine bằng bromine.
Lời giải:
a) Propane CH3–CH2–CH3 khi tác dụng với chlorine sẽ thu được 2 sản phẩm thế monochloro là CH3-CH2-CH2Cl và CH3-CHCl-CH3.
Vì tỉ lệ khả năng phản ứng tương đối của nguyên tử hydrogen gắn ở nguyên tử carbon bậc I và nguyên tử carbon bậc II tương ứng là 1 : 4 nên tổng khả năng phản ứng của 8 nguyên tử hydrogen (gồm 6 nguyên tử hydrogen gắn vào carbon bậc I và 2 nguyên tử hydrogen gắn vào carbon bậc II) là => Tỉ lệ phần trăm của sản phẩm CH3-CH2-CH2Cl là => Tỉ lệ phần trăm của sản phẩm CH3-CHCl-CH3 là
b) Phản ứng của propane với bromine sẽ xảy ra chậm hơn so với phản ứng của propane với chlorine. Tuy nhiên lúc này, do bromine có tính chọn lọc hơn so với chlorine nên khả năng phản ứng của nguyên tử carbon bậc II cao hơn nhiều so với của nguyên tử carbon bậc I, dẫn đến sản phẩm thế CH3–CHBr–CH3 sẽ chiếm tỉ lệ phần trăm cao hơn nhiều so với sản phẩm thế CH3–CH2–CH2Br.
Lời giải:
Lớp nhũ màu trắng bạc phản xạ tốt các tia nhiệt (hấp thụ các tia nhiệt kém) nên hạn chế được sự truyền nhiệt từ bên ngoài vào, nhờ đó xăng đỡ nóng hơn, tránh hiện tượng gây cháy nổ bể.
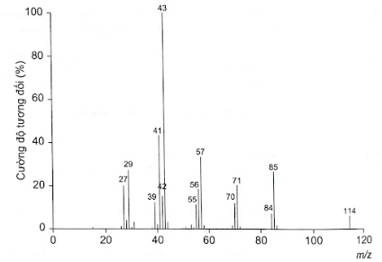
a) Xác định công thức phân tử của (X).
b) Nếu không có kết quả phân tích phổ khối lượng của (X), trình bày cách xác định công thức phân tử của (X) dựa trên những dữ kiện em đã biết.
Lời giải:
a) Vì
nên phân tử (X) chỉ chứa nguyên tố hydrogen và carbon.
Gọi công thức phân tử của (X) là CxHy.
Khối lượng mol phân tử của (X) được xác định trên phổ khối lượng tương ứng với peak có giá trị m/z lớn nhất. Do đó, từ phổ khối lượng của (X), ta có:
Vậy công thức phân tử của (X) là C8H18.
b) Vì nên phân tử (X) chỉ chứa nguyên tố hydrogen và carbon.
Gọi công thức đơn giản nhất của (X) là CxHy.
=> Công thức đơn giản nhất của (X) là (C4H9)n hay C4nH9n.
Vì trong hợp chất CxHyOz bất kì, ta có:
+) Với n = 1, công thức phân tử của (X) là C4H9
=> Loại trường hợp này vì số H trong hợp chất hydrocarbon luôn luôn là số chẵn.
+) Với n = 2, công thức phân tử của (X) là C8H18 (nhận).
Vậy công thức phân tử của (X) là C8H18.
Bài 12.19* trang 54 SBT Hóa học 11: Gọi tên alkane sau theo danh pháp thay thế:
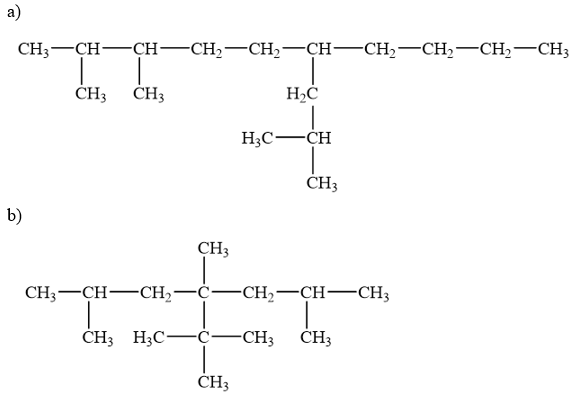
Phương pháp giải:
- Tên theo danh pháp thay thế của alkane:
+ Alkane không phân nhánh: Tiền tố ứng với số nguyên tử C trong alkane + ane.
+ Alkane phân nhánh: Sổ chỉ vị trí nhánh – Tên nhánh + Tiền tố ứng với số nguyên tử C trong alkane + ane.
- Lưu ý:
+ Để đọc tên nhánh này, carbon của nhánh phức tạp gắn vào mạch chính được đánh số 1. Tên nhánh phức tạp được cho vào ngoặc. Khi gọi tên nhánh, ưu tiên theo thứ tự chữ cái của nhánh, không ưu tiên theo chữ cái của các tiếp đầu ngữ iso, di, tri,... Ví dụ: isobutyl vẫn ưu tiên hơn dimethyl, mặc dù “i” đứng sau “d”.
Lời giải:
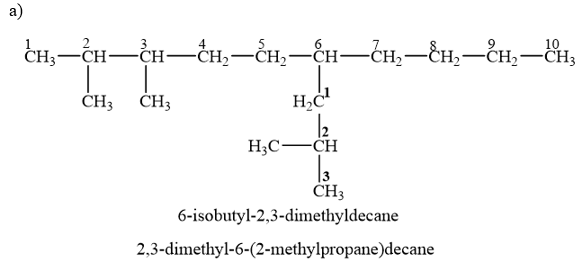
Người ta quy ước rằng chỉ số octane của 2,2,4-trimethylpentane là 100 và của heptane là 0. Các hydrocarbon mạch vòng và mạch phân nhánh có chỉ số octane cao hơn hydrocarbon mạch không phân nhánh.
Để xác định chỉ số octane của một mẫu xăng, người ta dùng máy đo chỉ số octane.
a) Chỉ số octane càng cao, chất lượng xăng sẽ như thế nào?
b) Trong thực tế, xăng không chỉ gồm 2,2,4-trimethylpentane và heptane mà là một hỗn hợp gồm nhiều hydrocarbon khác nhau. Giả thiết một mẫu xăng chỉ gồm 8 phần thể tích 2,2,4-trimethylpentane và 2 phần thể tích heptane thì chỉ số octane của mẫu xăng này là bao nhiêu?
Lời giải:
a) Chỉ số octane càng cao, độ chịu nén trước khi phát nổ của xăng càng lớn nên chất lượng xăng càng tốt. Ví dụ xăng có chỉ số octane 92 dễ bị cháy khi nén hơn so với xăng có chỉ số octane 95 nên xăng có chỉ số octane 95 giá trị hơn xăng có chỉ số octane 92. Tuy nhiên phải tuỳ vào tỉ số nén của động cơ để chọn xăng phù hợp. Động cơ có tỉ số nén thấp thì không cần dùng xăng có chỉ số octane cao.
b) Vì mẫu xăng trên chứa 80% thể tích là 2,2,4-trimethylpentane, nên chỉ số octane của mẫu xăng là 80.
Bài 12.21* trang 55 SBT Hóa học 11: Ethanol có thể làm tăng chỉ số octane của xăng không?
Lời giải:
Chỉ số octane là thước đo khả năng chống kích nổ của xăng. Ethanol có cấu trúc phân tử gồm các nguyên tử carbon và hydrogen liên kết đơn giản với nhau. Do đó ethanol có thể cháy ổn định hơn so với các phân tử xăng phức tạp khác. Ethanol có chỉ số octane cao hơn nhiều (khoảng 109) so với xăng. Khi trộn ethanol vào xăng với tỷ lệ nhất định, chỉ số octane trung bình của hỗn hợp sẽ được nâng lên, giúp xăng cháy ổn định và hiệu quả hơn trong động cơ.
Lời giải:
Xăng RON 92 là xăng có chỉ số octane 92.
Xăng RON 95 là xăng có chỉ số octane 95.
Do đó, xăng RON 95 có chỉ số octane cao hơn so với xăng RON 92.
Bài 12.23* trang 55 SBT Hóa học 11: Tính chỉ số octane của xăng E5 và xăng E10.
Lời giải:
Xăng E5 chứa 5% ethanol và 95% xăng RON 92 (theo thể tích).
=> Chỉ số octane của xăng E5 là:
Xăng E10 chứa 10% ethanol và 90% xăng RON 92 (theo thể tích).
=> Chỉ số octane của xăng E10 là:
Xem thêm các bài giải SBT Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác:
Bài 14: Arene (Hydrocarbon thơm)
Lý thuyết Alkane
1. Khái niệm về alkane
- Alkane là những hydrocarbon mạch hở chỉ chứa liên kết đơn trong phân tử và có công thức chung là CnH2n+2 (n1).
- Nguồn alkane trong tự nhiên: dầu mỏ, khí dầu mỏ, khí ao hồ.
2. Danh pháp
- Tên theo danh pháp thay thế của alkane không phân nhánh:
Tiền tố ứng với số nguyên tử carbon của alkane + ane
-Tên theo danh pháp thay thế của alkane phân nhánh
Số chỉ vị trí nhánh-Tên nhánh + Tiền tố ứng với số nguyên tử carbon mạch chính + ane
3. Tính chất vật lý
- Ở điều kiện thường, các alkane từ C1 đến C4 ở thể khí.
- Các alkane đều nhẹ hơn hơn nước, không tan truong nước, nhưng tan trong các dung môi không phân cực.
- Khi số nguyên tử carbon tăng, nhiệt độ sôi và nhiệt độ nóng chảy của các alkane tăng.
4. Tính chất hóa học
- Phản ứng thế halogen
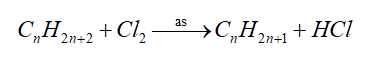
=> Phản ứng đặc trưng của alkane, nguyên tử H liên kết với nguyên tử C bậc cao dễ bị thế hơn nguyên tử H liên kết với nguyên tử C bậc thấp hơn.
- Phản ứng cracking: quá trình “bẻ gãy” các phân tử alkane mạch dài thành các phân tử hydrocarbon mạch ngắn hơn.
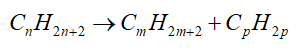
- Phản ứng reforming: quá trình biển đổi cấu trúc phân tử các alkane mạch không phân nhánh, mạch hở, không thơm thành các hydrocarbon có mạch nhánh hoặc mạch vòng.
- Phản ứng oxi hóa
+ Oxi hóa hoàn toàn: các alkane thường dễ cháy và tỏa nhiều nhiệt.
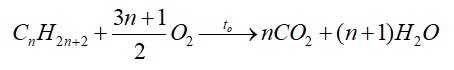
+ Oxi hóa không hoàn toàn: trong trường hợp thiếu oxygen, phản ứng cháy xảy ra không hoàn toàn, tạo CO và có thể có C.
5. Ứng dụng của alkane và điều chế alkane trong công nghiệp
- Alkane được sử dụng làm nhiên liệu, dung môi, dầu nhờn,… và nguyên liệu để tổng hợp các chất hữu cơ khác nhau.
- Trong công nghiệp, alkane được khai thác, chế biến từ khí thiên nhiên, khí đồng hành, dầu mỏ.
- Ô nhiễm không khí do khói thải từ các phương tiện giao thông góp phần làm Trái Đất nóng lên và gây ra sự biến đổi khí hậu toàn cầu.
- Tăng cường tham gia vận tải công cộng, giảm sự phụ thuộc nhiên liệu hóa thạch, bảo vệ rừng,… là những cách hạn chế sự ô nhiệm không khí.