Với giải sách bài tập Hóa học 11 Ôn tập chương 3 trang 48 sách Chân trời sáng tạo hay, chi tiết giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập trong SBT Hóa học 11. Mời các bạn đón xem:
Giải SBT Hóa học 11 Ôn tập chương 3 trang 48
A. chưng cất.
B. chiết.
C. kết tinh.
D. sắc kí.
Lời giải:
Để tách các chất lỏng có nhiệt độ sôi khác nhau thường dùng phương pháp chưng cất.
→ Chọn A.
A. chưng cất.
B. chiết.
C. kết tinh.
D. sắc kí.
Lời giải:
Để tách các chất từ một hỗn hợp lỏng không đồng nhất thường dùng phương pháp chiết.
→ Chọn B.
A. chưng cất.
B. chiết.
C. kết tinh.
D. sắc kí.
Lời giải:
Để tinh chế các chất rắn tan ra khỏi dung dịch thường dùng phương pháp kết tinh.
→ Chọn C.
Bài OT3.4 trang 48 SBT Hóa học 11: Cặp chất nào sau đây là đồng phân của nhau?
A. CH3COOH, HCOOCH3.
B. CH3OOH, HCOOH.
C. CH3OH, C2H5OH.
D. C2H5OH, CH3OCH2CH3.
Lời giải:
|
Công thức cấu tạo |
Công thức phân tử |
|
CH3COOH |
C2H4O2 |
|
HCOOCH3 |
C2H4O2 |
|
HCOOH |
CH2O2 |
|
CH3OH |
CH4O |
|
C2H5OH |
C2H6O |
|
CH3OCH2CH3 |
C3H8O |
Vì CH3COOH và HCOOCH3 đều có công thức phân tử là C2H4O2 nên CH3COOH và HCOOCH3 là đồng phân của nhau.
→ Chọn A.
Bài OT3.5 trang 48 SBT Hóa học 11: Cặp chất nào sau đây là đồng đẳng của nhau?
A. CH4, CH3-CH2-CH2-CH3.
B. CH3OCH3, CH3-CH2OH.
C. HCHO, CH3COOH.
D. CH2OH-CH2OH, C3H5(OH)3.
Lời giải:
CH4, CH3-CH2-CH2-CH3 là đồng đẳng của nhau, chúng đều là những alkane no, đơn, hở.
CH3OCH3 là ether, CH3-CH2OH là alcohol no, đơn hở. Hai chất này khác nhau về tính chất hóa học.
HCHO là aldehyde, CH3COOH là carboxylic acid. Hai chất này khác nhau về tính chất hóa học.
CH2OH-CH2OH, C3H5(OH)3 đều là polyalcohol, nhưng trong phân tử mỗi chất này lại khác nhau một nhóm (-CH(OH)) nên chúng không phải là đồng đẳng của nhau.
→ Chọn A.
Lời giải:
Chất hữu cơ: CH3–CH2–CH3, CH2=CH–CH2CH3, NaOOC-COONa, CH2OH-CH2OH, H-CH=O.
Chất vô cơ: AlCl3, HNO3, Ba(OH)2, Na2CO3, CO, CaC2, NaCN.
Lời giải:
Hydrocarbon: CH4, CH2=CH2, CH2=C(CH3)-CH=CH2, CH≡CH.
Dẫn xuất của hydrocarbon: CH3–CH2-NH2, CH3-COOH, C3H5(OH)3, C6H5OH, CH3CHO, CH3COOCH2CH3, H2N–CH(CH3)-COOH.
– Giai đoạn 1 (xử lí nguyên liệu): Sau khi lấy về, quả hồi phải được xử lí sơ bộ nhằm loại bỏ các tạp chất cơ học chứa lẫn như lá, cành vụn, cây, đất cát ... (không nên loại bỏ cuống của quả hồi vì cuống quả hồi có chứa một hàm lượng tinh dầu khá cao, từ 5,49% – 6,01%).
– Giai đoạn 2 (cản dập): Sau khi xử lí, nguyên liệu quả hồi dùng để chưng cất nên được cán dập.
– Giai đoạn 3: Chiết xuất tinh dầu hồi dựa trên cơ sở nhiệt độ sôi khác nhau giữa tinh dầu và nước có trong nguyên liệu.
– Giai đoạn 4: Tinh dầu hồi thu được ở giai đoạn 3 vẫn còn lẫn một ít nước, dù không đáng kể nhưng sẽ làm ảnh hưởng lớn đến chất lượng của tinh dầu hồi. Do đó, sau khi hoàn thành giai đoạn 3, tinh dầu hồi phải được khử nước bằng cách để lắng yên một ngày đêm trong phễu, sau đó tiến hành tách bỏ lớp nước phía dưới. Để dễ dàng hơn cho quá trình phân lớp, có thể cho thêm một ít muối ăn để làm tăng tỉ trọng của nước còn lẫn trong tinh dầu. Sau khi tách bỏ lớp nước phía dưới, lớp tinh dầu còn lại phía trên phễu vẫn còn chứa lẫn một lượng nước rất ít và sẽ được khử bỏ bằng cách xử lí với Na2SO4 khan.
Hãy cho biết phương pháp tách và tinh chế nào được sử dụng ở giai đoạn 3 và giai đoạn 4 trong quy trình trên.
Lời giải:
Phương pháp tách và tinh chế được sử dụng ở giai đoạn 3: phương pháp chưng cất.
Phương pháp tách và tinh chế được sử dụng ở giai đoạn 4: phương pháp chiết.
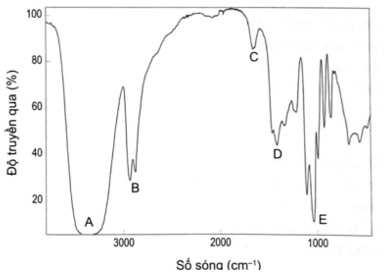
Lời giải:
Số sóng (peak) đặc trưng của nhóm chức OH nằm trong khoảng 3600 – 3300 (cm-1)
→ Peak đặc trưng với số sóng tương ứng của nhóm -OH trên phổ IR của X là A.
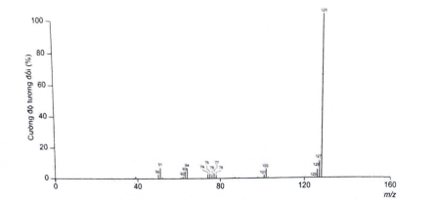
Lời giải:
Naphthalene là một hydrocarbon, do đó ta gọi công thức phân tử của naphthalene là CxHy.
%mH = 100% - 83,75% = 6,25%
Khối lượng mol phân tử của naphthalene được xác định trên phổ khối lượng tương ứng với peak có giá trị m/z lớn nhất. Do đó, từ phổ khối lượng của naphthalene, ta có:
Vậy công thức phân tử của naphthalene là C10H8.
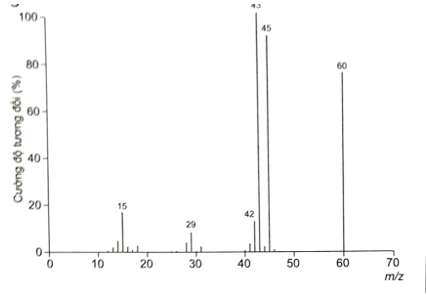
a) Lập công thức phân tử của acetic acid, biết kết quả phân tích nguyên tố của acetic acid có 40% C; 53,33% O về khối lượng; còn lại là H. Phân tử khối của acetic acid được xác định trên phổ khối lượng tương ứng với peak có giá trị m/z lớn nhất
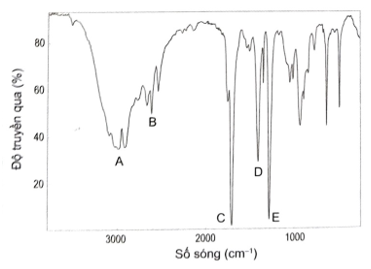
b) Dựa vào phổ IR bên, hãy cho biết có thể xác định được nhóm chức carboxyl có trong acetic acid từ peak nào.
Lời giải:
a) Gọi công thức phân tử của acetic acid là CxHyOz.
Vì phân tử khối của acetic acid được xác định trên phổ khối lượng tương ứng với peak có giá trị m/z lớn nhất.
nên
Vậy công thức phân tử của acetic acid là C2H4O2.
b) Trên phổ IR của acetic acid, peak C (khoảng 1700 cm-1) giúp dự đoán được trong hợp chất này có nhóm chức C=O và peak A nằm trong khoảng 3300 – 3000 cm-1 giúp dự đoán được trong hợp chất này có nhóm chức O-H. Dựa vào hai giá trị trên, ta có thể dự đoán hợp chất này có nhóm chức carboxyl trong phân tử.
Xem thêm các bài giải SBT Hóa học lớp 11 Chân trời sáng tạo hay, chi tiết khác: