Tailieumoi.vn xin giới thiệu Bài tập Hoá học 8 :Bài tập tính theo phương trình hóa học. Bài viết gồm 50 bài tập với đầy đủ các mức độ và có hướng dẫn giải chi tiết sẽ giúp học sinh ôn luyện kiến thức và rèn luyện kĩ năng làm bài tập Hoá học 8. Ngoài ra, bài viết còn có phần tóm tắt nội dung chính lý thuyết Bài tập tính theo phương trình hóa học. Mời các bạn đón xem:
Bài tập Hoá học 8: Bài tập tính theo phương trình hóa học
A. Bài tập tính theo phương trình hóa học
I. Ví dụ minh họa
Ví dụ 1: Cho khối lượng của Fe là 5,6 g phản ứng với dung dịch HCl. Tính khối lượng của FeCl2. Biết phương trình phản ứng là: Fe + 2HCl → FeCl2 + H2
Hướng dẫn giải
Ta có nFe = 5,6 : 56 = 0,1 mol
Phương trình phản ứng: Fe + 2HCl → FeCl2 + H2
Tỉ lệ theo phương trình: 1 mol 2mol 1 mol 1 mol
Theo bài ra : 0,1 mol ? mol ? mol ? mol
Theo phương trình phản ứng ta có = nFe = 0,1 mol
Suy ra khối lượng của FeCl2 là: = 0,1.127 = 12,7 g.
Ví dụ 2: Tính thể tích khí CO2 sinh ra (đktc) khi nhiệt phân 50g CaCO3. Biết phương trình phản ứng: CaCO3 CaO + CO2
Hướng dẫn giải
Ta có = 0,5 mol
Theo phương trình phản ứng ta có = 0,5 mol
Suy ra = .22,4 = 0,5.22,4 = 11,2 lít
Ví dụ 3: Cho khối lượng của Mg là 7,2 g. Tính khối lượng của MgO, biết phương trình phản ứng là: 2Mg + O2 2MgO
Hướng dẫn giải
Ta có số mol của Mg tham gia phản ứng là nMg = 7,2 : 24 = 0,3 mol.
Phương trình hóa học: 2Mg + O2 2MgO
Theo phương trình hóa học: nMg = nMgO = 0,3 mol
Vậy khối lượng của MgO là mMgO = nMgO.MMgO = 0,3.40 = 12 g.
Ví dụ 4: Đốt cháy hoàn toàn 13 gam Zn trong khí oxi thu được ZnO.
a) Lập phương trình hóa học của phản ứng.
b) Tính khối lượng ZnO thu được?
Hướng dẫn giải
a) Phương trình hóa học: 2Zn + O2 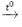
b) Số mol Zn tham gia phản ứng là: nZn = 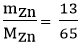
Phương trình hóa học: 2Zn + O2 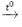
Theo phương trình hóa học ta có:
2 mol Zn tham gia phản ứng thu được 2 mol ZnO
Vậy 0,2 mol Zn tham gia phản ứng thu được 0,2 mol ZnO
Khối lượng ZnO thu được là: mZnO = nZnO. MZnO = 0,2.(65+16) = 16,2 gam.
Ví dụ 5: Cacbon cháy trong khí oxi sinh ra khí cacbon đioxit (CO2). Tính thể tích khí CO2 (đktc) sinh ra, nếu có 8 gam khí O2 tham gia phản ứng.
Hướng dẫn giải
Số mol O2 tham gia phản ứng là: nO2 = 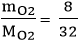
Phương trình hóa học: C + O2 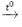
Theo phương trính hóa học ta có:
1 mol O2 tham gia phản ứng thu được 1 mol CO2
Vậy 0,25 mol O2 tham gia phản ứng thu được 0,25 mol CO2
Thể tích khí CO2 (đktc) sinh ra sau phản ứng là:
VCO2 = 22,4. nCO2 = 22,4.0,25 = 5,6 lít
Ví dụ 6: Đốt cháy hoàn toàn 27 gam Al trong khí oxi thu được Al2O3. Tính thể tích khí oxi (đktc) đã dùng trong phản ứng.
Hướng dẫn giải
Số mol Al tham gia phản ứng là: nAl = 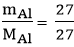
Phương trình hóa học: 4Al + 3O2 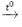
Theo phương trình hóa học: Đốt cháy 4 mol Al cần 3 mol O2
Vậy đốt cháy 1 mol Al cần 0,75 mol O2
Thể tích khí oxi (đktc) đã dùng trong phản ứng:
VO2 = 22,4.nO2 = 22,4.0,75 = 16,8 lít
II. Bài tập tự luyện
Câu 1: Cho phương trình phản ứng: 4P + 5O2 2P2O5. Biết khối lượng của P là 1,55 g. Số mol của P2O5 là
A. 0,025 mol
B. 0,05 mol
C. 0,1 mol
D. 0,25 mol
Đáp án: Chọn A
Ta có nP = 1,55 : 31 = 0,05 mol
Theo phương trình phản ứng ta có = 0,025 mol.
Câu 2: Cho 1,56 g Na2S tác dụng với dung dịch H2SO4 thu được m (g) H2S. Tính m, biết phương trình phản ứng là Na2S + H2SO4 → Na2SO4 + H2S
A. 1,02 g
B. 0,89 g
C. 0,68 g
D. 1,36 g
Đáp án: Chọn C
Ta có = 0,02 mol
Suy ra = 0,02.34 = 0,68 g
Câu 3: Cho phương trình phản ứng 2NO + O2 → 2NO2. Tính thể tích của NO biết khối lượng của NO2 là 0,46 g.
A. 0,224 lít
B. 0,336 lít
C. 0,448 lít
D. 0,560 lít
Đáp án: Chọn A
Ta có = 0,01 mol
2NO + O2 → 2NO2
0,01 mol 0,01 mol
VNO = nNO.22,4 = 0,01.22,4 = 0,224 lít
Câu 4: Cho 2,4 g Mg tác dụng với 8,96 lít khí clo (đktc). Hỏi sau phản ứng chất nào còn dư?
A. Clo
B. Mg
C. Không có chất dư
D. Cả 2 chất
Đáp án: Chọn A
Ta có nMg = 0,1 mol, = 0,4 mol
Phương trình phản ứng: Mg + Cl2 → MgCl2
Ban đầu 0,1 0,4 (mol)
Phản ứng 0,1 → 0,1 → 0,1 (mol)
Sau phản ứng 0 0,3 0,1 (mol)
Vậy sau phản ứng Clo còn dư.
Câu 5: Đốt cháy 8 g lưu huỳnh thu được m gam SO2. Tính m và thể tích (V) của khí oxi (đktc) tham gia phản ứng.
A. m = 12 g, V = 5,6 lít
B. m = 16 g, V = 2,24 lít
C. m = 16 g, V = 5,6 lít
D. m = 14g, V = 3,6 lít
Đáp án: Chọn C
Ta có nS = 8 : 32 = 0,25 mol
S + O2 SO2
0,25 0,25 0,25 (mol)
Vậy khối lượng của SO2 là m = 0,25.64 = 16 g
Thể tích của khí oxi (đktc) là V = 0,25.22,4 = 5,6 lít
Câu 6: Cho phương trình phản ứng AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
Biết khối lượng của NaOH là 1,2 g. Tìm số mol của NaCl sinh ra và AlCl3 phản ứng.
A. 0,03 mol, 0,02 mol
B. 0,03 mol, 0,01 mol
C. 0,02 mol, 0,04 mol
D. 0,03 mol, 0,04 mol
Đáp án: Chọn B
Ta có nNaOH = 1,2 : 40 = 0,03 mol
Vậy số mol của NaCl là 0,03 mol, số mol của AlCl3 là 0,01 mol
Câu 7: Phân hủy hoàn toàn 3,16 g KMnO4 (ở nhiệt độ cao) thu được V lít khí O2 ở đktc. Tính V
A. 0,336 lít
B. 0,448 lít
C. 0,112 lít
D. 0,224 lít
Đáp án: Chọn D
Ta có = 3,16 : 158 = 0,02 mol
Vậy thể tích của khí O2 là V = 0,01.22,4 = 0,224 lít
Câu 8: Cho a gam Mg tác dụng với dung dịch HCl thu được MgCl2 và 4 gam khí H2. Tìm a, biết phương trình phản ứng là: Mg + 2HCl → MgCl2 + H2
A. 4,8 gam
B. 48 gam
C. 24 gam
D. 0,24 gam
Đáp án: Chọn B
Có số mol của H2 là n = 4 : 2 = 2 mol
Vậy khối lượng của Mg là a = 2.24 = 48 gam.
Câu 9: Đốt cháy 3,36 (l) khí C2H2 trong không khí thu được khi và nước. Xác định khí và cho biết số mol của khí đó và số mol của nước.
A. CO2, 0,3 mol, 0,3 mol
B. C, 0,3 mol, 0,15 mol
C. CO, 0,3 mol, 0,3 mol
D. CO2, 0,3 mol, 0,15 mol
Đáp án: Chọn D
Số mol của C2H2 là 0,15 mol
Vậy khí cần tìm là CO2 với số mol là 0,3 mol, số mol của nước là 0,15 mol.
Câu 10: Cho 3,5 g N2 tác dụng với 0,56 lít khí O2 ở đktc. Giả sử hiệu suất phản ứng đạt 100%, sau phản ứng chất nào phản ứng hết?
A. O2
B. N2
C. Cả 2 chất
D. Không có chất phản ứng hết
Đáp án: Chọn A
Số mol của N2 là 0,125 mol, số mol của O2 là 0,025 mol
Phương trình phản ứng: N2 + O2 → 2NO
Ban đầu 0,125 0,025 (mol)
Phản ứng 0,025 0,025 0,05 (mol)
Sau phản ứng 0,1 0 0,05 (mol)
Vậy sau phản ứng O2 phản ứng hết.
B. Lý thuyết Bài tập tính theo phương trình hóa học
- Tìm khối lượng chất tham gia và chất sản phẩm
Các bước thực hiện:
+ Bước 1: Viết phương trình phản ứng.
+ Bước 2: Tính số mol của các chất.
+ Bước 3: Dựa vào phương trình phản ứng để tính được số mol chất cần tìm.
+ Bước 4: Tính khối lượng của chất cần tìm.
- Tìm thể tích chất khí tham gia và sản phẩm
Các bước thực hiện:
+ Bước 1: Viết phương trình phản ứng.
+ Bước 2: Tìm số mol chất khí.
+ Bước 3: Dựa vào phương trình hóa học tìm ra số mol chất cần tìm.
+ Bước 4: Tính thể tích khí.