Tailieumoi.vn xin giới thiệu Bài tập Hoá học 8 :Bài tập Xác định công thức hóa học của hợp chất khi biết thành phần các nguyên tố. Bài viết gồm 50 bài tập với đầy đủ các mức độ và có hướng dẫn giải chi tiết sẽ giúp học sinh ôn luyện kiến thức và rèn luyện kĩ năng làm bài tập Hoá học 8. Ngoài ra, bài viết còn có phần tóm tắt nội dung chính lý thuyết Bài tập Xác định công thức hóa học của hợp chất khi biết thành phần các nguyên tố. Mời các bạn đón xem:
Bài tập Hoá học 8: Xác định công thức hóa học của hợp chất khi biết thành phần các nguyên tố
A. Bài tập Xác định công thức hóa học của hợp chất khi biết thành phần các nguyên tố
I. Ví dụ minh họa
Ví dụ 1: Một hợp chất có thành phần các nguyên tố là 60% Mg và 40% O. Xác định công thức hóa học của hợp chất (biết khối lượng mol của hợp chất là 40 g/mol).
Hướng dẫn giải
+ Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
Ta có mMg = = 24 g, mO = = 16 g.
+ Số mol nguyên tử mỗi nguyên tố trong 1 mol hợp chất là
Ta có nMg = = 1 (mol), nO = = 1 (mol)
Suy ra trong 1 phân tử hợp chất có 1 nguyên tử Mg, 1 nguyên tử O
Vậy công thức hóa học của hợp chất là MgO.
Ví dụ 2: Cho hợp chất gồm sắt và oxi, biết %Fe = 72,41%. Tìm công thức hóa học của hợp chất.
Hướng dẫn giải
Gọi công thức của hợp chất là FexOy (x, y nguyên dương)
%O = 100% - %Fe = 100% - 72,41% = 27,59%
Ta có x : y = = 3 : 4 suy ra x = 3, y = 4
Vậy công thức hóa học của hợp chất là: Fe3O4
Ví dụ 3: Hợp chất X có khối lượng mol là 85 g/mol và chứa Na, N và O. Biết thành phần phần trăm về khối lượng các nguyên tố là %Na = 27,06%, %N = 16,47%, %O = 56,47%. Hãy xác định công thức hóa học của hợp chất X.
Hướng dẫn giải
+ Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất X là
Ta có mNa = = 23 g, mN = = 14 g, mO = = 48 g
+ Số mol nguyên tử của mỗi nguyên tố trong một mol hợp chất X là
Ta có nNa = 23 : 23 = 1 mol, nN = 14 : 14 = 1 mol, nO = 48 : 16 = 3 mol
Vậy trong 1 phân tử hợp chất X có 1 nguyên tử Na, 1 nguyên tử N, 3 nguyên tử O.
Vậy công thức hóa học của hợp chất X là NaNO3.
II. Bài tập tự luyện
Câu 1: Một hợp chất có thành phần các nguyên tố là 27,27% C, 72,73% O. Hãy xác định công thức hóa học của hợp chất (biết khối lượng mol của hợp chất là 44 g/mol).
A. CO
B. CO2
C. CO3
D. CO4
Đáp án: Chọn B
+ Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất là
Ta có mC = = 12 g, mO = = 32 g
+ Số mol nguyên tử của mỗi nguyên tố trong hợp chất là
nC = 12 : 12 = 1 mol, nO = 32 : 16 = 2 mol
Suy ra trong một phân tử hợp chất có 1 nguyên tử C và 2 nguyên tử O
Vậy công thức hóa học của hợp chất là CO2
Câu 2: Cho hợp chất có các nguyên tố K, O, H biết thành phần phần trăm về khối lượng các nguyên tố lần lượt là %K = 69,64%, %O = 28,57%, %H = 1,79% và khối lượng mol của hợp chất là 56 g/mol. Công thức của hợp chất là
A. KOH
B. K2(OH)
C. K(OH)2
D. K2O
Đáp án: Chọn A
Khối lượng của mõi nguyên tố có trong 1 mol hợp chất là
Ta có mK = 39 g, mO = 16g, mO = 1 g
Số mol nguyên tử mỗi nguyên tố trong 1 mol hợp chất là:
Có nK = 39 : 39 = 1 mol, nO = 16 : 16 = 1 mol, nH = 1 : 1 = 1mol
Vậy công thức hóa học của hợp chất là KOH.
Câu 3: Trong hợp chất C3H7OH hãy cho biết có bao nhiêu mol nguyên tử H có trong 1 mol hợp chất
A. 5
B. 6
C. 7
D. 8
Đáp án: Chọn D
Trong hợp chất C3H7OH có chứa 8 nguyên tử H nên trong 1 mol phân tử hợp chất có chứa 8 mol nguyên tử H.
Câu 4: Một hợp chất có thành phần các nguyên tố là 80,25% Zn và 19,75% O. Xác định công thức hóa học của hợp chất (biết khối lượng mol của hợp chất là 81 g/mol).
A. ZnO
B. Zn(OH)2
C. ZnO2
D. Zn2O
Đáp án: Chọn A
Gọi công thức của hợp chất là ZnxOy
Ta có x : y = = 1 : 1
Vậy công thức hóa học của hợp chất là ZnO.
Câu 5: Một chất gồm 2 nguyên tố kết hợp với nhau theo tỉ lệ khối lượng 3 phần Mg với 4 phần S. Công thức hóa học đơn giản của hợp chất là
A. Mg2S
B. Mg2S2
C. MgS
D. MgS2
Đáp án: Chọn C
Số mol Mg kết hợp với S là nMg = 3 : 24 = 0,125 mol
Số mol S kết hợp với Mg là nS = 4 : 32 = 0,125 mol
Vậy 0,125 mol nguyên tử Mg kết hợp với 0,125 nguyên tử S
Suy ra 1 mol nguyên tử Mg kết hợp với 1 mol nguyên tử S
Vậy công thức hóa học đơn giản của hợp chất là MgS
Câu 6: Chọn đáp án đúng
A. Có 5 bước để xác định công thức hóa học của hợp chất khi biết thành phần các nguyên tố.
B. Công thức tính khối lượng nguyên tố A trong hợp chất AxBy khi biết biết thành phần phần trăm về khối lượng: mA = (gam)
C. Công thức tính số mol của nguyên tử nguyên tố là n = m.M
D. Đơn vị của khối lượng mol là gam.
Đáp án: Chọn B
Câu 7: Cho hợp chất có khối lượng mol là 233 g/mol và chứa Ba, S và O. Biết thành phần phần trăm về khối lượng các nguyên tố là %Ba = 58,80%, %S = 13,73%, %O = 27,47%. Hãy xác định công thức hóa học của hợp chất.
A. BaSO2
B. BaSO3
C. Ba2SO3
D. BaSO4
Đáp án: Chọn D
Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là
Ta có mBa = 137 g, mS = 32 g, mO = 64 g
Số mol nguyên tử mỗi nguyên tố trong 1 mol hợp chất là
Có nBa = 137 : 137 = 1 mol, nS = 32 : 32 = 1 mol, nO = 64 : 16 = 4 mol
Vậy công thức hóa học của hợp chất là BaSO4
Câu 8: Cho hợp chất C4H9COOH. Tổng số mol của nguyên tử C và H có trong 1 mol hợp chất là
A. 12 mol
B. 13 mol
C. 14 mol
D. 15 mol
Đáp án: Chọn D
Trong hợp nhất có 5 nguyên tử C, 10 nguyên tử H nên trong 1 mol phân tử hợp chất có 5 mol nguyên tử C và 10 mol nguyên tử H
Vậy tổng số mol của nguyên tử C và H là 5 + 10 = 15 mol.
Câu 9: Một hợp chất A có công thức NOx biết khối lượng mol là 46 g/mol và thành phần phần trăm về khối lượng của N là %N = 30,43%. Công thức của hợp chất A là
A. NO
B. NO2
C. NO3
D. NO4
Đáp án: Chọn B
%O = 100% - %N = 100% - 30,43% = 69,57%
Có mO = = 32 g/mol
Số mol của nguyên tử O có trong 1 mol hợp chất là nO = 32 : 16 = 2 mol
Vậy công thức hóa học của hợp chất A là NO2
Câu 10: Tìm công thức hóa học của hợp chất Y biết khối lượng mol của Y là 122,5 g/mol và thành phần phần trăm về khối lượng các nguyên tố là %K = 31,84% và %Cl = 28,98%, còn lại là phần trăm khối lượng của O. Xác định công thức hóa học của hợp chất Y.
A. KClO3
B. KClO
C. KClO2
D. K2ClO
Đáp án: Chọn A
%O = 100% - (31,84% + 28,98%) = 39,18%
Khối lượng của mối nguyên tố trong 1 mol hợp chất là
Ta có mK = 39 gam, mCl = 35,5 gam, mO = 48 gam
Số mol nguyên tử mỗi nguyên tố có trong 1 mol hợp chất là
Có nK = 39 : 39 = 1 mol, nCl = 35,5 : 35,5 = 1 mol, nO = 48 : 16 = 3 mol.
Vậy công thức hóa học của hợp chất Y là KClO3.
Câu 11: Một hơp chất có thành phần các nguyên tố là 40% Cu; 20% S và 40% O. Hãy xác định công thức hoá học của hợp chất (biết khối lượng mol của hợp chất là 160 g/mol)
Đáp án:
- Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
mCu = 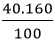
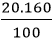
mO = 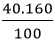
- Số mol nguyên tử của mỗi nguyên tố trong 1 mol hợp chất là:
nCu = 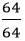
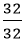
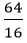
Suy ra trong 1 phân tử hợp chất có : 1 nguyên tử Cu, 1 nguyên tử S và 4 nguyên tử O.
Vậy công thức hoá học của hợp chất là: CuSO4
Câu 12: Một hợp chất khí A có thành phần về khối lượng của các nguyên tố là 40% S và 60% O. Hãy xác định công thức hóa học của hợp chất khí A biết A có tỉ khối so với khí H2 là 40?
Đáp án:
Gọi công thức hóa học cần tìm của A là SxOy
A có tỉ khối so với khí H2 là 40: MSxOy = 40. MH2 = 40. 2 = 80 g/mol
- Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
mS = 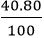
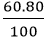
- Số mol nguyên tử của mỗi nguyên tố trong một mol hợp chất là:
nS = 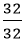
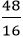
Suy ra trong 1 phân tử hợp chất có 1 nguyên tử S và 3 nguyên tử O.
Vậy công thức hoá học của hợp chất là: SO3
Câu 13: Hợp chất A chứa Ca, C và O. Biết thành phần phần trăm về khối lượng của các nguyên tố Ca, C, O lần lượt là: 40%, 12%, 48%. Lập công thức hóa học của A biết khối lượng mol của hợp chất là: 100 g/mol.
Đáp án:
- Khối lượng của mỗi nguyên tố trong 1 mol hợp chất là:
mCa = 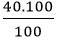
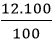
mO = 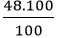
- Số mol nguyên tử của mỗi nguyên tố trong một mol hợp chất là:
nCa = 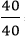
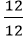
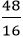
Vậy trong 1 phân tử hợp chất có 1 nguyên tử Ca, 1 nguyên tử C và 3 nguyên tử O.
Vậy công thức hoá học của hợp chất là: CaCO3
B. Lý thuyết Xác định công thức hóa học của hợp chất khi biết thành phần các nguyên tố
Gọi công thức tổng quát là AxBy
Để xác định công thức hóa học của hợp chất khi biết thành phần các nguyên tố ta cần thực hiện các bước sau:
+ Bước 1: Tìm khối lượng mỗi nguyên tố có trong 1 mol hợp chất
Ta có mA = (gam), mB = (gam)
+ Bước 2: Tìm số mol nguyên tử mỗi nguyên tố trong 1 mol hợp chất
Công thức: nA = (mol), nB = (mol)
+ Bước 3: Lập công thức hóa học của hợp chất.
Lưu ý: Nếu đề bài không cho dữ kiện tính khối lượng mol thì ta cần thực hiện theo cách sau: x : y =