Với tóm tắt lý thuyết Hóa học lớp 9 Clo hay, chi tiết cùng với 25 câu hỏi trắc nghiệm chọn lọc có đáp án giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt môn Hóa học lớp 9.
Hóa học 9 Bài 26: Clo
A. Lý thuyết Clo
I. Tính chất vật lí
- Clo là chất khí, màu vàng lục, mùi hắc, nặng gấp 2,5 lần không khí
( ) và tan được trong nước.
- Ở 20oC, một thể tích nước hòa tan được 20 thể tích khí clo.
- Tác dụng sinh lí: Clo là một khí độc.

Hình 1: Bình chứa khí clo
II. Tính chất hoá học
1. Clo có những tính chất hóa học của phi kim
a. Tác dụng kim loại → muối clorua
- Clo phản ứng với với hầu hết kim loại tạo thành muối clorua
- Ví dụ:
2Fe + 3Cl2 2FeCl3 (sắt(III) clorua)
2Na + Cl2 2NaCl (natri clorua)

Hình 2: Sắt tác dụng với clo
b. Tác dụng hiđro → khí hiđro clorua
- Phương trình hóa học:
H2 (k) + Cl2 (k) 2HCl (k) (khí hiđro clorua)
- Khí hiđro clorua tan nhiều trong nước tạo thành dung dịch axit clohiđric.
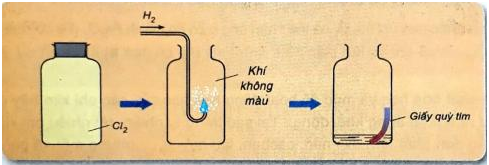
Hình 3: Khí hiđro tác dụng với khí clo.
Chú ý: Clo không phản ứng trực tiếp với oxi.
2. Tính chất hóa học khác của clo
a. Tác dụng với nước
- Phương trình hóa học:
Cl2 (k) + H2O (l) HCl (dd) + HClO (dd)
- Nước clo là dung dịch hỗn hợp các chất Cl2, HCl, HClO có màu vàng lục, mùi hắc.
- Khi cho quỳ tím vào nước clo, lúc đầu dung dịch làm quỳ tím hóa đỏ, sau đó nhanh chóng mất màu do tác dụng oxi hóa mạnh của axit hipoclorơ HClO.
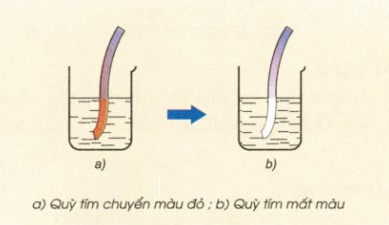
Hình 4: Nhúng giấy quỳ tím vào nước clo
- Nước clo có tính tẩy màu, sát trùng.
b. Tác dụng với dung dịch kiềm (NaOH, KOH, …)
- Khí clo có thể tác dụng với dung dịch kiềm.
Ví dụ:
Cl2 + 2NaOH → NaCl + NaClO + H2O
- Dung dịch hỗn hợp hai muối natri clorua (NaCl) và natri hipoclorit (NaClO) được gọi là nước Gia - ven. Dung dịch này có tính tẩy màu tương tự nước clo, vì NaClO cũng là chất oxi hóa mạnh tương tự HClO.
III. Ứng dụng của clo
- Nước clo dùng khử trùng nước sinh hoạt.
- Tẩy trắng vải sợi, bột giấy....
- Điều chế nước Gia - ven, clorua vôi...
- Điều chế nhựa PVC, chất dẻo, chất màu...
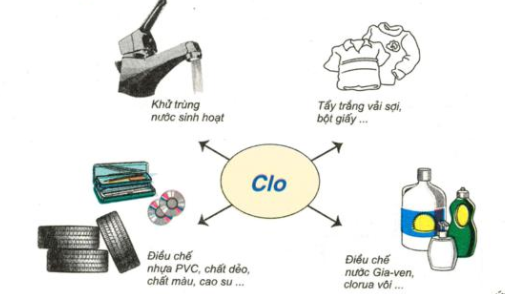
Hình 5: Sơ đồ về một số ứng dụng của khí clo
IV. Điều chế khí Clo
1. Trong phòng thí nghiệm
- Phương pháp Đun nóng nhẹ dung dịch HCl đậm đặc với các chất oxi hóa mạnh như MnO2, KMnO4,...
- Ví dụ:
MnO2 + 4HCl MnCl2 + Cl2 + 2H2O
- Thu khí clo bằng cách đẩy không khí.
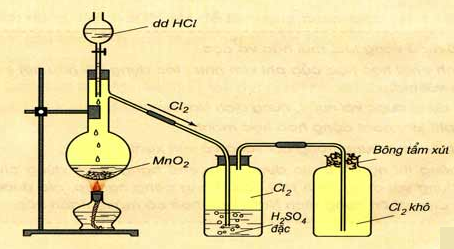
Hình 6: Điều chế clo trong phòng thí nghiệm
2. Trong công nghiệp
Phương pháp Điện phân dung dịch NaCl bão hòa (có màng ngăn xốp ngăn không cho khí Cl2 thoát ra tác dụng với NaOH tạo thành nước Gia-ven)
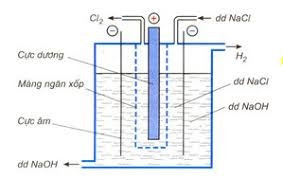
Hình 7: Sơ đồ thùng điện phân dung dịch NaCl
B. Trắc nghiệm Clo
Bài 1: Nước clo thường được dùng phổ biến để diệt trùng trong bể bơi. Vậy nước clo là:
A. HCl.
B. HClO.
C. HCl và HClO.
D. H2O.
Lời giải
Cl2 tan một phần trong nước tạo ra dd nước clo có tính sát khuẩn nên được dùng trong các bể bơi.
Cl2 + H2O ⇆ HCl + HClO (dd nước clo)
Đáp án: C
Bài 2: Clo tác dụng với hiđro tạo thành sản phẩm gì?
A. Hiđro clorua
B. Hiđro florua
C. Hiđro bromua
D. Hiđro iotua
Lời giải
Clo tác dụng với hiđro tạo thành hiđro clorua
H2 + Cl2 → 2HCl
Đáp án: A
Bài 3: Trong công nghiệp, clo được điều chế bằng phương pháp gì?
A. Điện phân dung dịch
B. Thủy phân
C. Nhiệt phân
D. Điện phân nóng chảy
Lời giải
Trong công nghiệp, clo được điều chế bằng phương pháp điện phân dung dịch
Đáp án: A
Bài 4: Clo tác dụng với sắt dư, sản phẩm thu được là:
A. FeCl3
B. FeCl2
C. Fe
D. Fe và FeCl3
Lời giải
Clo tác dụng với sắt xảy ra phản ứng:
3Cl2 + 2Fe → 2FeCl3
Tuy Fe dư nhưng đây không phải trong dung dịch, do đó Fe không tiếp tục phản ứng với FeCl3 để tạo ra FeCl2
Vậy sản phâm thu được gồm Fe và FeCl3
Đáp án: D
Bài 5: Cho dung dịch NaOH 1M để tác dụng vừa đủ với 1,12 lít khí clo (đktc). Nồng độ mol của muối natri clorua thu được là
A. 0,05M.
B. 0,5M.
C. 1,0M.
D. 1,5M.
Lời giải
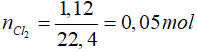
2NaOH + Cl2 → NaCl + NaClO + H2O
0,1 ← 0,05 → 0,05 mol
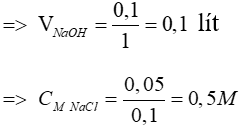
Đáp án: B
Bài 6: Hòa tan hoàn toàn 52,2 gam MnO2 trong dung dịch HCl đặc, nóng, dư thì sau phản ứng thu được bao nhiêu lít khí Cl2 (đktc)?
A. 6,72 lít.
B. 13,44 lít.
C. 14,56 lít.
D. 19,2 lít.
Lời giải
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
⇒ nCl2 = nMnO2 = 0,6 mol
=> V = 13,44 lít
Đáp án: B
Bài 7: Nguyên liệu được dùng để điều chế khí clo trong phòng thí nghiệm là:
A. H2SO4
B. HCl đặc
C. HNO3
D. H2SO3
Lời giải
Nguyên liệu được dùng để điều chế khí clo trong phòng thí nghiệm là HCl đặc
MnO2(r) + 4HClđặc → MnCl2 + Cl2(k) + 2H2O
Đáp án: B
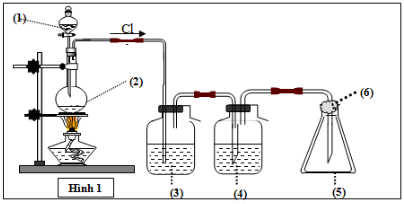
Bài 8: Mô hình điều chế khí clo trong phòng thí nghiệm được cho như hình vẽ bên (Hình 1). Quy trình thí nghiệm xảy ra như sau:
Nhỏ từ từ dung dịch (1) xuống bình cầu có chứa chất rắn màu đen (2). Đun nóng hỗn hợp thì thoát ra khí clo (màu vàng lục). Khí clo sinh ra di chuyển theo hệ thống bình (3); (4); (5). Tại bình số (5), khí clo được giữ lại. Để tránh việc clo thoát ra ngoài không khí, người ta tẩm vào (6) dung dịch T. Vậy (6) là:
A. HCl.
B. NaOH.
C. H2SO4.
D. NaCl.
Lời giải
Để tránh Cl2 thoát ra ngoài không khí, người ta tẩm NaOH vào (6). Vì Cl2 có phản ứng với NaOH do đó bị giữ lại
PTPƯ: Cl2 + 2NaOH → NaCl + NaClO + H2O
Đáp án: B
Bài 9: Dung dịch hỗn hợp hai muối natri clorua và natri hipoclorit được gọi là gì?
A. Nước gia-ven
B. Nước muối
C. Nước axeton
D. Nước cất
Lời giải
Dung dịch hỗn hợp hai muối natri cloruavà natri hipoclorit được gọi là nước gia-ven
Đáp án: A
Bài 10: Dung dịch nước clo có màu gì?
A. Xanh lục
B. Hồng
C. Tím
D. Vàng lục
Lời giải
Nước clo là dung dịch hỗn hợp các chất HCl, HClO và Cl2 nên có màu vàng lục, mùi hắc của khí clo.
Đáp án: D
Bài 11: Có 3 khí đựng riêng biệt trong 3 lọ là oxi, clo, hiđroclorua. Để phân biệt các khí đó có thể dùng một hóa chất là
A. quì tím ẩm
B. dd NaOH
C. dd AgNO3
D. dd brom
Lời giải
Để phân biệt 3 khí O2, Cl2 và HCl ta dùng giấy quỳ tím ẩm.
- O2 không làm đổi màu quỳ
- Cl2 làm mất màu quỳ tím ẩm (do có tính tẩy màu)
- HCl làm quỳ tím ẩm hóa đỏ (vì HCl tan vào nước tạo thành axit HCl)
Đáp án: A
Bài 12: Có 4 lọ đựng 4 khí riêng biệt: oxi, hiđro, clo và khí cacbonic. Bằng cách nào trong các cách sau đây để phân biệt mỗi khí trên (tiến hành theo trình tự sau):
A. Dùng nước vôi trong dư.
B. Dùng nước vôi trong dư, sau đó dùng quỳ tím ẩm.
C. Dùng tàn đom đóm, sau đó dùng quỳ tím ẩm.
D. Dùng quỳ tím ẩm, sau đó dùng nước vôi trong.
Lời giải
Ban đầu dùng tàn đóm đỏ => khí làm tàn đóm bùng cháy là O2
H2, Cl2, CO2 đều làm tàn đóm tắt
Sau đó dùng quỳ tím ẩm, khí làm mất màu quỳ ẩm là Cl2, khí làm quỳ ẩm hóa đỏ là CO2, khí không hiện tượng là H2
Đáp án: C
Câu 13: Nước clo có tính tẩy màu và sát trùng vì có đặc điểm nào sau đây?
A. Tạo ra ion Cl+ có tính oxi hóa mạnh
B. Tạo ra axit HClO có tính oxi hóa mạnh
C. Clo tác dụng với nước tạo ra HCl có tính tẩy màu
D. Clo có tính oxi hóa mạnh
Đáp án: B
Câu 14: Phương pháp để thu khí clo trong phòng thí nghiệm là:
A. Phương pháp đẩy không khí
B. Thu qua dung dịch NaCl bão hòa
C. Thu qua nước nóng
D. Cả ba phương pháp trên
Câu 15: Phát biểu nào sau đây là không đúng khi nói về số oxi hóa của clo?
A. Clo có số oxi hóa đặc trưng là -1
B. Clo chỉ có một số oxi hóa là -1
C. Clo có thể có các oxi hóa sau: -1; +1; +3; +5; +7
D. Do clo có phân lớp 3d còn trống nên clo có nhiều số oxi hóa
Đáp án: B
Câu 16: Đốt cháy 11,9 gam hỗn hợp gồm Zn, Al trong khí Cl2 dư. Sauk hi các phản ứng xảy ra hoàn toàn, thu được 40,3 gam hỗn hợp muối. Thể tích khí Cl2 (đktc) đã phản ứng là
A. 17,92 lít.
B. 6,72 lít.
C. 8,96 lít.
D. 11,20 lít.
Đáp án: C
Câu 17: Nguyên tố nào sau đây không phản ứng trực tiếp với clo?
A. Cacbon
B. Magie
C. Kẽm
D. Lưu huỳnh
Đáp án: A
Câu 18: Nguyên tố Cl ở ô thứ 17 trong bảng tuần hoàn, cấu hình electron của ion Cl- là :
A. 1s22s22p63s23p4.
B. 1s22s22p63s23p2.
C. 1s22s22p63s23p6.
D. 1s22s22p63s23p5.
Đáp án: C
Câu 19: Hiện tượng sẽ quan sát được khi cho nước clo thêm dần vào dung dịch KI có chứa sẵn hồ tinh bột?
A. Có hơi màu tím bay lên
B. Dung dịch chuyển sang màu vàng
C. Dung dịch có màu xanh đặc trưng
D. Không có hiện tượng gì
Đáp án: C
Câu 20: Khi hạ nhiệt độ xuống giá trị -100,98∘C thì khí clo sẽ hóa rắn. Ở trạng thái rắn, clo thuộc loại tinh thể nào?
A. Tinh thể ion
B. Tinh thể nguyên tử
C. Tinh thể phân tử
D. Không xác định được
Đáp án: C
Câu 21: Phản ứng nào sau đây thể hiện clo vừa có tính khử vừa có tính oxi hóa?
A. 3Cl2 + 2NH3 → 6HCl + N2
B. Cl2 + SO2 + 2H2O → 2HCl + H2SO4
C. Cl2 + 2NaOH → NaCl + NaClO + H2O
D. 3Cl2 + 2Fe → 2FeCl3
Đáp án: A
Câu 22: Cho 7,84 lít hỗn hợp khí X (đktc) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 75,68%.
B. 24,32%.
C. 51,35%.
D. 48,65%.
Đáp án: B
Câu 23: Sục Cl2 vào nước, thu được nước clo màu vàng nhạt. Trong nước clo có chứa các chất là :
A. Cl2, H2O.
B. HCl, HClO.
C. HCl, HClO, H2O.
D. Cl2, HCl, HClO, H2O.
Câu 24: Hoà tan khí Cl2 vào dung dịch KOH đặc, nóng, dư. Dung dịch thu được có các chất thuộc dãy nào dưới đây ?
A. KCl, KClO3, Cl2.
B. KCl, KClO3, KOH, H2O.
C. KCl, KClO, KOH, H2O.
D. KCl, KClO3.
Đáp án: B
Câu 25: Cho 10,8 gam kim loại M hóa trị III tác dụng với khí clo dư thì thu được 53,4 gam muối. Kim loại M là:
A. Al
B. Cr
D.Ni
Đáp án: C