Với giải Câu hỏi 7 trang 37 Khoa học tự nhiên lớp 7 Cánh diều chi tiết trong Bài 5: Giới thiệu về liên kết hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Khoa học tự nhiên 7. Mời các bạn đón xem:
Giải bài tập Khoa học tự nhiên lớp 7 Bài 5: Giới thiệu về liên kết hóa học
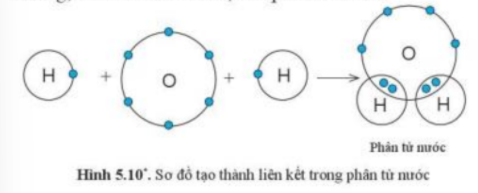
Câu hỏi 7 trang 37 KHTN lớp 7: Quan sát hình 5.10, cho biết trong phân tử nước, mỗi nguyên tử H và O có bao nhiêu electron ở lớp ngoài cùng
Phương pháp giải:
Đếm số quả cầu ở lớp ngoài cùng của nguyên tử H và O trong phân tử nước
Trả lời:
- Trong phân tử nước:
+ Nguyên tử H có 2 quả cầu màu xanh => Có 2 electron ở lớp ngoài cùng
+ Nguyên tử O có 8 quả cầu màu xanh => Có 8 electron ở lớp ngoài cùng
Lý thuyết Liên kết cộng hóa trị
1. Sự tạo thành liên kết cộng hóa trị
- Liên kết cộng hóa trị là liên kết được tạo thành bởi một hoặc nhiều đôi electron dùng chung giữa hai nguyên tử.
- Chất được tạo thành nhờ liên kết cộng hóa trị giữa các nguyên tử được gọi là chất cộng hóa trị.
- Để có lớp vỏ electron bền vững tương tự khí hiếm, các nguyên tử phi kim sẽ góp các electron để tạo ra một hoặc nhiều đôi electron dùng chung giữa các nguyên tử và liên kết với nhau thành phân tử.
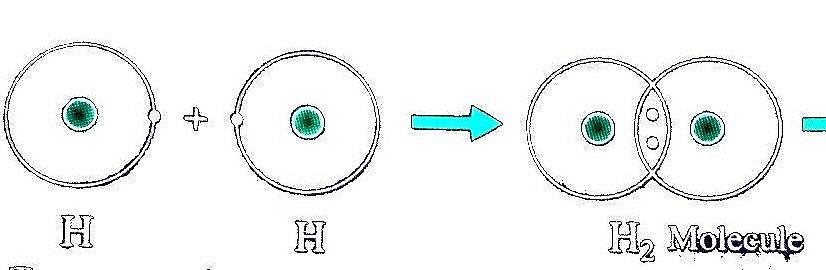
Ví dụ 1: Sự tạo thành liên kết trong phân tử hydrogen
+ Nguyên tử H chỉ có 1 electron và cần thêm 1 electron để có lớp vỏ bền vững tương tự khí hiếm.
+ Khi hai nguyên tử H liên kết với nhau, mỗi nguyên tử góp 1 electron để tạo ra đôi electron dùng chung.
+ Hạt nhân của hai nguyên tử H cùng hút đôi electron dùng chung và liên kết với nhau tạo thanh phân tử hydrogen. Liên kết như này được gọi là liên kết cộng hóa trị.
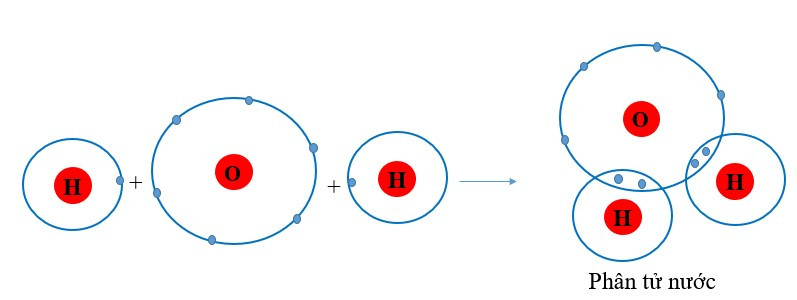
Ví dụ 2: Sự tạo thành liên kết trong phân tử nước
+ Khi O kết hợp với H, nguyên tử O góp 2 electron, mỗi nguyên tử H góp 1 electron. Giữa nguyên tử O và nguyên tử H có 1 electron dùng chung.
+ Hạt nhân nguyên tử O và H cùng hút đôi electron dùng chung, liên kết với nhau tạo ra phân tử nước.
2. Một số đặc điểm của chất cộng hóa trị
+ Có cả ba thể: thế rắn (đường ăn, iodine,…), thể lỏng (bromine, ethanol,…), thể khí (oxygen, nitrogen, khí carbonic,…).
+ Các chất cộng hóa trị thường có nhiệt độ sôi và nhiệt độ nóng chảy thấp.
+ Nhiều chất cộng hóa trị không dẫn điện (đường ăn, ethanol,…).
Xem thêm các bài giải Khoa học tự nhiên lớp 7 Cánh diều hay, chi tiết khác:
Mở đầu trang 33 KHTN lớp 7: Trong điều kiện thường, nguyên tử của các nguyên tố khí hiếm tồn tại độc lập vì có lớp electron ngoài cùng bền vững. Nguyên tử của các nguyên tố khác luôn có xu hướng tham gia liên kết để có được lớp electron ngoài cùng bền vững tương tự khí hiếm. Vậy liên kết giữa các nguyên tử được hình thành như thế nào?...
Câu hỏi 1 trang 33 KHTN lớp 7: Quan sát hình 5.1, hãy cho biết số electron ở lớp ngoài cùng của vỏ nguyên tử khí hiếm...
Tìm hiểu thêm trang 34 KHTN lớp 7: Helium được phát hiện vào năm 1868, khi các nhà khoa học nhận thấy một nguyên tố chưa được biết đến trong quang phổ ánh sáng từ Mặt Trời. Helium được đặt theo tên của thần Mặt Trời – Helios (theo tiếng Hy Lạp)....
Câu hỏi 2 trang 34 KHTN lớp 7: Quan sát hình 5.2 và hình 5.3, cho biết lớp vỏ của các ion Na+, Cl- tương tự vỏ nguyên tử của nguyên tố khí hiếm nào....
Câu hỏi 3 trang 34 KHTN lớp 7: Quan sát hình 5.2, hãy so sánh về số electron, số lớp electron giữa nguyên tử Na và ion Na+...
Luyện tập 1 trang 35 KHTN lớp 7: Số electron ở lớp ngoài cùng của nguyên tử K và F lần lượt là 1 và 7. Hãy cho biết khi K hết hợp với F để tạo thành phân tử potassium fluoride, nguyên tử K cho hay nhận bao nhiêu electron. Vẽ sơ đồ tạo thành liên kết trong phân tử potassium fluoride...
Câu hỏi 4 trang 35 KHTN lớp 7: Quan sát các hình 5.5 và 5.6, cho biết các ion Mg2+ và O2- có lớp vỏ tương tự khí hiếm nào...
Câu hỏi 5 trang 35 KHTN lớp 7: Quan sát hình 5.5, hãy so sánh về số electron, số lớp electron giữa nguyên tử Mg và ion Mg2+...
Luyện tập 2 trang 35 KHTN lớp 7: Nguyên tử Ca có 2 electron ở lớp ngoài cùng. Hãy vẽ sơ đồ tạo thành liên kết khi nguyên tử Ca kết hợp với nguyên tử O tạo ra phân tử calcium oxide...
Luyện tập 3 trang 36 KHTN lớp 7: Nguyên tử K kết hợp với nguyên tử Cl tạo thành phân tử potassium chloride. Theo em, ở điều kiện thường, potassium chloride là chất rắn, chất lỏng hay chất khí? Vì sao?...
Câu hỏi 6 trang 36 KHTN lớp 7: Quan sát hình 5.9, hãy cho biết nguyên tử H trong phân tử hydrogen có lớp vỏ tương tự khí hiếm nào...
Luyện tập 4 trang 36 KHTN lớp 7: Hai nguyên tử Cl liên kết với nhau tạo thành phân tử chlorine...
Luyện tập 5 trang 37 KHTN lớp 7: Mỗi nguyên tử H kết hợp với 1 nguyên tử Cl tạo thành phân tử hydrogen chloride. Hãy vẽ sơ đồ tạo thành phân tử hydrogen chloride từ nguyên tử H và nguyên tử Cl...
Luyện tập 6 trang 37 KHTN lớp 7: Mỗi nguyên tử N kết hợp với 3 nguyên tử H tạo thành phân tử ammonia. Hãy vẽ sơ đồ tạo thành liên kết trong phân tử ammonia....
Câu hỏi 8 trang 37 KHTN lớp 7: Quan sát hình 5.11, hãy cho biết trong phân tử khí carbonic, nguyên tử C có bao nhiêu electron dùng chung với nguyên tử O...
Luyện tập 7 trang 37 KHTN lớp 7: Hai nguyên tử N kết hợp với nhau tạo thành phân tử nitrogen. Hãy vẽ sơ đồ tạo thành liên kết trong phân tử nitrogen...
Vận dụng trang 38 KHTN lớp 7: Hãy giải thích các hiện tượng sau:...
Câu hỏi 9 trang 38 KHTN lớp 7: So sánh một số tính chất chung của chất cộng hóa trị với chất ion...
Xem thêm các bài giải SGK Khoa học tự nhiên lớp 7 Cánh diều hay, chi tiết khác:
Bài 4: Phân tử, đơn chất, hợp chất
Bài 5: Giới thiệu về liên kết hóa học
Bài 6: Hóa trị, công thức hóa học
Bài tập Chủ đề 3
Bài 7: Tốc độ của chuyển động


