Lời giải bài tập Khoa học tự nhiên lớp 7 Bài 4: Sơ lược về bảng tuần hoàn các nguyên tố hóa học sách Kết nối tri thức ngắn gọn, chi tiết sẽ giúp học sinh dễ dàng trả lời câu hỏi KHTN 7 Bài 4 từ đó học tốt môn Khoa học tự nhiên 7.
Giải bài tập KHTN lớp 7 Bài 4: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Video giải KHTN 7 Bài 4: Sơ lược về bảng tuần hoàn các nguyên tố hóa học - Kết nối tri thức
Trả lời:
- Nguyên tắc sắp xếp các nguyên tố để dễ dàng nhận ra tính chất của chúng
+ Các nguyên tố hóa học được xếp theo chiều tăng dần của điện tích hạt nhân
+ Các nguyên tố trong cùng một hàng có cùng số lớp electron trong nguyên tử
+ Các nguyên tố trong cùng cột có tính chất gần giống nhau
1. Nguyên tắc sắp xếp các nguyên tố hóa học trong bảng tuần hoàn
Hoạt động 1 trang 23 KHTN lớp 7: Sắp xếp các nguyên tố hóa học
Chuẩn bị:
- 18 thẻ ghi thông tin của 18 nguyên tố đầu tiện theo mẫu trong Hình 4.1.
Tiến hành: gắn các thẻ vào bảng mẫu ở trên từ trái qua phải, từ trên xuống dưới, mỗi thẻ vào 1 ô theo chiều tăng dần số đơn vị điện tích hạt nhân của các nguyên tố.
Thảo luận nhóm và nhận xét về các đặc điểm của bảng sau khi đã sắp xếp:
Sự thay đổi số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong một hàng khi đi từ trái sang phải
Phương pháp giải:
Số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong một hàng khi đi từ trái sang phải: tăng dần
Trả lời :
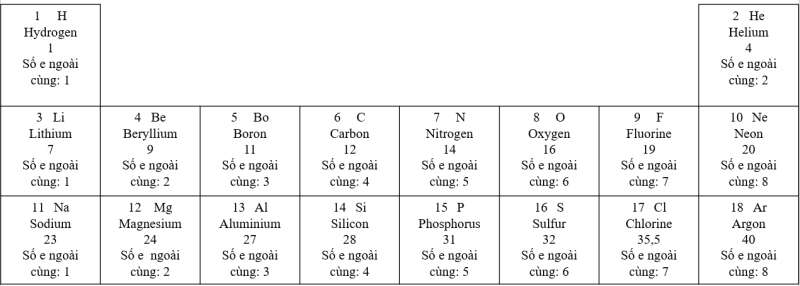
- Sự thay đổi số electron ở lớp ngoài cùng trong cùng 1 hàng khi đi từ trái sang phải:
+ Hàng thứ 1: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 2
+ Hàng thứ 2: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 8
+ Hàng thứ 3: Số electron ở lớp ngoài cùng tăng dần từ 1 đến 8
Hoạt động 2 trang 23 KHTN lớp 7: Sắp xếp các nguyên tố hóa học
Chuẩn bị:
- 18 thẻ ghi thông tin của 18 nguyên tố đầu tiện theo mẫu trong Hình 4.1.
Tiến hành: gắn các thẻ vào bảng mẫu ở trên từ trái qua phải, từ trên xuống dưới, mỗi thẻ vào 1 ô theo chiều tăng dần số đơn vị điện tích hạt nhân của các nguyên tố.
Thảo luận nhóm và nhận xét về các đặc điểm của bảng sau khi đã sắp xếp:
Số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong cùng một cột
Phương pháp giải:
Số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong cùng một cột: bằng nhau
Trả lời:
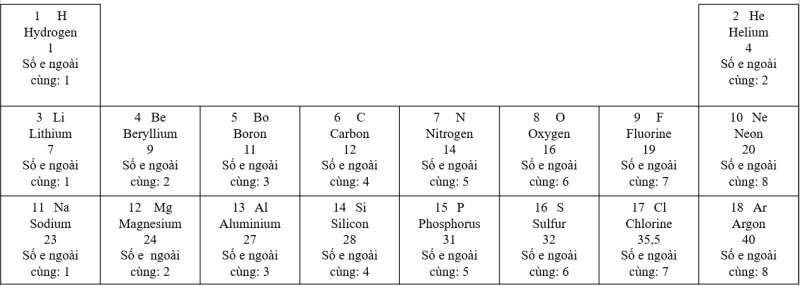
- Sự thay đổi số electron ở lớp ngoài cùng trong cùng 1 cột khi đi từ trên xuống dưới: Trong cùng 1 cột, các nguyên tử có số electron ở lớp ngoài cùng bằng nhau. Ví dụ
+ Cột 1: Số electron ở lớp ngoài cùng = 1
+ Cột 2: Số electron ở lớp ngoài cùng = 2
+ Cột 8: Trừ He, số electron ở lớp ngoài cùng = 8
Phương pháp giải:
Dựa vào số electron ở lớp ngoài cùng và số lớp electron của nguyên tố đó
Trả lời:
- Dựa vào số electron ở lớp ngoài cùng và số lớp electron của nguyên tố đó. Ví dụ
+ Trong cùng một hàng, tính từ trái sang phải: Các nguyên tử có cùng số lớp electron, số electron ở lớp ngoài cùng tăng dần
+ Trong cùng một cột, tính từ trên xuống dưới: Các nguyên tử có cùng số electron ở lớp ngoài cùng, số lớp electron tăng dần
Phương pháp giải:
Các nguyên tố trong cùng một hàng sẽ có cùng số lớp electron
Trả lời:
Trong 4 nguyên tố: Li, Na, C, O có 3 nguyên tố trong cùng 1 hàng đó là: Li, C, O đều nằm ở hàng thứ 2
=> 3 nguyên tố Li, C, O đều có 2 lớp electron
2. Cấu tạo bảng tuần hoàn các nguyên tố hóa học
Phương pháp giải:
Số hiệu nguyên tử = số đơn vị điện tích hạt nhân = số electron trong nguyên tử
Trả lời:
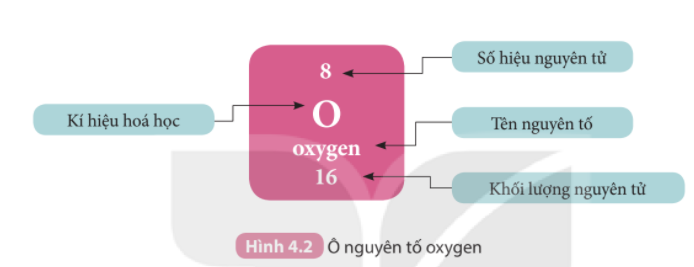
Ta có: số hiệu nguyên tử = số đơn vị điện tích hạt nhân (số proton) = số electron trong nguyên tử
- Oxygen có số hiệu nguyên tử là 8
=> Oxygen có 8 proton và 8 electron
Phương pháp giải:
Trả lời:
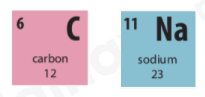
- Ô số 6:
+ Kí hiệu hóa học: C
+ Tên nguyên tố: Carbon
+ Số hiệu nguyên tử: 6
+ Khối lượng nguyên tử: 12
+ Số electron trong nguyên tử = số hiệu nguyên tử: 6
- Ô số 11:
+ Kí hiệu hóa học: Na
+ Tên nguyên tố: Sodium
+ Số hiệu nguyên tử: 11
+ Khối lượng nguyên tử: 23
+ Số electron trong nguyên tử = số hiệu nguyên tử: 12
Chuẩn bị: 6 mô hình sắp xếp electron ở vỏ nguyên tử của sáu nguyên tố H, He, Li, Be, C, N theo mẫu được mô tả trong Hình 4.4
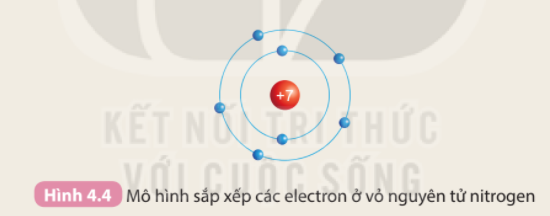
Quan sát các mô hình đã chuẩn bị, thảo luận và thực hiện các yêu cầu sau: Hãy cho biết số lớp electron của nguyên tử các nguyên tố trên.
Phương pháp giải:
Số lớp electron là số đường tròn xung quanh hạt nhân
Trả lời:
- Nguyên tố H (Z = 1), He (Z = 2), Li (Z = 3), Be ( Z = 4), C (Z = 6), N (Z = 7)
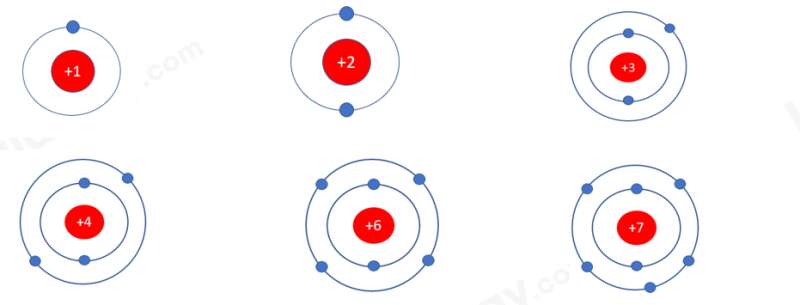
- Nguyên tố H, He có 1 đường tròn => 1 lớp electron
- Nguyên tố Li, Be, C, N có 2 đường tròn => 2 lớp electron
Chuẩn bị: 6 mô hình sắp xếp electron ở vỏ nguyên tử của sáu nguyên tố H, He, Li, Be, C, N theo mẫu được mô tả trong Hình 4.4

Quan sát các mô hình đã chuẩn bị, thảo luận và thực hiện các yêu cầu sau: So sánh số lớp electron của nguyên tử các nguyên tố trên với số thứ tự chu kì của các nguyên tố đó.
Phương pháp giải:
Số lớp electron = số thứ tự chu kì của nguyên tố
Trả lời:
- Nguyên tố H (Z = 1), He (Z = 2), Li (Z = 3), Be ( Z = 4), C (Z = 6), N (Z = 7)

- Nguyên tố H, He có 1 lớp electron, nằm ở chu kì 1
- Nguyên tố Li, Be, C, N có 2 lớp electron, nằm ở chu kì 2
=> Số lớp electron của nguyên tử các nguyên tố = số thứ tự chu kì của các nguyên tố đó
Phương pháp giải:
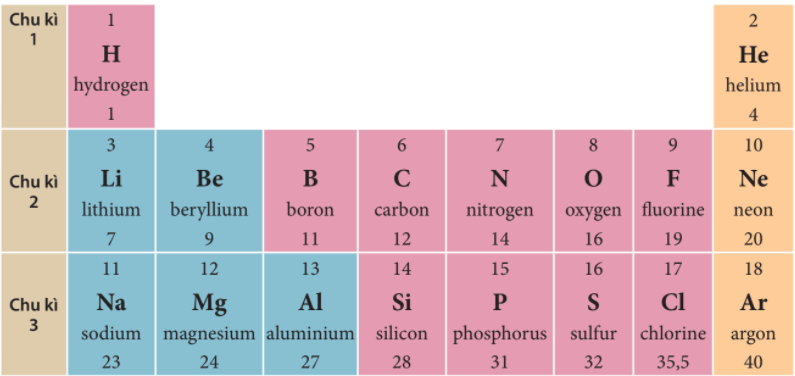
Nguyên tố xung quanh nguyên tố C: B, N, Si
Trả lời:
- Các nguyên tố xung quanh nguyên tố C là: B, N, Si
- Nguyên tố B:
+ Tên: Boron
+ Kí hiệu hóa học: B
+ Điện tích hạt nhân: 5
- Nguyên tố N:
+ Tên: Nitrogen
+ Kí hiệu hóa học: N
+ Điện tích hạt nhân: 7
- Nguyên tố Si:
+ Tên: silicon
+ Kí hiệu hóa học: Si
+ Điện tích hạt nhân: 14
Phương pháp giải:
Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron
Trả lời:
- Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron
=> Nguyên tử các nguyên tố thuộc chu kì 3 đều có 3 lớp electron
Chuẩn bị: 4 mô hình sắp xếp electron ở vỏ nguyên tử của Li, Na, F, Cl theo mẫu mô tả trong Hình 4.4.
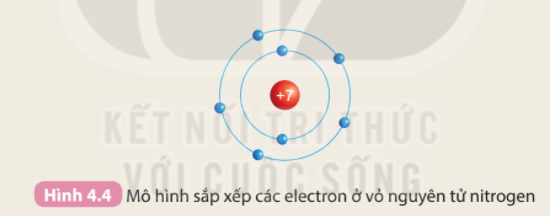
Quan sát các mô hình đã chuẩn bị, thảo luận và trả lời câu hỏi:
Hãy cho biết nguyên tử các nguyên tố nào có cùng số electron ở lớp ngoài cùng
Phương pháp giải:
Dựa vào mô hình đã chuẩn bị, đếm số electron ở lớp ngoài cùng
Trả lời:
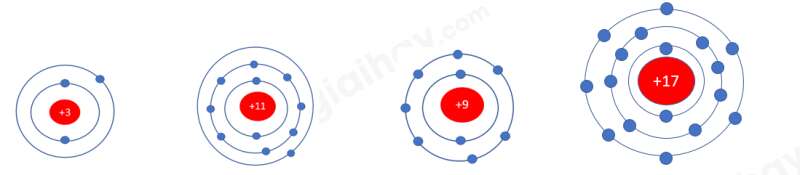
- Nguyên tử Li (Z = 3): Có 1 electron ở lớp ngoài cùng
- Nguyên tử Na (Z = 11): Có 1 electron ở lớp ngoài cùng
- Nguyên tử F (Z = 9): Có 7 electron ở lớp ngoài cùng
- Nguyên tử Cl (Z = 17): Có 7 electron ở lớp ngoài cùng
=> Nguyên tử Li, Na có cùng số electron ở lớp ngoài cùng, nguyên tử F, Cl có cùng số electron ở lớp ngoài cùng
Chuẩn bị: 4 mô hình sắp xếp electron ở vỏ nguyên tử của Li, Na, F, Cl theo mẫu mô tả trong Hình 4.4.

Quan sát các mô hình đã chuẩn bị, thảo luận và trả lời câu hỏi:
Hãy so sánh số electron lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự nhóm của các nguyên tố đó
Phương pháp giải:
Các nguyên tố trong cùng 1 nhóm A có số electron ở lớp ngoài cùng bằng nhau
Trả lời:
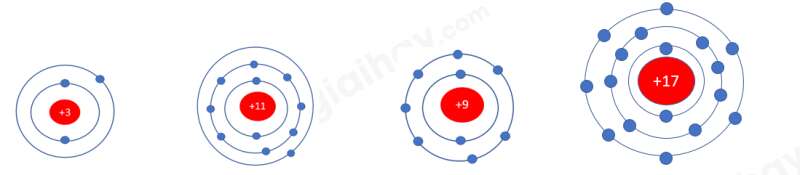
- Nguyên tử Li, Na có 1 electron ở lớp ngoài cùng => Nằm trong nhóm IA
- Nguyên tử F, Cl có 7 electron ở lớp ngoài cùng => Nằm ở nhóm VIIA
=> Số electron ở lớp ngoài cùng của nguyên tử các nguyên tố = số thứ tự nhóm
Phương pháp giải:
Các nguyên tố trong cùng 1 nhóm A có số electron ở lớp ngoài cùng bằng nhau = số thứ tự của nhóm
Trả lời:
- Al thuộc nhóm IIIA => Al có 3 electron ở lớp ngoài cùng
- S thuộc nhóm VIA => S có 6 electron ở lớp ngoài cùng
Phương pháp giải:
- Chu kì 1, 2, 3 được gọi là các chu kì nhỏ
- Beryllium thuộc nhóm IIA
Trả lời:
- Beryllium thuộc chu kì 2 nhóm IIA
=> Có nguyên tố Magnesium thuộc chu kì 3 nhóm IIA (cùng nhóm với nguyên tố beryllium)
3. Vị trí các nhóm nguyên tố kim loại, phi kim và khí hiếm trong bảng tuần hoàn
Phương pháp giải:
- Số thứ tự = số hiệu nguyên tử
- Số chu kì = số thứ tự hàng
- Số nhóm = số thứ tự cột A
Trả lời:
- Nguyên tố Al:
+ Số thứ tự: 13
+ Chu kì: 3
+ Nhóm: IIIA
- Nguyên tố Ca:
+ Số thứ tự: 20
+ Chu kì: 4
+ Nhóm: IIA
- Nguyên tố Na:
+ Số thứ tự: 11
+ Chu kì: 3
+ Nhóm: IA

Phương pháp giải:
Các tính chất của kim loại: tính dẻo, bền, dẫn điện, dẫn nhiệt, có tính ánh kim
Trả lời:
- Trong Hình 4.6:
+ Nhôm có tính dẻo, được dùng làm màng bọc thực phẩm
+ Sắt cứng, bền với môi trường, được dùng làm công trình xây dựng
+ Đồng có tính dẫn điện tốt, được dùng làm lõi dây điện

Phương pháp giải:
- Số thứ tự = số hiệu nguyên tử
- Số chu kì = số thứ tự hàng
- Số nhóm = số thứ tự cột A
Trả lời:
- Nguyên tố oxygen (O)
+ Số thứ tự: 8
+ Chu kì: 2
+ Nhóm: VIA
- Nguyên tố chlorine (Cl)
+ Số thứ tự: 17
+ Chu kì: 3
+ Nhóm: VIIA
- Nguyên tố sulfur (S)
+ Số thứ tự: 16
+ Chu kì: 3
+ Nhóm: VIIA
- Nguyên tố bromine (Br)
+ Số thứ tự: 35
+ Chu kì: 4
+ Nhóm: VIIA
Phương pháp giải:
- Số thứ tự = số hiệu nguyên tử
- Số chu kì = số thứ tự hàng
- Số nhóm = số thứ tự cột A
Trả lời:
Khí hiếm Neon
+ Số thứ tự: 10
+ Chu kì: 2
+ Nhóm: VIIIA
Câu hỏi 2 trang 31 KHTN lớp 7: Bảng tuần hoàn các nguyên tố hóa học gồm các nguyên tố:
A. Kim loại và phi kim
B. Phi kim và khí hiếm
C. Kim loại và khí hiếm
D. Kim loại, phi kim và khí hiếm
Hãy chọn đáp án đúng nhất.
Phương pháp giải:
Bảng tuần hoàn gồm các nguyên tố: kim loại, phi kim và khí hiếm
Trả lời:
Bảng tuần hoàn các nguyên tố hóa học gồm các nguyên tố: kim loại (màu xanh), phi kim (màu hồng) và khí hiếm (màu vàng). Xem ở Bảng tuần hoàn trang 25
=> Đáp án D
Câu hỏi 3 trang 31 KHTN lớp 7: Cho các nguyên tố sau:

a) Sử dụng bảng tuần hoàn, hãy cho biết trong các nguyên tố trên, nguyên tố nào là kim loại, nguyên tố nào là phi kim
b) Nêu ứng dụng trong đời sống của một nguyên tố trong số các nguyên tố trên.
Phương pháp giải:
- Nguyên tố kim loại ở góc dưới bên trái của bảng, được thể hiện bằng màu xanh
- Nguyên tố phi kim chủ yếu ở góc trên bên phải, được thể hiện bằng màu hồng
Trả lời:
a)
- Các nguyên tố kim loại là: Ba, Rb, Cu, Fe
- Các nguyên tố phi kim là: P, Si
b) Ứng dụng của nguyên tố Nhôm (Al) trong đời sống
- Được dùng để chế tạo máy bay, ô tô, tên lửa, tàu vũ trụ
- Dùng trong xây dựng nhà cửa và trang trí nội thất
- Dụng cụ nhà bếp vì dẫn nhiệt tốt, ít bị gỉ và không độc
- Bột nhôm trộn với bột sắt oxit để thực hiện phản ứng nhiệt nhôm dùng hàn đường ray
Lý thuyết KHTN 7 Bài 4: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
I. Nguyên tắc sắp xếp các nguyên tố hóa học trong bảng tuần hoàn
- Năm 1869, Men-đê-lê-ép (D.I.Mendeleev) (1834 -1907), nhà hóa học người Nga đã xây dựng bảng tuần hoàn các nguyên tố hóa học theo chiều tăng dần khối lượng nguyên tử. Sau đó, các nhà khoa học đã chứng minh rằng điện tích hạt nhân nguyên tử mới là cơ sở để xây dựng bảng tuần hoàn các nguyên tố hóa học.
- Ngày nay, bảng tuần hoàn các nguyên tố hóa học gồm 118 nguyên tố hóa học, được xây dựng theo nguyên tắc sau:
+ Các nguyên tố hóa học được sắp xếp theo chiều tăng dần của điện tích hạt nhân.
+ Các nguyên tố trong cũng một hàng có cùng số lớp electron trong nguyên tử.
+ Các nguyên tố trong cùng một cột có tính chất gần giống nhau.
II. Cấu tạo bảng tuần hoàn các nguyên tố hóa học
1. Ô nguyên tố
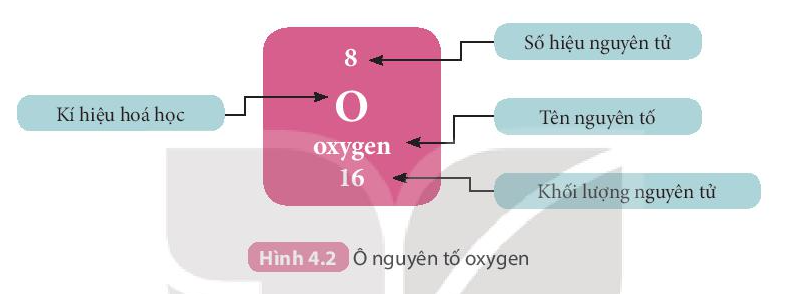
- Mỗi nguyên tố hóa học được xếp vào một ô của bảng tuần hoàn, gọi là ô nguyên tố.
- Ô nguyên tố cho biết:
+ Kí hiệu hóa học.
+ Tên nguyên tố
+ Số hiệu nguyên tử
+ Khối lượng nguyên tử.
- Số hiệu nguyên tử = Số đơn vị điện tích hạt nhân = Số electron trong nguyên tử.
- Số hiệu nguyên tử chính là số thứ tự của nguyên tố trong bảng tuần hoàn.
Ví dụ: Các thông tin về nguyên tố ở ô số 8 trong bảng tuần hoàn chi biết:
+ Kí hiệu hóa học: O
+ Tên nguyên tố: Oxygen
+ Số hiệu nguyên tử Z = 8
+ Khối lượng nguyên tử: 16 amu
Ngoài ra: Số hiệu nguyên tử = Số đơn vị điện tích hạt nhân = Số electron = số proton = 8
2. Chu kì
- Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron, được xếp theo chiều điện tích hạt nhân tăng dần khi đi từ trái sang phải.
- Bảng tuần hoàn hiện nay gồm 7 chu kì được đánh số từ 1 đến 7, mỗi chu kì là một hàng ngang (riêng chu kì 6 và chu kì 7, mỗi chu kì có thêm 1 hàng xếp tách riêng ở cuối bảng).
+ Chu kì 1, 2, 3 được gọi là các chu kì nhỏ;
+ Chu kì 4, 5, 6, 7 được gọi là các chu kì lớn.
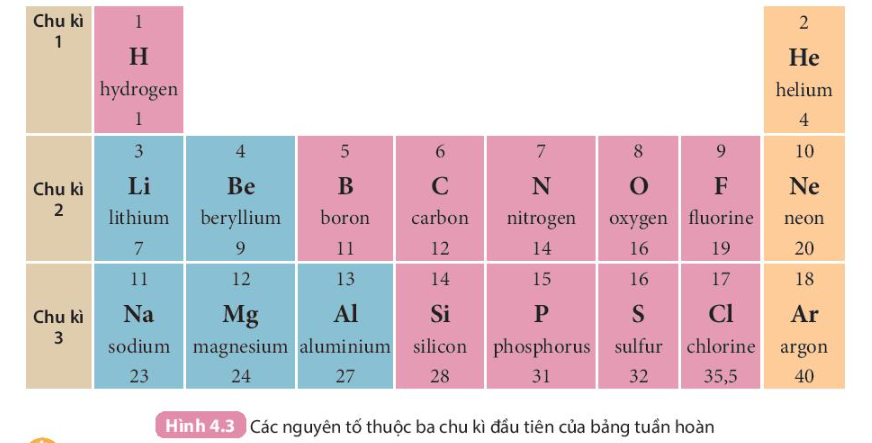
- Trong bảng tuần hoàn, số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố trong chu kì đó.
Ví dụ: Các nguyên tố lithium, carbon, oxygen thuộc chu kì 2 đều có 2 lớp electron trong nguyên tử.
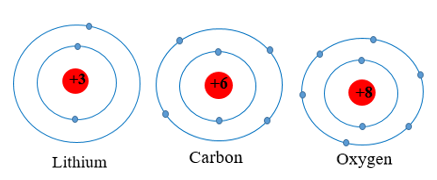
3. Nhóm
- Bảng tuần hoàn gồm có 8 nhóm A được đánh só từ IA đến VIIIA và 8 nhóm B được đánh số từ IB đến VIIIB.
- Các nguyên tố trong cùng một nhóm A có số electron ở lớp ngoài cùng bằng nhau (trừ trường hợp nguyên tố He), do vậy chúng có tính chất gần giống nhau.
Ví dụ: Nhóm IA gồm 7 nguyên tố từ H đến Fr. Các nguyên tố trong nhóm IA (trừ H) đều có 1 electron lớp ngoài cùng ⇒ Dễ nhường electron ⇒ Tính kim loại mạnh (nhóm các kim loại điển hình).
- Trong một nhóm, khi đi từ trên xuống dưới điện tích hạt nhân nguyên tử của các nguyên tố tăng dần.
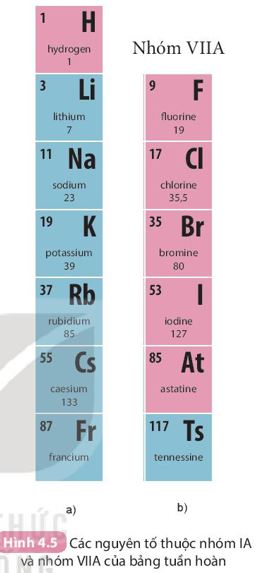
- Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong nhóm đó.
Ví dụ:
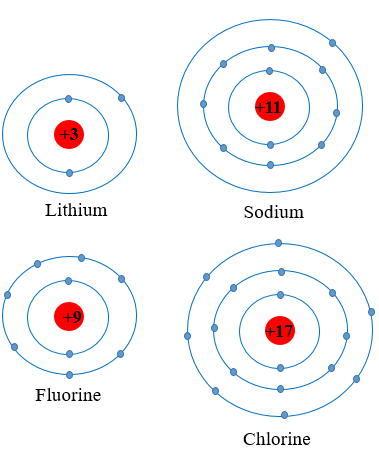
Nguyên tử các nguyên tố Li, Na cùng có 1 electron ở lớp ngoài cùng ⇒ thuộc nhóm IA trong bảng tuần hoàn.
Nguyên tử các nguyên tố F, Cl cùng có 7 electron ở lớp ngoài cùng ⇒ thuộc nhóm VIIA trong bảng tuần hoàn.
Mở rộng:
+ Một số nhóm có tên gọi riêng như: nhóm IA (nhóm kim loại kiềm); nhóm IIA (nhóm kim loại kiềm thổ); nhóm VIIA (nhóm halogen); nhóm VIIIA (nhóm khí hiếm).
+ Nguyên tố H có nhiều tính chất gần giống với nguyên tố nhóm VIIA; nên có thể được xếp ở vị trí đầu nhóm VIIA.
III. Vị trí nhóm các nguyên tố kim loại, phi kim và khí hiếm trong bảng tuần hoàn
1. Các nguyên tố kim loại
- Trong số 118 nguyên tố hóa học đã biết có hơn 90 nguyên tố kim loại.
- Trong bảng tuần hoàn các nguyên tố kim loại ở góc dưới, bên trái của bảng và được thể hiện bằng màu xanh, gồm:
+ Hầu hết các nguyên tố thuộc nhóm IA, IIA, IIIA và một số nguyên tố ở các nhóm IVA, VA, VIA.
+ Các nguyên tố thuộc nhóm IB đến VIIIB, các nguyên tố lathanide và các nguyên tố actinide được xếp riêng thành hai hàng ở cuối bảng.
- Một số nguyên tố kim loại thông dụng và ứng dụng của chúng trong đời sống:
+ Aluminium (Al) được dùng nằm màng bọc thực phẩm vì nhôm dễ dát mỏng, nhẹ, dẫn nhiệt tốt.
+ Copper(Cu) được dùng làm lõi dây điện vì đồng dễ uốn, dẫn điện tốt.
+ Iron (Fe) được dùng trong các công trình xây dựng vì sắt cứng, chịu lực tốt, bền.
+ Gold (Au) được ứng dụng là đồ trang sức vì có tính ánh kim, sáng lấp lánh và dễ dát mỏng.

2. Các nguyên tố phi kim
- Trong 118 nguyên tố hóa học đã biết, có chưa đến 20 nguyên tố là phi kim.
- Ở điều kiện thường các phi kim có thể ở thể rắn, thể lỏng hay thể khí.
Ví dụ:
+ Iodine, sulfur, carbon ở thể rắn
+ Bromine ở thể lỏng
+ Oxygen, nitrogen ở thể khí
- Trong bảng tuần hoàn, các phi kim chủ yếu ở góc bên phải của bảng, được thể hiện bằng màu hồng, gồm:
+ Hầu hết các nguyên tố thuộc nhóm VIIA, VIA, VA.
+ Một số nguyên tố thuộc nhóm IVA, IIIA.
+ Nguyên tố H ở nhóm IA.

- Các nguyên tố phi kim có nhiều ứng dụng như:
+ Oxygen là phi kim không thể thiếu với sự sống của hầu hết các sinh vật, được tạo ra trong quá trình quang hợp và được sử dụng trong quá trình hô hấp.
+ Chlorine có thể được dùng để khử trùng nước sinh hoạt.
3. Các nguyên tố khí hiếm
- Trong số 118 nguyên tố đã biết có 7 nguyên tố là nguyên tố khí hiếm.
- Nguyên tử của chúng có lớp electron ngoài cùng bền vững nên khó bị biến đổi hóa học.
- Trong bảng tuần hoàn, nguyên tố khí hiếm nằm ở nhóm VIIIA và được thể hiện bằng màu vàng.
- Một số ứng dụng trong đời sống của khí hiếm như: He được sử dụng trong khinh khí cầu; Ne được sử dụng trong đèn LED…
Mở rộng:
- Các nguyên tử kim loại có xu hướng nhường electron (để tạo ion dương), còn các phi kim có xu hướng nhận electron (để tạo ion âm) để đạt được lớp electron ngoài cùng bền vững giống khí hiếm là 8 electron hoặc 2 electron (với trường hợp He).
Xem thêm các bài giải SGK Khoa học tự nhiên lớp 7 Kết nối tri thức hay, chi tiết khác:
Bài 5: Phân tử - Đơn chất - Hợp chất
Bài 6: Giới thiệu về liên kết hóa học
Bài 7: Hóa trị và công thức hóa học