Với giải Câu 1 trang 66 Hóa học lớp 10 Kết nối tri thức với cuộc sống chi tiết trong Bài 13: Liên kết hydrogen và tương tác van der waals giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 10 Bài 13: Liên kết hydrogen và tương tác van der waals
Câu 1 trang 66 Hóa học 10: Vẽ sơ đồ biểu diễn liên kết hydrogen giữa:
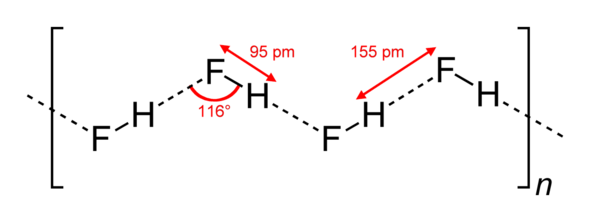
a) hai phân tử hydrogen fluoride (HF)
b) phân tử hydrogen fluoride (HF) và phân tử ammonia (NH3).
Phương pháp giải:
- Liên kết hydrogen được hình thành giữa nguyên tử hydrogen với các nguyên tử có độ âm điện lớn (F, N, O…) và các nguyên tử này phải có 1 ít nhất một cặp electron hóa trị chưa tham gia liên kết.
- Liên kết hydrogen được biểu diễn bằng dấu ba chấm (…)
Lời giải:
a)
b)
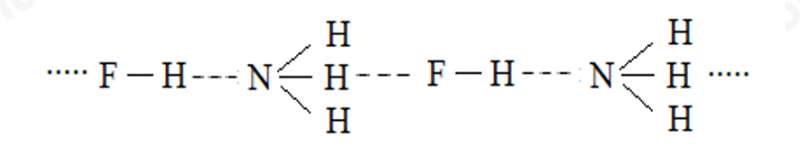
Lý thuyết Liên kết hydrogen
1. Bản chất của liên kết hydrogen
Liên kết hydrogen được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn) với một nguyên tử khác (có độ âm điện lớn) còn cặp electron hóa trị chưa tham gia liên kết.
Ví dụ:
 Một số kiểu tạo thành liên kết hydrogen:
Một số kiểu tạo thành liên kết hydrogen:
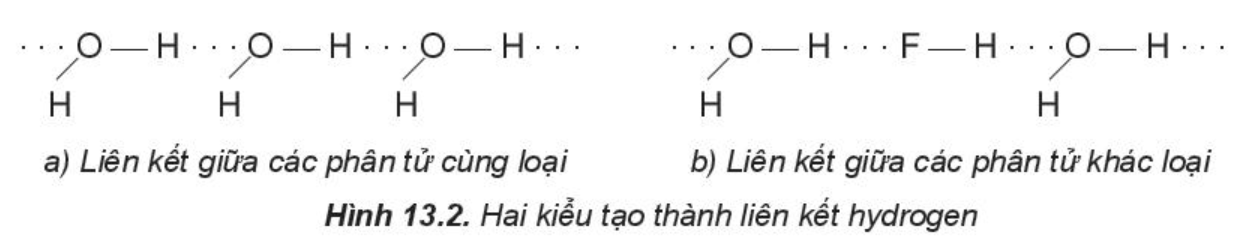
Chú ý:
- Điều kiện cần và đủ để tạo thành liên kết hydrogen:
+ Nguyên tử hydrogen liên kết với các nguyên tử có độ âm điện lớn như F, O, N …
+ Nguyên tử F, O, N, … liên kết với hydrogen phải có ít nhất một cặp electron hóa trị chưa liên kết.
2. Vai trò và ảnh hưởng của liên kết hydrogen tới tính chất vật lí của nước
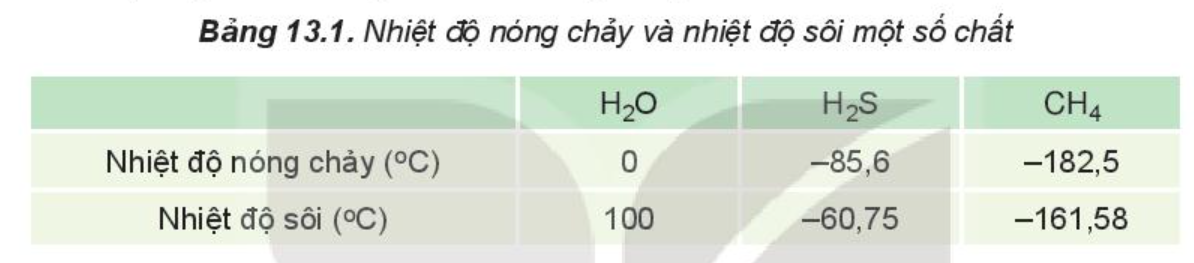
Liên kết hydrogen làm tăng nhiệt độ nóng chảy, nhiệt độ sôi của nước.
Ví dụ: Do ảnh hưởng của liên kết hydrogen nên nhiệt độ nóng chảy và nhiệt độ sôi của H2O cao hơn nhiều so với H2S và CH4.
Xem thêm các bài giải Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Câu 3 trang 67 Hóa học 10: Hãy giải thích sự khác nhau về nhiệt độ sôi của butane và isobutane...
Xem thêm các bài giải SGK Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 13: Liên kết hydrogen và tương tác van der waals
Bài 15: Phản ứng oxi hóa - khử