Với giải Câu hỏi 7 trang 88 Hóa học lớp 10 Kết nối tri thức với cuộc sống chi tiết trong Bài 17: Biến thiên enthalpy trong các phản ứng hóa học giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 10 Bài 17: Biến thiên enthalpy trong các phản ứng hóa học
Câu hỏi 7 trang 88 Hóa học 10: a) Cho biết năng lượng liên kết trong các phân tử O2, N2 và NO lần lượt là 494 kJ/mol, 945 kJ/mol và 607 kJ/mol. Tính biến thiên enthalpy chuẩn của phản ứng:
N2(g) + O2(g) → 2NO(g)
b) Giải thích vì sao nitrogen chỉ phản ứng với oxygen ở nhiệt độ cao hoặc khi có tia lửa điện.
Phương pháp giải:
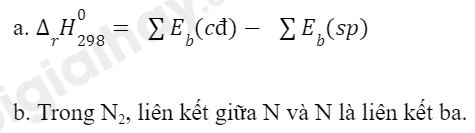
Lời giải:
![]()
b) Trong N2, liên kết giữa 2 nguyên tử là liên kết ba – một loại liên kết bển, cần 1 năng lượng rất lớn để phá vỡ liên kết đó.
=> N2 khá trơ về mặt hóa học và chỉ phản ứng với oxy khi có nhiệt đô cao hoặc có tia lửa điện
Lý thuyết Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết
Biến thiên enthalpy của phản ứng (mà các chất đều ở thể khí), bằng hiệu số giữa tổng năng lượng liên kết của các chất đầu và tổng năng lượng liên kết của các sản phẩm (ở cùng điều kiện nhiệt độ và áp suất).
Ở điều kiện chuẩn: = (cđ) – .
Ví dụ 1: Tính biến thiên enthalpy chuẩn của phản ứng
H2(g) + Cl2(g) 2HCl(g)
biết Eb (H–H) = 436 kJ/mol, Eb (Cl–Cl) = 243 kJ/mol, Eb (H–Cl) = 432 kJ/mol.
Hướng dẫn giải:
Biến thiên enthalpy chuẩn của phản ứng là:
= Eb (H–H) + Eb (Cl–Cl) – 2×Eb (H–Cl) = 436 + 243 – 2×432 = –185 (kJ).
Phản ứng tỏa nhiệt vì khi tạo thành 2 liên kết H–Cl tỏa ra năng lượng lớn hơn năng lượng cần thiết để phá vỡ liên kết H–H và Cl–Cl.
Ví dụ 2: Xác định biến thiên enthalpy chuẩn của phản ứng
C2H4(g) + H2(g) C2H6(g)
biết năng lượng liên kết (ở điều kiện chuẩn):

Hướng dẫn giải:
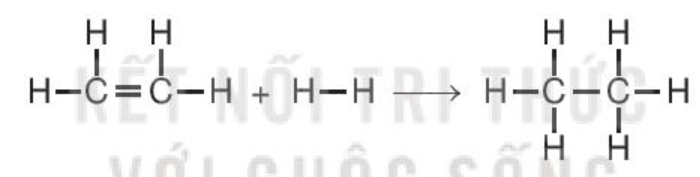
= Eb (C=C) + 4Eb (C–H) + Eb (H–H) – Eb (C–C) – 6Eb (C–H)
= 612 + 4×418 + 436 – 346 – 6×418 = –134 (kJ).
Xem thêm lời giải bài tập Hóa học lớp 10 Kết nối tri thức với cuộc sống hay, chi tiết khác:
Câu hỏi 2 trang 83 Hóa học 10: Cho các phương trình nhiệt hóa học:...
Câu hỏi 3 trang 83 Hóa học 10: Biết phản ứng đốt cháy khí carbon monoxide (CO) như sau:...
Câu hỏi 5 trang 86 Hóa học 10: Cho phản ứng:...
Xem thêm các bài giải SGK Hóa học lớp 10 Kết nối tri thức hay, chi tiết khác:
Bài 17: Biến thiên enthalpy trong các phản ứng hóa học