Với giải Câu hỏi 6 trang 61 Hóa học lớp 10 Chân trời sáng tạo chi tiết tron Bài 10: Liên kết cộng hóa trị giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 10. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 10 Bài 10: Liên kết cộng hóa trị
Câu hỏi 6 trang 61 Hóa học 10: Cho biết đặc điểm của nguyên tử “cho” và nguyên tử “nhận” trong phân tử có liên kết cho – nhận.
Phương pháp giải:
- Nguyên tử “cho” là nguyên tử đóng góp cặp electron chung
- Nguyên tử “nhận” là nguyên tử không đóng góp eletron
Lời giải:
- Đặc điểm của nguyên tử “cho”: còn cặp electron chưa tham gia liên kết => Đóng góp cặp electron chung
- Đặc điểm của nguyên tử “nhận”: có orbital trống, không chưa electron, số electron lớp ngoài cùng chưa đạt quy tắc octet => Không đóng góp electron mà nhận cặp eletron của nguyên tử “cho”
Lý thuyết Liên kết cho - nhận
- Liên kết cho – nhận là một trường hợp đặc biệt của liên kết cộng hóa trị, trong đó cặp electron chung chỉ do một nguyên tử đóng góp.
- Nguyên tử “cho” là nguyên tử đóng góp cặp electron chung, nguyên tử đó phải còn cặp electron chưa liên kết.
- Nguyên tử “nhận” là nguyên tử không đóng góp electron, nguyên tử đó phải còn orbital trống, không chứa electron.
- Để biễu diễn liên kết cho - nhận, một mũi tên được hướng từ nguyên tử cho sang nguyên tử nhận để phân biệt với các liên kết còn lại.
Ví dụ: Sự tạo thành liên kết cho - nhận trong ion NH4+
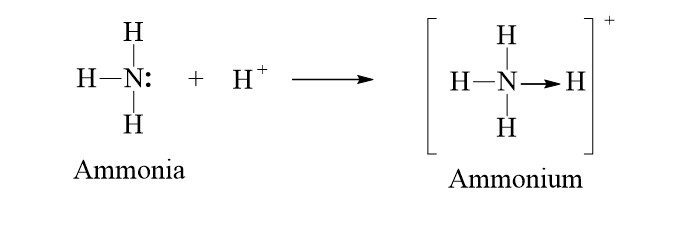
+ Trong phân tử NH3, nguyên tử N còn 1 cặp electron chưa tham gia liên kết, ion H+ có orbital trống, không chứa electron. Khi cho NH3 kết hợp với ion H+, nguyên tử N sử dụng một cặp electron chưa liên kết làm cặp electron chung với ion H+ tạo thành ion NH4+.
+ Nguyên tử N đóng góp cặp electron chung nên là nguyên tử cho.
+ Ion H+ không đóng góp electron, đóng vai trò nhận electron.
Xem thêm lời giải bài tập Hóa học 10 Chân trời sáng tạo hay, chi tiết khác:
Câu hỏi 3 trang 60 Hóa học 10: Thế nào là liên kết đơn, liên kết đôi và liên kết ba?...
Luyện tập 1 trang 60 Hóa học 10: Trình bày sự hình thành liên kết cộng hóa trị trong phân tử Cl2
Luyện tập 2 trang 60 Hóa học 10: Trình bày sự hình thành liên kết cộng hóa trị trong phân tử NH3
Luyện tập trang 63 Hóa học 10: Cho biết loại liên kết trong các phân tử MgCl2, CO2 và C2H4.
Câu hỏi 12 trang 63 Hóa học 10: Mô tả sự hình thành liên kết σ...
Câu hỏi 13 trang 64 Hóa học 10: Mô tả sự hình thành liên kết п...
Câu hỏi 16 trang 64 Hóa học 10: Sự xen phủ có sự tham gia của orbital nào luôn là xen phủ trục?...
Câu hỏi 20 trang 66 Hóa học 10: Trình bày các bước trong quá trình lắp ráp mô hình phân tử NH3...
Câu hỏi 21 trang 66 Hóa học 10: Mô hình sau biểu diễn phân tử CH4 hay phân tử CH3Cl?...
Bài 3 trang 66 Hóa học 10: Viết công thức Lewis của các phân tử CS2, SCl2 và CCl4
Bài 7 trang 66 Hóa học 10: Cho biết số liên kết σ và liên kết п trong phân tử acetylene (C2H2)....
Xem thêm các bài giải SGK Hóa học lớp 10 Chân trời sáng tạo hay, chi tiết khác:
Bài 11: Liên kết hydrogen và tương tác van der waals
Bài 12: Phản ứng oxi hóa – khử và ứng dụng trong cuộc sống
Bài 13: Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học